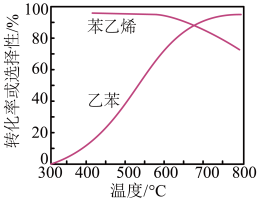
现代制备乙烯常用乙烷氧化裂解法,主反应为C2H6(g)+ O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]________ ,反应的最佳温度为_________ 。
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是___________ 。
 O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]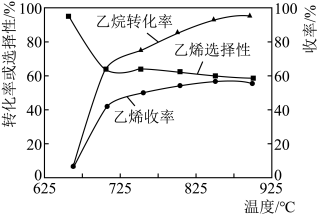
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是
2023高三·全国·专题练习 查看更多[2]
(已下线)题型四 平衡图像原因解释-备战2024年高考化学答题技巧与模板构建(已下线)06 常考题空6 平衡图像原因解释之转化率、产率变化分析 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
更新时间:2023-05-12 10:32:33
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】聚合反应的条件往往笼统表示为“高温、高压、催化剂”。从“又快又多”角度考虑,其中高温至少有利于____________ ,高压至少有利于___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】密闭容器中发生反应: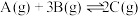
 ,根据下列
,根据下列 图象,回答问题:
图象,回答问题:
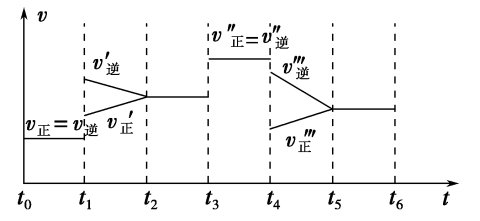
(1)下列时刻所改变的外界条件是
_______ ;
_______ ;
_______ 。
(2)反应速率最快的时间段是_______ 。
(3)下列措施能增大正反应速率的是_______。
 ,根据下列
,根据下列 图象,回答问题:
图象,回答问题:
(1)下列时刻所改变的外界条件是



(2)反应速率最快的时间段是
(3)下列措施能增大正反应速率的是_______。
A.通入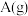 | B.分离出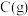 | C.降温 | D.增大容积 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】在工业上常用CO与H2合成甲醇,热化学方程式为CO(g)+2H2(g)  CH3OH(g) ΔH= −574.4kJ∙mol−1
CH3OH(g) ΔH= −574.4kJ∙mol−1
(1)在T1时,向容积为2 L的恒容容器中充入物质的量之和为3 mol的CO和H2,发生反应CO(g)+2H2(g) CH3OH(g),反应达到平衡时CH3OH(g)的体积分数[φ(CH3OH)]与
CH3OH(g),反应达到平衡时CH3OH(g)的体积分数[φ(CH3OH)]与 的关系如图1所示。
的关系如图1所示。
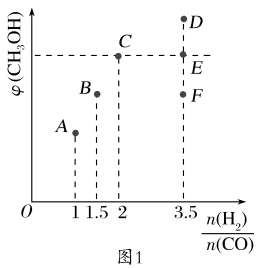
①当起始 =2时,经过5 min反应达到平衡,CO的转化率为0.6,则0~5 min内平均反应速率υ(H2)=
=2时,经过5 min反应达到平衡,CO的转化率为0.6,则0~5 min内平均反应速率υ(H2)=___________ 。若此刻再向容器中加入CO(g)和CH3OH(g)各0.4 mol,达到新平衡时H2的转化率将___________ (填“增大”“减小”或“不变”)。
②当 =3.5时,反应达到平衡后,CH3OH的体积分数可能是图1中的
=3.5时,反应达到平衡后,CH3OH的体积分数可能是图1中的___________ (填“D”“E”或“F”)点。
(2)在一容积可变的密闭容器中充有10 mol CO和20 mol H2.CO的平衡转化率[α(CO)]与温度(T)、压强(p)的关系如图2所示。
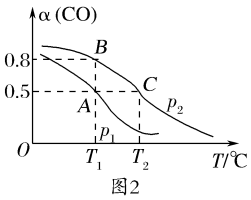
A、B、C三点对应的平衡常数KA、KB、KC的大小关系为___________ 。
 CH3OH(g) ΔH= −574.4kJ∙mol−1
CH3OH(g) ΔH= −574.4kJ∙mol−1(1)在T1时,向容积为2 L的恒容容器中充入物质的量之和为3 mol的CO和H2,发生反应CO(g)+2H2(g)
 CH3OH(g),反应达到平衡时CH3OH(g)的体积分数[φ(CH3OH)]与
CH3OH(g),反应达到平衡时CH3OH(g)的体积分数[φ(CH3OH)]与 的关系如图1所示。
的关系如图1所示。
①当起始
 =2时,经过5 min反应达到平衡,CO的转化率为0.6,则0~5 min内平均反应速率υ(H2)=
=2时,经过5 min反应达到平衡,CO的转化率为0.6,则0~5 min内平均反应速率υ(H2)=②当
 =3.5时,反应达到平衡后,CH3OH的体积分数可能是图1中的
=3.5时,反应达到平衡后,CH3OH的体积分数可能是图1中的(2)在一容积可变的密闭容器中充有10 mol CO和20 mol H2.CO的平衡转化率[α(CO)]与温度(T)、压强(p)的关系如图2所示。

A、B、C三点对应的平衡常数KA、KB、KC的大小关系为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】羰基硫(COS)广泛应用于农药、医药和其它化工生产中。
(1)氧和硫元素位于同一主族,其原子结构的共同点是______ ;羰基硫中含有的化学键类型是______ 。
(2)CO和H2S混合加热生成羰基硫的反应是CO(g) + H2S(g) COS(g) + H2(g),
COS(g) + H2(g),
请回答下列问题。
①某温度下,在1L恒容密闭容器中,加入10mol CO和10mol H2S,平衡时测得CO转化率为40%,则该温度下反应的平衡常数K=______ 。
②由下图分析该反应是_______ 反应(填“吸热”或“放热”)。
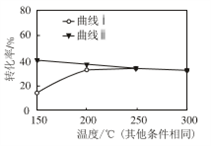

③请解释上图250℃以前, 曲线 ⅰ 变化的可能原因是_________ 。
(1)氧和硫元素位于同一主族,其原子结构的共同点是
(2)CO和H2S混合加热生成羰基硫的反应是CO(g) + H2S(g)
 COS(g) + H2(g),
COS(g) + H2(g),请回答下列问题。
①某温度下,在1L恒容密闭容器中,加入10mol CO和10mol H2S,平衡时测得CO转化率为40%,则该温度下反应的平衡常数K=
②由下图分析该反应是


③请解释上图250℃以前, 曲线 ⅰ 变化的可能原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
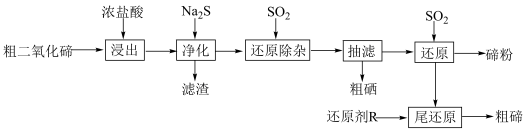
【推荐2】碲(Te)是半导体、红外探测等领域的重要战略元素。从阳极泥或冶炼烟尘中提取的粗二氧化碲中含有SeO2、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。
化学反应的吉布斯自由能变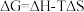 。SO2还原TeCl4和SeCl4的∆G随温度T的变化曲线如下图所示。则“还原除杂”步骤的温度不宜超过
。SO2还原TeCl4和SeCl4的∆G随温度T的变化曲线如下图所示。则“还原除杂”步骤的温度不宜超过_______ K,该步骤控制在此温度以下的原因是_______ 。
化学反应的吉布斯自由能变
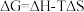 。SO2还原TeCl4和SeCl4的∆G随温度T的变化曲线如下图所示。则“还原除杂”步骤的温度不宜超过
。SO2还原TeCl4和SeCl4的∆G随温度T的变化曲线如下图所示。则“还原除杂”步骤的温度不宜超过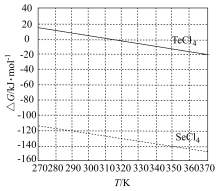
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】二甲醚(CH3OCH3)是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)⇌CH3OCH3(g)+H2O(g)△H=﹣23.5J•mol﹣1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.

①上述由甲醇制二甲醚的反应属于_____ 反应.在T1℃时,反应的平衡常数为___ ;
②相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4mol•L﹣1,c(H2O)=0.6mol•L﹣1、c(CH3OCH3)=1.2mol•L﹣1,此时正、逆反应速率的大小:v(正)_____ v(逆)(填“>”、“<”或“=”).

①上述由甲醇制二甲醚的反应属于
②相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4mol•L﹣1,c(H2O)=0.6mol•L﹣1、c(CH3OCH3)=1.2mol•L﹣1,此时正、逆反应速率的大小:v(正)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】氮的化合物在生产、生活中广泛存在。回答下列问题:
(1)用焦炭还原NO的反应为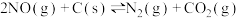 ,向容积均为1L的甲、乙、丙三个恒容、恒温(反应温度分别为400℃、400℃、
,向容积均为1L的甲、乙、丙三个恒容、恒温(反应温度分别为400℃、400℃、 )容器中分别加入足量的焦炭和一定量的NO,测得各容器中
)容器中分别加入足量的焦炭和一定量的NO,测得各容器中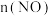 随反应时间
随反应时间 的变化情况如下表所示:
的变化情况如下表所示:
①该反应为___________ (填“放热”或“吸热”)反应,该反应的平衡常数的表达式为K=___________ 。
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率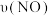 =
=___________ 。
(2)用焦炭还原 的反应为
的反应为 。在恒温(
。在恒温( )条件下,1mol
)条件下,1mol 和足量的焦炭发生该反应,测得平衡时
和足量的焦炭发生该反应,测得平衡时 和
和 的物质的量浓度与平衡总压的关系如图所示。
的物质的量浓度与平衡总压的关系如图所示。
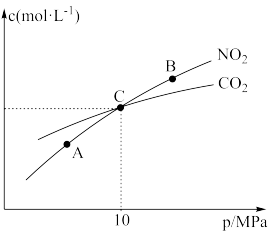
①A、B两点的浓度平衡常数关系为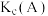
___________ 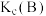 (填“<”“>”或“=”)。A、B、C三点中,
(填“<”“>”或“=”)。A、B、C三点中, 的平衡转化率最高的是
的平衡转化率最高的是___________ 点(填“A”“B”或“C”)。
②该温度( )下,反应的压强平衡常数
)下,反应的压强平衡常数 =
=___________ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)一定温度下,向1L恒容密闭容器中充入0.1mol NO和0.3mol CO,发生可逆反应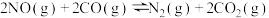 。能判断该反应达到平衡状态的依据是___________(填标号)。
。能判断该反应达到平衡状态的依据是___________(填标号)。
(1)用焦炭还原NO的反应为
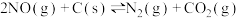 ,向容积均为1L的甲、乙、丙三个恒容、恒温(反应温度分别为400℃、400℃、
,向容积均为1L的甲、乙、丙三个恒容、恒温(反应温度分别为400℃、400℃、 )容器中分别加入足量的焦炭和一定量的NO,测得各容器中
)容器中分别加入足量的焦炭和一定量的NO,测得各容器中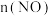 随反应时间
随反应时间 的变化情况如下表所示:
的变化情况如下表所示: /min /min | 0 | 40 | 80 | 120 | 160 |
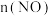 (甲容器)/mol (甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
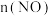 (乙容器)/mol (乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
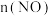 (丙容器)/mol (丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①该反应为
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率
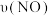 =
=(2)用焦炭还原
 的反应为
的反应为 。在恒温(
。在恒温( )条件下,1mol
)条件下,1mol 和足量的焦炭发生该反应,测得平衡时
和足量的焦炭发生该反应,测得平衡时 和
和 的物质的量浓度与平衡总压的关系如图所示。
的物质的量浓度与平衡总压的关系如图所示。
①A、B两点的浓度平衡常数关系为
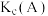
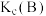 (填“<”“>”或“=”)。A、B、C三点中,
(填“<”“>”或“=”)。A、B、C三点中, 的平衡转化率最高的是
的平衡转化率最高的是②该温度(
 )下,反应的压强平衡常数
)下,反应的压强平衡常数 =
=(3)一定温度下,向1L恒容密闭容器中充入0.1mol NO和0.3mol CO,发生可逆反应
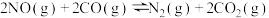 。能判断该反应达到平衡状态的依据是___________(填标号)。
。能判断该反应达到平衡状态的依据是___________(填标号)。A. | B.容器中混合气体的密度保持不变 |
C. | D.容器中混合气体的平均摩尔质量保持不变 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在某温度时,2A B+C 反应达到平衡,试回答:
B+C 反应达到平衡,试回答:
(1)若升高温度时,平衡向右移动,则正反应是______ 热反应;
(2)若增加或减少B,平衡不发生移动,则B的状态是_____ 态,因为___________ ;
(3)若B为气态,且增加体系的压强时,平衡不发生移动,则A为___ 态,C为___ 态,因为_______ 。
 B+C 反应达到平衡,试回答:
B+C 反应达到平衡,试回答:(1)若升高温度时,平衡向右移动,则正反应是
(2)若增加或减少B,平衡不发生移动,则B的状态是
(3)若B为气态,且增加体系的压强时,平衡不发生移动,则A为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现有反应mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)若加入B(容器体积不变),则A的转化率______ (填增大、减小或不变,下同),B的转化率______ 。
(2)若升高温度,则平衡时B、C的浓度之比c(B)/c(C)将______ (填增大、减小或不变)。
(3)若B是有色物质,A、C均无色,则加入C(容积不变)时混合物颜色________ (填变深、变浅或不变,下同),而维持容器内压强不变,充入Ne时,混合物的颜色_________ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)若加入B(容器体积不变),则A的转化率
(2)若升高温度,则平衡时B、C的浓度之比c(B)/c(C)将
(3)若B是有色物质,A、C均无色,则加入C(容积不变)时混合物颜色
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】对于反应:FeCl3(aq)+3KSCN(aq) Fe(SCN)3(aq)+3KCl(aq)增大体系的压强,平衡是否发生移动
Fe(SCN)3(aq)+3KCl(aq)增大体系的压强,平衡是否发生移动________ ?为什么________ ?
 Fe(SCN)3(aq)+3KCl(aq)增大体系的压强,平衡是否发生移动
Fe(SCN)3(aq)+3KCl(aq)增大体系的压强,平衡是否发生移动
您最近一年使用:0次

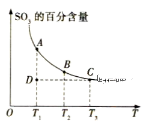
 "或"
"或" ")0;若在恒温恒压条件下向上述平衡体系中通入氦气,平衡
")0;若在恒温恒压条件下向上述平衡体系中通入氦气,平衡