现有反应

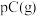 ,ΔH<0,达到平衡后,减小压强,混合物体系中C的质量分数减小,则:
,ΔH<0,达到平衡后,减小压强,混合物体系中C的质量分数减小,则:
(1)该反应
_______ p(填“>”“=”或“<”)。
(2)该反应在一定条件下能否自发进行_______ (填“能”或“不能”),说明理由_______ 。
(3)若B是有色物质,A、C均无色,则加入C(容器容积不变)时混合物的颜色_______ (填“变深”、“变浅”或“不变”);若容器容积不变,充入氖气时,容器内压强增大,这时化学平衡_______ 移动(填“正向”、“逆向”或“不”)。


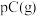 ,ΔH<0,达到平衡后,减小压强,混合物体系中C的质量分数减小,则:
,ΔH<0,达到平衡后,减小压强,混合物体系中C的质量分数减小,则:(1)该反应

(2)该反应在一定条件下能否自发进行
(3)若B是有色物质,A、C均无色,则加入C(容器容积不变)时混合物的颜色
更新时间:2022-11-10 14:35:35
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】反应mA+nB pC,某温度下达到平衡时,
pC,某温度下达到平衡时,
(1)若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系为____ 。
(2)若c为气体,且m+n=p,在加压时,化学平衡发生移动,则平衡必定是向____ 方向移动。
(3)如果在体系中增大或减小B的量平衡均不移动,则B为____ 态。
(4)若升高温度,A的转化率降低,此反应的逆反应是____ 热反应。
 pC,某温度下达到平衡时,
pC,某温度下达到平衡时,(1)若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系为
(2)若c为气体,且m+n=p,在加压时,化学平衡发生移动,则平衡必定是向
(3)如果在体系中增大或减小B的量平衡均不移动,则B为
(4)若升高温度,A的转化率降低,此反应的逆反应是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】恒温刚性密闭容器中通入气体分压比为p(C3H8)∶p(O2)∶p(N2)=2∶13∶85的混合气体,已知某反应条件下只发生如下反应(k,k′为速率常数):
反应II:2C3H8(g)+O2(g)=2C3H6(g)+2H2O(g) k
反应III:2C3H6(g)+9O2(g)=6CO2(g)+6H2O(g) k′
实验测得丙烯的净生成速率方程为v(C3H6)=kp(C3H8)-k′p(C3H6),可推测丙烯的浓度随时间的变化趋势为_______ ,其理由是______ 。
反应II:2C3H8(g)+O2(g)=2C3H6(g)+2H2O(g) k
反应III:2C3H6(g)+9O2(g)=6CO2(g)+6H2O(g) k′
实验测得丙烯的净生成速率方程为v(C3H6)=kp(C3H8)-k′p(C3H6),可推测丙烯的浓度随时间的变化趋势为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】利用反应CO(g)+H2O(g) H2(g)+CO2(g)可得到清洁能源H2。
H2(g)+CO2(g)可得到清洁能源H2。
(1)该反应化学平衡常数表达式K=____ 。
(2)该反应的平衡常数随温度的变化如表:
从上表可以推断:此反应是____ (填“吸热”或“放热”)反应。
(3)830℃时,向容积为2L的密闭容器中充入1molCO与1molH2O,2min时CO为0.6mol。2min内v(CO2)=____ ,此时反应进行的方向是___ ,依据是____ ,可以判断该反应达到平衡的标志是____ (填字母)。
a.体系的压强不再发生变化 b.混合气体的密度不变
c.CO的消耗速率与CO2的消耗速率相等 d.各组分的物质的量浓度不再改变
 H2(g)+CO2(g)可得到清洁能源H2。
H2(g)+CO2(g)可得到清洁能源H2。(1)该反应化学平衡常数表达式K=
(2)该反应的平衡常数随温度的变化如表:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(3)830℃时,向容积为2L的密闭容器中充入1molCO与1molH2O,2min时CO为0.6mol。2min内v(CO2)=
a.体系的压强不再发生变化 b.混合气体的密度不变
c.CO的消耗速率与CO2的消耗速率相等 d.各组分的物质的量浓度不再改变
您最近一年使用:0次
填空题
|
较易
(0.85)
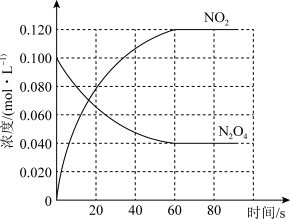
【推荐1】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:
(1)100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为___________ mol·L-1·s-1,平衡时NO2的体积分数为___________ 。升高温度,混合气体的平均相对分子质量将___________ (填“增大”、“减小”或“不变”)
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,经10s又达到平衡。T___________ 100℃(填“大于”“小于”),判断理由是___________ 。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向(填“正反应”或“逆反应”)___________ 方向移动,判断理由是___________ 。
 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:
(1)100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,经10s又达到平衡。T
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向(填“正反应”或“逆反应”)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】3A 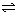 3B+C在某一温度时,达到平衡。
3B+C在某一温度时,达到平衡。
(1)若温度升高,平衡向正反应方向移动,则正反应是______ 热反应;
(2)若温度固定,扩大容器的体积,平衡向逆反应方向移动,则A一定呈_______ 态;
(3)若A是气态时,加压时,平衡不移动,则B为______ 态,C为_____ 态。
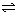 3B+C在某一温度时,达到平衡。
3B+C在某一温度时,达到平衡。(1)若温度升高,平衡向正反应方向移动,则正反应是
(2)若温度固定,扩大容器的体积,平衡向逆反应方向移动,则A一定呈
(3)若A是气态时,加压时,平衡不移动,则B为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】【情境问题思考】观察下列几个自发进行的化学反应。
4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) ΔH=-444.3kJ·mol-1
②2Na(s)+2H2O(l)=2NaOH(aq)+H2(g) ΔH=-368kJ·mol-1
③2H2O2(l)=2H2(g)+O2(g) ΔH=-571.6kJ·mol-1
④NH4HCO3(s)+CH3COOH(aq)=CO2(g)+CH3COONH4(aq)+H2O(l) ΔH=+37.30kJ·mol-1
(1)放热反应是否都能自发进行____ ?吸热反应是否都不能自发进行____ ?
(2)能否仅用反应焓变来判断反应能否自发进行____ ?
4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) ΔH=-444.3kJ·mol-1
②2Na(s)+2H2O(l)=2NaOH(aq)+H2(g) ΔH=-368kJ·mol-1
③2H2O2(l)=2H2(g)+O2(g) ΔH=-571.6kJ·mol-1
④NH4HCO3(s)+CH3COOH(aq)=CO2(g)+CH3COONH4(aq)+H2O(l) ΔH=+37.30kJ·mol-1
(1)放热反应是否都能自发进行
(2)能否仅用反应焓变来判断反应能否自发进行
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】将 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:
①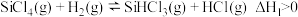
②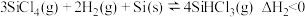
③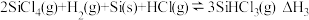
已知体系自由能变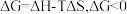 时反应自发进行。三个氢化反应的
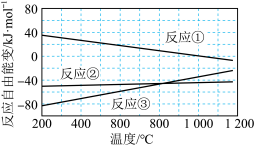
时反应自发进行。三个氢化反应的 与温度的关系如图所示,可知:反应①能自发进行的最低温度是
与温度的关系如图所示,可知:反应①能自发进行的最低温度是_______ ;相同温度下,反应②比反应①的 小,主要原因是
小,主要原因是_________ 。
 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:①
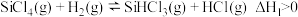
②
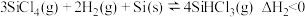
③
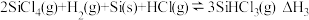
已知体系自由能变
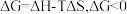 时反应自发进行。三个氢化反应的
时反应自发进行。三个氢化反应的 与温度的关系如图所示,可知:反应①能自发进行的最低温度是
与温度的关系如图所示,可知:反应①能自发进行的最低温度是 小,主要原因是
小,主要原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】根据所学知识和已有生活经验,分析以下反应在给定温度下能否正向自发进行,将这些反应的焓变和熵变“>0”或“<0”填入表格。
| 化学反应 | 正向是否自发 | ΔH | ΔS |
| 常温Zn(s)+2HCl(aq)=ZnCl2(aq)+H2(g) | |||
| 常温6CO2(g)+6H2O(l)=C6H12O6(s)+6O2(g) | >0 | <0 | |
| 常温NH3(g)+HCl(g)=NH4Cl(s) | |||
| 常温C(s)+CO2(g)=2CO(g) |
您最近一年使用:0次



