 的电离方程式为
的电离方程式为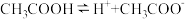 ,25℃时,
,25℃时, 溶液的
溶液的 。下列说法正确的是( )
。下列说法正确的是( )A.向该溶液中滴加几滴浓盐酸,平衡逆向移动, 减小 减小 |
B.向该溶液中加少量 固体,平衡正向移动 固体,平衡正向移动 |
C.该温度下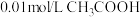 溶液的 溶液的 |
D.升高温度, 增大, 增大, 变大 变大 |
17-18高二下·北京朝阳·期末 查看更多[16]
山东省济南市商河县第一中学2020-2021学年高二10月月考化学试题辽宁省辽河油田第二高级中学2021-2022学年高二上学期开学考试化学试题选择性必修1(SJ)专题3第一单元课时2 电离平衡常数云南省丽江市第一中学2020-2021学年高二下学期期中考试化学试题福建省南安市柳城中学2020-2021学年高二上学期第二次月考化学试题贵州省北师大遵义附属高级中学2020-2021学年高二上学期期中考试化学试题人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第一节 电离平衡 课时2 电离平衡常数鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第2节 弱电解质的电离盐类的水解甘肃省兰州大学附属中学(33中)2019-2020学年高二上学期期中考试化学试题江西省新余市八校2019-2020学年高二上学期期中考试化学试题江西省南康中学2019-2020学年高二上学期期中考试化学试题【全国百强校】江西省南昌市第二中学2018-2019学年高二上学期期中考试化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二(理)上学期期中考试化学试题新疆维吾尔自治区兵团第二师华山中学2018-2019学年高二上学期第一次调研考试化学试题【全国百强校】内蒙古集宁一中(西校区)2018-2019学年高二上学期第一次月考理科综合化学试题【全国区级联考】北京市朝阳区2017-2018学年高二下学期期末考试化学试题
更新时间:2020-09-17 19:11:27
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】0.1 mol·L-1氨水10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是
①电离程度增大 ②c(NH3·H2O)增大 ③NH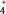 数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥c(H+)增大
数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥c(H+)增大
①电离程度增大 ②c(NH3·H2O)增大 ③NH
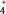 数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥c(H+)增大
数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥c(H+)增大| A.①②③ | B.①③⑤ | C.①③⑥ | D.②④⑥ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在0.01mol·L-1 的醋酸溶液中逐渐加入冰醋酸至1mol·L-1,随着浓度的增加,在一定时间内始终保持减小趋势的是
| A.c(H+) | B.c(CH3COO-) |
| C.c(H+)/c(CH3COOH)的比值 | D.c(CH3COOH)/c(H+)的比值 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关物质的量浓度的说法正确的是
A.将4g NaOH溶解在1L水中,可以得到 的NaOH溶液 的NaOH溶液 |
B.将 的NaOH溶液分成两等份,其物质的量浓度变为原来的一半 的NaOH溶液分成两等份,其物质的量浓度变为原来的一半 |
C.将 的NaOH溶液分成两等份,其溶质的物质的量变为原来的一半 的NaOH溶液分成两等份,其溶质的物质的量变为原来的一半 |
D.向50mL  NaOH溶液中加入50mL水,可以得到 NaOH溶液中加入50mL水,可以得到 的NaOH溶液 的NaOH溶液 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下HF的电离常数Ka=3.3×10-4 ,CaF2的溶度积常数Ksp=1.46×10-10。在该温度下取浓度为0.31 mol·L-1的HF与浓度为0.002 mol·L-1的CaCl2溶液等体积混合。下列说法正确的是
| A.该温度下,0.31 mol·L-1的HF溶液的pH=2 |
| B.升高温度或增大浓度,HF的电离平衡常数都将增大 |
| C.两溶液混合不会产生沉淀 |
| D.向饱和的CaF2溶液中加入少量CaCl2固体后,溶度积常数Ksp一定比之前减小 |
您最近半年使用:0次

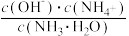 不变
不变 的两种钾盐
的两种钾盐 溶液中加水,溶液的
溶液中加水,溶液的 与稀释倍数
与稀释倍数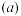 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是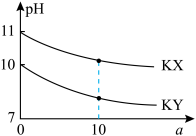
 的水解常数
的水解常数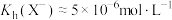
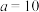 时,
时, 溶液中
溶液中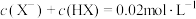
 的
的 溶液中离子总浓度:
溶液中离子总浓度:


