煤和石油在燃烧时会产生NO2,为保护环境需要脱硝处理。某种脱硝方法中利用了如下反应。
8NH3+6NO2 7N2+12H2O
7N2+12H2O
(1)作为还原剂的物质是____ ,NO2中氮元素的化合价___ (填“升高”或“降低”)。
(2)若反应中消耗了8molNH3,则可脱除NO2的物质的量为___ mol,转移电子的物质的量为___ mol。
8NH3+6NO2
 7N2+12H2O
7N2+12H2O(1)作为还原剂的物质是
(2)若反应中消耗了8molNH3,则可脱除NO2的物质的量为
更新时间:2020/09/21 10:18:03
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
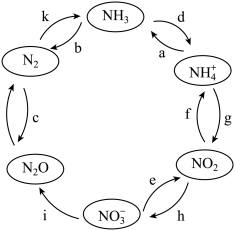
【推荐1】一定条件下,氮元素可发生如图所示的循环转化。___________ (填字母);转化过程为非氧化还原反应的是___________ ,过程h的化学方程式为:___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】在明代宋应星所著的《天工开物》中,有关于火法炼锌的工艺记载:“每炉甘石(主要成分为碳酸锌)十斤,装载入一泥罐内,∙∙∙∙∙∙然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团。冷定毁罐取出。∙∙∙∙∙∙即倭铅也。”
(1)请完成上述火法炼锌反应的化学方程:
ZnCO3+2C
_____ +______ CO↑
(2)在该反应中,还原剂是___________ (填化学式,下同),氧化剂是______ 。
(3)利用生成的锌粒,加入稀硫酸会发生以下反应:Zn+H2SO4=ZnSO4+H2↑,请用“双线桥法”标出电子转移的方向和数目:___________ 。
(1)请完成上述火法炼锌反应的化学方程:
ZnCO3+2C

(2)在该反应中,还原剂是
(3)利用生成的锌粒,加入稀硫酸会发生以下反应:Zn+H2SO4=ZnSO4+H2↑,请用“双线桥法”标出电子转移的方向和数目:
您最近一年使用:0次
【推荐3】在Cu+HNO3 ———— Cu(NO3)2+NO↑+4H2O反应中,
(1)______ 元素被氧化, ______ 是氧化剂;
(2)______ 是氧化产物, ______ 发生氧化反应;
(3)被还原的HNO3与参加反应的HNO3物质的量之比是______ ;
(4)用双线桥标出该反应电子转移的方向和数目:
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O_____________________________________ ;
(5)当有8mol HNO3被还原时,反应转移___________ 个电子;
(6)写出该反应的离子反应方程式___________________________ 。
(1)
(2)
(3)被还原的HNO3与参加反应的HNO3物质的量之比是
(4)用双线桥标出该反应电子转移的方向和数目:
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(5)当有8mol HNO3被还原时,反应转移
(6)写出该反应的离子反应方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题
(1)野外焊接铁轨常常采用铝热反应。已知铝热反应的化学方程式为 。该反应所属基本反应类型是
。该反应所属基本反应类型是_______ ,在反应中铁元素的化合价_______ (填“升高”或“降低”),该元素的原子_______ (填“失去”或“得到”)电子。发生氧化反应的是_______ (填化学式,下同),发生还原反应的是_______ 。
(2)在反应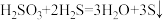 中,被氧化与被还原元素的原子个数比为
中,被氧化与被还原元素的原子个数比为_______ 。
(1)野外焊接铁轨常常采用铝热反应。已知铝热反应的化学方程式为
 。该反应所属基本反应类型是
。该反应所属基本反应类型是(2)在反应
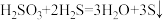 中,被氧化与被还原元素的原子个数比为
中,被氧化与被还原元素的原子个数比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收。
(1)在人体中进行的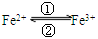 转化时,②中的Fe3+作
转化时,②中的Fe3+作______________ 剂;
(2)“服用维生素C,可使食物中的Fe3+ 还原成Fe2+”这句话指出,维生素C在这一反应中作_____ 剂,具有__________________ 性。
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为______________________________________ 。
(1)在人体中进行的
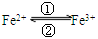 转化时,②中的Fe3+作
转化时,②中的Fe3+作(2)“服用维生素C,可使食物中的Fe3+ 还原成Fe2+”这句话指出,维生素C在这一反应中作
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:
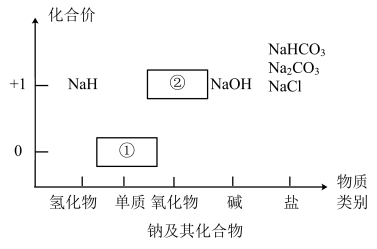
(1)物质①与水反应的离子方程式为_________ ,所以通常将其保存在_________ 中。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式并用双线桥表示出电子转移的方向和数目_________ 。
(3)从核心元素价态的视角看,NaH中H元素的化合价为_________ ,从H元素的价态分析,NaH常用作_________ (填“氧化剂”或“还原剂”)。
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
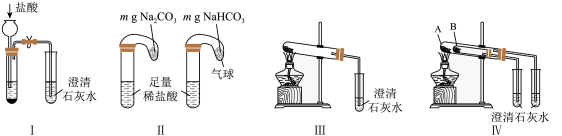
①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是_________ (填装置序号)。
②图Ⅲ、Ⅳ中_________ 能更好说明二者的稳定性(填装置序号),写出Ⅳ中使澄清石灰水变浑浊的离子方程式_________ 。

(1)物质①与水反应的离子方程式为
(2)写出淡黄色固体②与二氧化碳反应的化学方程式并用双线桥表示出电子转移的方向和数目
(3)从核心元素价态的视角看,NaH中H元素的化合价为
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。

①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是
②图Ⅲ、Ⅳ中
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】根据所学知识,回答下列问题。
(1)汽车尾气中常含有NO、CO等气体,在催化剂的作用下NO和CO可反应生成 和
和 ,请写出该反应的化学方程式:
,请写出该反应的化学方程式:___________ 。
(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:___________ 。
(3)胶体和溶液的本质区别是___________ (填标号)。
A.能否发生电泳 B.分散质粒子的直径大小不同 C.能否产生丁达尔效应
(4)下列状态的物质既属于电解质又能导电的是___________(填标号)。
(5)饮用水中的 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: ,上述反应中若生成标准状况下
,上述反应中若生成标准状况下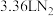 ,则转移的电子数目为
,则转移的电子数目为___________ 。
(1)汽车尾气中常含有NO、CO等气体,在催化剂的作用下NO和CO可反应生成
 和
和 ,请写出该反应的化学方程式:
,请写出该反应的化学方程式:(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:
(3)胶体和溶液的本质区别是
A.能否发生电泳 B.分散质粒子的直径大小不同 C.能否产生丁达尔效应
(4)下列状态的物质既属于电解质又能导电的是___________(填标号)。
| A.熔融的NaCl | B.纯净的矿泉水 | C.某品牌的饮料 | D.熟石灰固体 |
 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: ,上述反应中若生成标准状况下
,上述反应中若生成标准状况下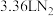 ,则转移的电子数目为
,则转移的电子数目为
您最近一年使用:0次
【推荐2】如下图在衬白纸的玻璃片中央放置适量的KMnO4颗粒,在周围分别滴加一滴含有酚酞的澄清石灰水、FeCl2溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿。提示:实验室中所用的少量氯气可以用下述原理制取:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应在常温下即能进行。
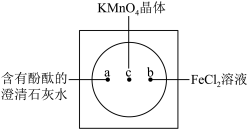
(1)氧化剂与还原剂物质的量之比为____________ ,氧化产物为_______ 。
(2)产生0.1molCl2,则转移电子的物质的量为______ mol。
(3)b处离子方程式是___________ 。
(4)高锰酸钾标准溶液经常用来滴定测量物质的含量。配平并完成下列高锰酸钾滴定草酸反应的离子方程式:_____  +
+______ H2C2O4+______  =
=____  +
+_____ CO2↑+___________

(1)氧化剂与还原剂物质的量之比为
(2)产生0.1molCl2,则转移电子的物质的量为
(3)b处离子方程式是
(4)高锰酸钾标准溶液经常用来滴定测量物质的含量。配平并完成下列高锰酸钾滴定草酸反应的离子方程式:
 +
+ =
= +
+
您最近一年使用:0次



