部分中学化学常见元素原子结构及性质如下表所示。
(1)这五种元素的原子半径由大到小的顺序为_______________ (用元素符号表示)。
(2)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的实验方案为________ 。E与C组成的两种化合物M、N,所含电子数分别与X、Y相等,M中共用电子对对数为_______________ ,N的结构式为_______________ 。
(3)A与C可以形成一种新型陶瓷材料,机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是_______________ 。
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发此种陶瓷的全陶发动机替代同类型金属发动机
D.此种陶瓷的开发受到资源的限制,没有发展前途
| 序号 | 元素 | 结构及性质 |
| ① | A | A为地壳中含量仅次于氧的非金属元素,其单质晶体结构与金刚石相似 |
| ② | B | B原子最外层电子数是内层电子总数的1/5 |
| ③ | C | C是常用化肥的主要元素,单质常温下呈气态 |
| ④ | D | 通常情况下,D在化合物中显负价,A、B、C都能与D形成中学常见化合物 |
| ⑤ | E | E是宇宙中最丰富的元素 |
(1)这五种元素的原子半径由大到小的顺序为
(2)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的实验方案为
(3)A与C可以形成一种新型陶瓷材料,机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发此种陶瓷的全陶发动机替代同类型金属发动机
D.此种陶瓷的开发受到资源的限制,没有发展前途
更新时间:2020-09-25 09:20:45
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】判断
(1)同周期元素,从左到右,原子半径逐渐减小,离子半径也逐渐减小____________
(2)第二周期元素从左到右,最高正价从+1递增到+7____________
(3)元素的原子得电子越多,非金属性越强;失电子越多,金属性越强____________
(4)元素的氧化物对应的水化物酸性越强,非金属性越强;碱性越强,金属性越强____________
(5)已知Ra是第7周期ⅡA族的元素,故Ra(OH)2的碱性比Mg(OH)2的碱性强____________
(6)已知As是第4周期ⅤA族的元素,故AsH3的稳定性比NH3的稳定性弱____________
(7)已知Cs的原子半径比Na的原子半径大,故Cs与水反应比Na与水反应更剧烈____________
(8)已知Cl的非金属性比S的强,故HClO的酸性比H2SO3的强____________
(9)第ⅠA族与第ⅦA族元素间可形成共价化合物或离子化合物____________
(10)第二周期元素从左到右,最高正价从+1递增到+7____________
(11)同主族元素的简单阴离子还原性越强,水解程度越大____________
(12)同周期金属元素的化合价越高,其原子失电子能力越强____________
(13)由水溶液的酸性:HCl>HF,不能推断出元素的非金属性:Cl>F____________
(14)人们可以在周期表的过渡元素中寻找催化剂和耐腐蚀、耐高温的合金材料____________
(15)短周期元素正化合价数值和其族序数相同____________
(16)短周期元素形成的微粒X2-和Y2+核外电子排布相同,离子半径:X2->Y2+____________
(1)同周期元素,从左到右,原子半径逐渐减小,离子半径也逐渐减小
(2)第二周期元素从左到右,最高正价从+1递增到+7
(3)元素的原子得电子越多,非金属性越强;失电子越多,金属性越强
(4)元素的氧化物对应的水化物酸性越强,非金属性越强;碱性越强,金属性越强
(5)已知Ra是第7周期ⅡA族的元素,故Ra(OH)2的碱性比Mg(OH)2的碱性强
(6)已知As是第4周期ⅤA族的元素,故AsH3的稳定性比NH3的稳定性弱
(7)已知Cs的原子半径比Na的原子半径大,故Cs与水反应比Na与水反应更剧烈
(8)已知Cl的非金属性比S的强,故HClO的酸性比H2SO3的强
(9)第ⅠA族与第ⅦA族元素间可形成共价化合物或离子化合物
(10)第二周期元素从左到右,最高正价从+1递增到+7
(11)同主族元素的简单阴离子还原性越强,水解程度越大
(12)同周期金属元素的化合价越高,其原子失电子能力越强
(13)由水溶液的酸性:HCl>HF,不能推断出元素的非金属性:Cl>F
(14)人们可以在周期表的过渡元素中寻找催化剂和耐腐蚀、耐高温的合金材料
(15)短周期元素正化合价数值和其族序数相同
(16)短周期元素形成的微粒X2-和Y2+核外电子排布相同,离子半径:X2->Y2+
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】现有A、B、C、D、E、F、G七种短周期主族元素,原子序数依次增大。A与C形成的化合物能使湿润的红色石蕊试纸变蓝;D是地壳中含量最多的元素;D、F原子的最外层电子数相等;E的焰色反应呈黄色;B元素的一种同位素在考古时可用于测定一些文物的年代。请回答下列问题:(注意回答问题时均用元素符号表示)
(1)元素B在周期表中的位置:___________ 。
(2)元素A与C组成的10电子的阳离子的电子式:___________ 。元素A与D组成的18电子分子的结构式:___________ 。
(3) 和
和 形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:
形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:___________ 。
(4)D和F的简单气态氢化物沸点比较高的是:___________ (写分子式),原因:______ 。
(5)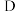 、
、 、
、 、G的简单离子半径由小到大的顺序为
、G的简单离子半径由小到大的顺序为___________ (用离子符号表示)。
(6)用电子式表示化合物E2D的形成过程:___________ 。
(1)元素B在周期表中的位置:
(2)元素A与C组成的10电子的阳离子的电子式:
(3)
 和
和 形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:
形成的一种化合物与A2D发生氧化还原反应,写出该反应的化学方程式并用双线桥标出电子转移的方向与数目:(4)D和F的简单气态氢化物沸点比较高的是:
(5)
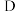 、
、 、
、 、G的简单离子半径由小到大的顺序为
、G的简单离子半径由小到大的顺序为(6)用电子式表示化合物E2D的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,针对表中的①~⑧种元素,请按要求填写下列空白:
(1)在元素①②⑤⑥⑦⑧对应的最高价氧化物的水化物中,碱性最强的化合物的电子式 是:___________ ;酸性最强的化合物的化学式为:___________
(2)写出元素②的最简单氢化物的结构式 ___________ ;写出N2H4结构式___________ 。
(3)④⑤⑥⑦四种元素的简单离子半径从大到小排序___________ (用离子符号表示);
(4)写出元素⑥的最高价氧化物与元素⑤的最高价氧化物的水化物反应的离子方程式___________ ;
(5)写出元素③的常见氢化物和它的最高价氧化物的水化物反应的化学方程式___________ ;
(6)用电子式表示⑤与⑦组成化合物的形成过程___________ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | ① | ② | ③ | ④ | |||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)写出元素②的最简单氢化物的
(3)④⑤⑥⑦四种元素的简单离子半径从大到小排序
(4)写出元素⑥的最高价氧化物与元素⑤的最高价氧化物的水化物反应的离子方程式
(5)写出元素③的常见氢化物和它的最高价氧化物的水化物反应的化学方程式
(6)用电子式表示⑤与⑦组成化合物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有A、B、C、D四种元素,其中A和B原子都有1个未成对电子,A+比B-少一个电子层。B原子得一个电子填入3p轨道后,3p轨道已充满,C原子的p轨道中有3个未成对电子,其气态氢化物的水溶液的pH在同族氢化物中最大,D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D 40%,且其核内质子数等于中子数,据此判断:
(1)A是_______ ,B是_______ ,C是_______ ,D是_______ 。(填元素名称)
(2)B-的电子排布式_______ ,A+ 的结构示意图_______ ,D原子的价层电子排布图_______ 。
(3)题中元素“C”的原子中有_______ 种不同运动状态的电子,能量最高的是_______ 电子,其原子轨道呈_______ 状。
(4)用电子式表示化合物AB的形成过程_______ 。
(1)A是
(2)B-的电子排布式
(3)题中元素“C”的原子中有
(4)用电子式表示化合物AB的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】短周期主族元素A、B、C、D、E、F的原子序数依次递增,A是自然界中形成化合物种类最多的元素,且A、B两元素在元素周期表中相邻,B、C、E原子的最外层电子数之和为13,C原子最外层电子数是E原子最外层电子数的3倍,B、F原子最外层电子数之和等于C、E原子最外层电子数之和,D在同周期元素中原子半径最大。
请回答下列问题:
(1)A的元素符号为_______ ,其在元素周期表的位置:第______ 周期,第______ 族。
(2)元素A、B形成的最简单的气态氢化物稳定性较强的是_______ (填化学式),元素C和D可形成化合物D2C2,其电子式为_______ 。
(3)F的单质加入到D的最高价氧化物对应水化物的溶液中,发生反应的离子方程式为________ ;上述反应的气体产物和C元素的单质设计成的燃料电池已用于航天飞机。试写出以30%KOH溶液为电解质溶液的这种电池在工作时负极的电极反应式为________ 。
(4)工业制取E的化学反应方程式为_______ 。
请回答下列问题:
(1)A的元素符号为
(2)元素A、B形成的最简单的气态氢化物稳定性较强的是
(3)F的单质加入到D的最高价氧化物对应水化物的溶液中,发生反应的离子方程式为
(4)工业制取E的化学反应方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】甲、乙、丙、丁四种短周期元素的位置如图所示(其中乙、丙、丁的位置未标出)。已知四种元素的原子序数之和为36,乙的原子序数与甲、丁原子序数之和相等。
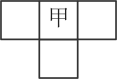
(1)甲元素在周期表中的位置为__________ 。
(2)丙、丁可形成AB2型化合物,其化学式为_______ 。
(3)丙是自然界中形成化合物种类最多的元素,则丙是________ (填名称),其单质与甲元素的最高价氧化物对应水化物的浓溶液共热时反应的化学方程式是__________ 。
(4)若甲、乙、丙、丁四种元素两两化合时,丁与其他三种元素得到的化合物种类最多,则丁是_______ (填元素符号)。

(1)甲元素在周期表中的位置为
(2)丙、丁可形成AB2型化合物,其化学式为
(3)丙是自然界中形成化合物种类最多的元素,则丙是
(4)若甲、乙、丙、丁四种元素两两化合时,丁与其他三种元素得到的化合物种类最多,则丁是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D四种元素都是短周期元素。A元素的离子具有黄色的焰色反应。B离子带有2个单位正电荷,且B元素的离子结构和Ne具有相同的电子层排布。H2在C单质中燃烧产生苍白色火焰,D元素原子的电子层结构里,最外层电子数是次外层电子数的3倍。根据上述条件回答:
(1)元素C位于第___ 周期第___ 族。
(2)A是___ 元素,B是___ 元素,D是___ 元素。
(3)A与D形成稳定的化合物的化学式为___ ,此化合物与水反应的化学方程式为___ 。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为___ 。
(1)元素C位于第
(2)A是
(3)A与D形成稳定的化合物的化学式为
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有四种短周期元素,它们的结构、性质等信息如表所述:
(1)X元素在周期表中的位置_____ ;其相对分子质量最小的气态氢化物常用作_____ 。
(2)用电子式表示X最高价氧化物的形成过程_____________________ 。
(3)Y的最高价氧化物对应水化物的电子式________ 。
(4)Z的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式为______________ 。
(5)举出实例说明M的非金属性比X强:_____________ 。
元素 | 结构、性质等信息 |
X | 构成有机物的核心元素,该元素的一种氧化物和气态氢化物都是典型的温室气体 |
Y | 短周期中(除稀有气体外)原子半径最大的元素,该单质与冷水剧烈反应 |
Z | 与Y同周期,其最高价氧化物的水化物呈两性 |
M | 海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒剂和杀菌剂 |
(2)用电子式表示X最高价氧化物的形成过程
(3)Y的最高价氧化物对应水化物的电子式
(4)Z的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式为
(5)举出实例说明M的非金属性比X强:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D 同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是_________ ,非金属性最强的是_________ (填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是___________ (用化学式表示);
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为______________ ,其中存在的化学键类型为_______________ ;
(4)比较D、E最高价氧化物的水化物的酸性大小关系_____________________ ; (用化学式表示)
(5)单质E与水反应的离子方程式为_________________________ ;
(6)C最高价氧化物对应水化物与E最高价氧化物对应水化物反应的离子方程式____________ 。
(1)五种元素中,原子半径最大的是
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为
(4)比较D、E最高价氧化物的水化物的酸性大小关系
(5)单质E与水反应的离子方程式为
(6)C最高价氧化物对应水化物与E最高价氧化物对应水化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,请根据元素①~⑧所处的位置回答下列问题:
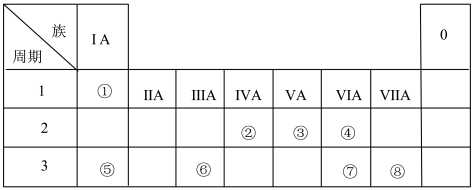
(1)元素⑦的原子结构示意图为___________ ,元素④⑦的最简单氢化物的稳定性关系为___________ (填化学式)。
(2)34号元素Se与④同主族,则Se在元素周期表中的位置为___________
(3)元素①~⑧形成的物质中,最高价氧化物的水化物碱性最强的是___________ ,最高价氧化物的水化物酸性最强的是___________ (填化学式)。
(4)由元素④⑤组成原子个数比为 的化合物中含
的化合物中含___________ (填化学键类型)
(5)由③④⑥可形成一种高硬度、耐高温的防弹材料,这三种元素的简单离子半径由大到小的排列顺序是___________ 。(填离子符号)
(6)可用于比较元素⑦与⑧非金属性相对强弱的事实是___________ 。

(1)元素⑦的原子结构示意图为
(2)34号元素Se与④同主族,则Se在元素周期表中的位置为
(3)元素①~⑧形成的物质中,最高价氧化物的水化物碱性最强的是
(4)由元素④⑤组成原子个数比为
 的化合物中含
的化合物中含(5)由③④⑥可形成一种高硬度、耐高温的防弹材料,这三种元素的简单离子半径由大到小的排列顺序是
(6)可用于比较元素⑦与⑧非金属性相对强弱的事实是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】表为元素周期表的一部分(短周期),其中每个数字序号代表一种元素。
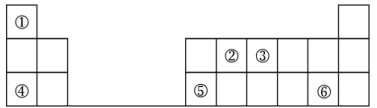
请按要求回答下列问题:
(1)④⑤⑥三种元素相比较,金属性最强的是___________ (填元素符号)。
(2)②③的原子半径大小关系是:②___________ ③(填“>”“<”或“=”)。
(3)③的单质的结构式为___________ 。
(4)元素⑥的最高价氧化物对应的水化物的化学式为___________ 。
(5)请任意举出一例证明元素③的最高价氧化物对应的水化物的溶液具有强氧化性___________ 。
(6)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可观察到大量的白烟,写出产生该现象的化学方程式:___________ 。

请按要求回答下列问题:
(1)④⑤⑥三种元素相比较,金属性最强的是
(2)②③的原子半径大小关系是:②
(3)③的单质的结构式为
(4)元素⑥的最高价氧化物对应的水化物的化学式为
(5)请任意举出一例证明元素③的最高价氧化物对应的水化物的溶液具有强氧化性
(6)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可观察到大量的白烟,写出产生该现象的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】已知元素X、Y均为短周期元素,X元素的一种核素常用于测文物的年代,Y元素原子半径是所有原子中最小的,元素X、Y可形成两种常见化合物M和N,已知M可以使高锰酸钾酸性溶液褪色,M分子中所含X元素的质量是Y元素质量的6倍,且M的相对分子质量为56。N是一种常用溶剂,它的实验式XY。回答下列问题:
(1)符合条件的M的有______ 种。
(2)任意写一种不带支链的M的结构简式__________ 。
(3)若在N与液溴的混合液中加入铁粉可以发生反应(在如图装置a容器中反应),则:
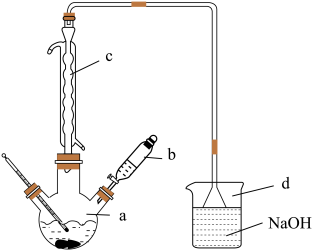
①写出a容器中发生的所有反应的化学方程式:_____________ 。
②d容器中NaOH溶液的作用是_____________ 。
(4)在碘水中加入N振荡静置后的现象是__________ 。
(5)等质量M、N完全燃烧时消耗O2的物质的量较多的是________ (填“M”或“N”)。
(1)符合条件的M的有
(2)任意写一种不带支链的M的结构简式
(3)若在N与液溴的混合液中加入铁粉可以发生反应(在如图装置a容器中反应),则:

①写出a容器中发生的所有反应的化学方程式:
②d容器中NaOH溶液的作用是
(4)在碘水中加入N振荡静置后的现象是
(5)等质量M、N完全燃烧时消耗O2的物质的量较多的是
您最近一年使用:0次



