A、B、C、D四种元素都是短周期元素。A元素的离子具有黄色的焰色反应。B离子带有2个单位正电荷,且B元素的离子结构和Ne具有相同的电子层排布。H2在C单质中燃烧产生苍白色火焰,D元素原子的电子层结构里,最外层电子数是次外层电子数的3倍。根据上述条件回答:
(1)元素C位于第___ 周期第___ 族。
(2)A是___ 元素,B是___ 元素,D是___ 元素。
(3)A与D形成稳定的化合物的化学式为___ ,此化合物与水反应的化学方程式为___ 。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为___ 。
(1)元素C位于第
(2)A是
(3)A与D形成稳定的化合物的化学式为
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为
更新时间:2020-03-09 19:57:42
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如图反应(图中有些反应的产物和反应条件没有标出)。
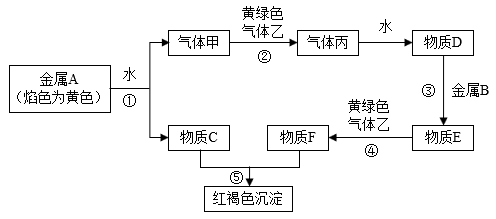
请回答下列问题:
(1)A的化学式为_____ ,F的化学式为____ 。
(2)写出物质C的溶液与黄绿色气体乙反应的离子反应方程式:_____ 。

请回答下列问题:
(1)A的化学式为
(2)写出物质C的溶液与黄绿色气体乙反应的离子反应方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】二氧化氯(ClO2)是一种高效气体消毒剂,易溶于水,沸点为11.0℃,ClO2气体浓度过高极易爆炸分解,制备过程中要严格控制其浓度。用干燥的氯气与固体亚氯酸钠制备纯净的二氧化氯,反应原理:2NaClO2+ Cl2= 2ClO2+2NaCl,反应装置如图所示:
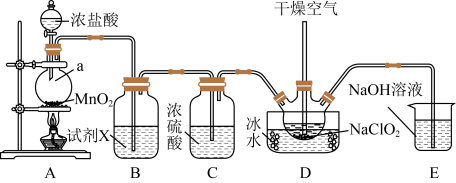
(1)仪器a的名称为:_______ 。
(2)A中发生的离子反应方程式为:_______ 。
(3)试剂X的作用是:_______ 。
(4)装置D中通入干燥空气的作用是:_______ 。
(5)写出处该实验装置存在的缺陷:_______ 。

(1)仪器a的名称为:
(2)A中发生的离子反应方程式为:
(3)试剂X的作用是:
(4)装置D中通入干燥空气的作用是:
(5)写出处该实验装置存在的缺陷:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氯酸钾( )可用于烟花、医药、火箭推进剂等。实验室中用下图装置制取氯气,并用氯气与
)可用于烟花、医药、火箭推进剂等。实验室中用下图装置制取氯气,并用氯气与 溶液反应制取氯酸钾(部分仪器已省略)。
溶液反应制取氯酸钾(部分仪器已省略)。

(1)仪器b的名称是___________ ,b中发生反应的化学方程式是___________ 。
(2)仪器c中盛放的液体是___________ ,其作用是___________ 。
(3)氯气与 溶液反应时,采用水浴加热的优点是
溶液反应时,采用水浴加热的优点是___________ (答一条)。
(4)仪器d中盛放的液体是___________ ,其作用是___________ 。
 )可用于烟花、医药、火箭推进剂等。实验室中用下图装置制取氯气,并用氯气与
)可用于烟花、医药、火箭推进剂等。实验室中用下图装置制取氯气,并用氯气与 溶液反应制取氯酸钾(部分仪器已省略)。
溶液反应制取氯酸钾(部分仪器已省略)。
(1)仪器b的名称是
(2)仪器c中盛放的液体是
(3)氯气与
 溶液反应时,采用水浴加热的优点是
溶液反应时,采用水浴加热的优点是(4)仪器d中盛放的液体是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】测定含Na2O杂质的Na2O2试样的质量分数有多种方法。
方法一:质量法。实验流程如图:

(1)操作Ⅰ的名称为___ ,所需实验仪器有(固定、夹持仪器除外)酒精灯、___ 。
(2)流程结束时称量固体质量为23.4g,则试样中Na2O2的质量百分数为___ %。
(3)在溶液转移步骤,若有少量液体溅出来,Na2O2质量分数的测定结果___ (填“偏低”、“偏高”、“不影响”)。
方法二:气体体积法
已知:气体体积可通过一定的计算公式换算成质量。
请设计一个最简单 的实验来测定试样中Na2O2的质量分数(试样质量依然是14.0g)。可供选择的药品和装置如图:
①CaCO3固体、浓盐酸、水。
②
(4)该实验的目的是通过测___ (填气体的分子式)的体积来换算成质量,再求Na2O2的质量。产生该气体的化学方程式是___ 。
(5)所选装置的接口顺序为(连接用的乳胶管忽略)___ 。
方法一:质量法。实验流程如图:

(1)操作Ⅰ的名称为
(2)流程结束时称量固体质量为23.4g,则试样中Na2O2的质量百分数为
(3)在溶液转移步骤,若有少量液体溅出来,Na2O2质量分数的测定结果
方法二:气体体积法
已知:气体体积可通过一定的计算公式换算成质量。
请设计一个
①CaCO3固体、浓盐酸、水。
②

(4)该实验的目的是通过测
(5)所选装置的接口顺序为(连接用的乳胶管忽略)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下图中,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请据图回答下列问题:

(1)A、G的化学式分别为___________ 、___________ 。
(2)写出反应②的化学方程式:___________ 。
(3)A与石灰乳反应制得的漂白粉的有效成分是___________ (填化学式),该物质在空气中失效的原因是___________ (用化学方程式表示)。
(4)标准状况下,把8.96LCO2通入一定量的过氧化钠固体中,充分反应后收集到6.72L气体,则这6.72L气体的质量是___________ g。

(1)A、G的化学式分别为
(2)写出反应②的化学方程式:
(3)A与石灰乳反应制得的漂白粉的有效成分是
(4)标准状况下,把8.96LCO2通入一定量的过氧化钠固体中,充分反应后收集到6.72L气体,则这6.72L气体的质量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某校科学兴趣小组探究二氧化碳与过氧化钠反应是否有氧气生成,设计了下图的实验装置。B中盛有饱和碳酸氢钠溶液,目的是除去二氧化碳中混有的氯化氢气体,E为收集氧气装置。
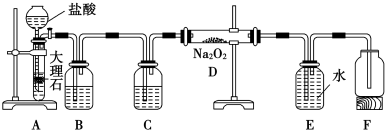
(1)写出装置A中发生反应的离子方程式_______ 。
(2)C中盛有_______ ,目的是_______ 。
(3)写出装置D中发生反应的化学方程式_______ 。
(4)指出装置E的错误_______ 。
(5)写出过氧化钠与水反应的化学方程式_______ 。

(1)写出装置A中发生反应的离子方程式
(2)C中盛有
(3)写出装置D中发生反应的化学方程式
(4)指出装置E的错误
(5)写出过氧化钠与水反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知X、Y、Z、M、G、Q是六种短周期主族元素,分别在三个周期且原子序数依次增大。X、Z、Q的单质在常温下呈气态;Y的原子最外层电子数是其电子层数的2倍;X与M同主族;Z、G分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)Z在元素周期表中的位置为
(2)Z和Q的最低价氢化物沸点更高的是(写化学式)
(3)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)
(4)M2Z2的电子式为
(5)常温下,能与G的单质发生反应的是(填字母序号)
A.CuSO4溶液 B.浓硫酸 C.NaOH溶液 D.Na2CO3固体
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C为短周期元素,在周期表中所处位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。

(1)写出元素名称:A_________ 、B_________ 、C_________ 。
(2)B位于元素周期表第_________ 周期第_________ 族。
(3)比较B、C的原子半径:B___________ C。写出A的气态氢化物与B的最高价氧化物对应的水化物反应的化学方程式________________________ 。

(1)写出元素名称:A
(2)B位于元素周期表第
(3)比较B、C的原子半径:B
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有 A、B、C、D、E 五种短周期主族元素,原子序数由 A 到 E 逐渐增大.①A 元素最外层电子数是次外层电子数的 2 倍. ②B 的阴离子和 C 的阳离子与氖原子的电子层结构相同.③在通常状况下,B 的单质是气体,0.1molB 的气体与足量的氢气完全反应共有 0.4mol 电子转移.④C 的单质在点燃时与 B 的单质充分反应,生成淡黄色的固体, 此淡黄色固体能与 AB2 反应可生成 B 的单质.⑤D 的气态氢化物与其最高价含氧酸间能发生氧化还原反应.请写出:
(1)A 元素的最高价氧化物的电子式_________________ ,A 元素简单气态氢化物可构成碱性燃料电池,该电池的的负极电极方程式为:_____________________
(2)B 元素在周期表中的位置_____________________
(3)B 单质与 C 单质在点燃时反应的生成物中所含化学键类型有_________________
(4)D 元素的低价氧化物与 E 的单质的水溶液反应的化学方程式为 :____________________
(5)C 与 D 能形成 2:1 的化合物,用电子式表示该化合物的形成过程:_________________________
(1)A 元素的最高价氧化物的电子式
(2)B 元素在周期表中的位置
(3)B 单质与 C 单质在点燃时反应的生成物中所含化学键类型有
(4)D 元素的低价氧化物与 E 的单质的水溶液反应的化学方程式为 :
(5)C 与 D 能形成 2:1 的化合物,用电子式表示该化合物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。
请回答下列问题:
(1)元素D在周期表中的位置___ 。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)___ 。
(3)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有___ 。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:______________ 。
若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:______________ 。
(5)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的离子方程式______________ 。
请回答下列问题:
(1)元素D在周期表中的位置
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)
(3)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:
若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:
(5)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和。
(1)B为__________ (填写元素符号),D的最高价氧化物对应的水化物是_________ (填写化学式),离子半径大小B_________ C(填“>”“<”或“=”);
(2)写出A、B的化合物与E反应的化学方程式:______________________ ;A、B两元素形成的化合物属于_________ (填“离子”或“共价”)化合物。
(3)A的单质与D的最高价氧化物对应的水化物反应的化学方程式为_______________ 。
Ⅱ.常温下由三种短周期元素形成的气体单质X、Y、Z,有下列转化关系(反应条件已略去):

已知:X分子中含共价键最多;甲分子中含10个电子,乙分子含有18个电子。
(4)化合物甲的电子式是_____________ ;化合物丙中存在的化学键为___________ 、_________
(1)B为
(2)写出A、B的化合物与E反应的化学方程式:
(3)A的单质与D的最高价氧化物对应的水化物反应的化学方程式为
Ⅱ.常温下由三种短周期元素形成的气体单质X、Y、Z,有下列转化关系(反应条件已略去):

已知:X分子中含共价键最多;甲分子中含10个电子,乙分子含有18个电子。
(4)化合物甲的电子式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E、F、G是短周期元素,周期表中A与B相邻、B与C相邻;C与E同主族;A与C最外层电子数之比为2:3,B的最外层电子数比C的最外层电子数少1个;F元素的原子在周期表中半径最小;常见化合物D2C2与水反应生成C的单质(气体),且滴入酚酞后溶液变红。G是第三周期原子半径最小的主族元素。
(1)A在元素周期表中的位置为___ ;F和C形成的18电子分子的化学式为___ 。
(2)用一个化学方程式证明E、G的非金属性强弱___ 。
(3)C、D、E、G简单离子半径由大到小的顺序为___ (用离子符号表示)。
(4)将G的单质溶于水中,所得溶液中具有氧化性的含G粒子有___ (用化学符号表示)。
(5)B有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成B的含氧酸盐只有一种,则该含氧酸盐的化学式是__ 。
(1)A在元素周期表中的位置为
(2)用一个化学方程式证明E、G的非金属性强弱
(3)C、D、E、G简单离子半径由大到小的顺序为
(4)将G的单质溶于水中,所得溶液中具有氧化性的含G粒子有
(5)B有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成B的含氧酸盐只有一种,则该含氧酸盐的化学式是
您最近一年使用:0次



