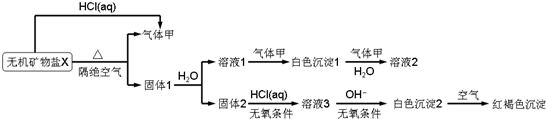
某研究小组为了探究一种无机矿物盐X(仅含四种元素)的组成和性质,设计并完成了如图所示实验:
另取 在惰性气流中加热至完全分解,得到
在惰性气流中加热至完全分解,得到 固体1。请回答如下问题:
固体1。请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图____ ,写出气体甲的化学式______ 。
(2)X的化学式是______ ,在惰性气流中加热X至完全分解的化学反应方程式为_________ 。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是___________ (用化学反应方程式表示)。
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式_______ ,并设计实验方案验证该反应的产物_____ 。

另取
 在惰性气流中加热至完全分解,得到
在惰性气流中加热至完全分解,得到 固体1。请回答如下问题:
固体1。请回答如下问题:(1)画出白色沉淀1中金属元素的原子结构示意图
(2)X的化学式是
(3)白色沉淀2在空气中变成红褐色沉淀的原因是
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式
更新时间:2020-10-02 16:46:46
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】已知X为 和CuO的混合物,且知氧化性顺序:
和CuO的混合物,且知氧化性顺序: 。取等质量的两份X样品进行如图所示的实验:
。取等质量的两份X样品进行如图所示的实验:
(1)若溶液D中只有一种金属离子,则一定是___________ ;若C固体是纯净物,该固体是___________ 。
(2)印刷电路板是由高分子材料和铜箔复合而成,可用A溶液作“腐蚀剂"刻制印刷电路的离子反应方程式为___________ 。
(3)若溶液D中只有一种金属离子,步骤③所得固体C是纯净物,质量为12.8g,无色气体E在标准状况下的体积为2.24L。则每份X样品中 的质量为
的质量为___________ 。
 和CuO的混合物,且知氧化性顺序:
和CuO的混合物,且知氧化性顺序: 。取等质量的两份X样品进行如图所示的实验:
。取等质量的两份X样品进行如图所示的实验:
(1)若溶液D中只有一种金属离子,则一定是
(2)印刷电路板是由高分子材料和铜箔复合而成,可用A溶液作“腐蚀剂"刻制印刷电路的离子反应方程式为
(3)若溶液D中只有一种金属离子,步骤③所得固体C是纯净物,质量为12.8g,无色气体E在标准状况下的体积为2.24L。则每份X样品中
 的质量为
的质量为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】A~H 是中学化学中常见的物质,转化关系如下图所示(部分反应物、反应条件和产物已略去)。A、H 是常见的金属单质,工业上常用电解法冶炼H;通常状况下B 为黄绿色气体;G 为红棕色固体;C、D、E、F、G 物种化合物含有同一种元素。

(1) B 的电子式为____________ 。
(2) 检验D中金属阳离子的实验方案是____________ 。
(3) 金属H 既能与强酸反应又能与强碱反应,其与NaOH 溶液反应的离子方程式为____________ 。
(4) E 在空气中转化成F 的化学方程式为____________ 。
(5) 理论上G 与H 反应生成1mol 固体A 放出428kJ 热量,G 与H 反应的热化学方程式为____________ 。
(6) 单质A 在氧气中的燃烧产物X 可用于去除地下水中的 具有放射性)。在酸性条件下,X 将TcO4-−转化为难溶于水的TcO2,同时得到F,该反应的离子方程式为
具有放射性)。在酸性条件下,X 将TcO4-−转化为难溶于水的TcO2,同时得到F,该反应的离子方程式为____________ 。

(1) B 的电子式为
(2) 检验D中金属阳离子的实验方案是
(3) 金属H 既能与强酸反应又能与强碱反应,其与NaOH 溶液反应的离子方程式为
(4) E 在空气中转化成F 的化学方程式为
(5) 理论上G 与H 反应生成1mol 固体A 放出428kJ 热量,G 与H 反应的热化学方程式为
(6) 单质A 在氧气中的燃烧产物X 可用于去除地下水中的
 具有放射性)。在酸性条件下,X 将TcO4-−转化为难溶于水的TcO2,同时得到F,该反应的离子方程式为
具有放射性)。在酸性条件下,X 将TcO4-−转化为难溶于水的TcO2,同时得到F,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】由三种元素组成的难溶化合物A是一种新型超薄二维纳米材料,可用作锂电池的正极材料。可按如图流程探究A的组成(已知A与稀盐酸恰好完全反应,且溶液B与KSCN溶液作用显血红色)。
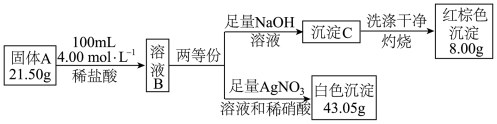
(1)A中非金属元素是___________ ,A的化学式是 ___________ 。
(2)固体A与稀盐酸反应的离子方程式是___________ 。
(3)上述流程探究中有过滤操作,该操作时需要用到的玻璃仪器有___________ 。
(4)Li、化合物A、有机溶剂(可传导Li+)组成电池,放电时正极生成金属单质和两种含锂的化合物,放电时正极的电极反应式为___________ 。

(1)A中非金属元素是
(2)固体A与稀盐酸反应的离子方程式是
(3)上述流程探究中有过滤操作,该操作时需要用到的玻璃仪器有
(4)Li、化合物A、有机溶剂(可传导Li+)组成电池,放电时正极生成金属单质和两种含锂的化合物,放电时正极的电极反应式为
您最近一年使用:0次
【推荐2】北京时间2021年10月16日上午,神舟十三号航天员顺利进驻“天和”核心舱,开启为期6个月的航天飞行任务。航天员生活、工作于其中的“天和”核心舱是利用三结砷化镓太阳能电池作为其动力。一种由砷化家废料(主要成分为GaAs,含Fe2O3、SiO2等杂质)制备镓的工艺流程如图:
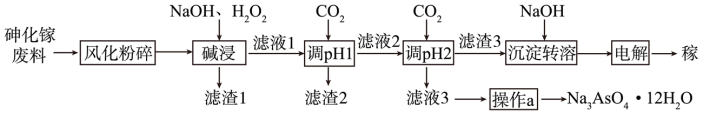
已知:①Ga在周期表中位于Al的正下方,性质与Al相似;
②离子完全沉淀的pH值: 为8,
为8,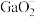 为5.5。
为5.5。
回答下列问题:
(1)“风化粉碎”的目的是_______ 。
(2)“碱浸”温度控制在70℃左右,温度不能过高或过低的原因是_______ 。
(3)“碱浸”时,GaAs中Ga以 的形式进入溶液中,该反应的离子方程式是
的形式进入溶液中,该反应的离子方程式是_______ 。
(4)“滤渣1”的成分为_______ (填化学式),“操作a”为_______ 、过滤、洗涤、干燥。
(5)“调pH1”时,不能通入过量的 ,其原因是
,其原因是_______ 。
(6)若用240kg含7.25%砷化镓的废料回收家,得到纯度为96%的镓7.0kg,则家的回收率为_______ %(保留3位有效数字)。

已知:①Ga在周期表中位于Al的正下方,性质与Al相似;
②离子完全沉淀的pH值:
 为8,
为8,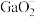 为5.5。
为5.5。回答下列问题:
(1)“风化粉碎”的目的是
(2)“碱浸”温度控制在70℃左右,温度不能过高或过低的原因是
(3)“碱浸”时,GaAs中Ga以
 的形式进入溶液中,该反应的离子方程式是
的形式进入溶液中,该反应的离子方程式是(4)“滤渣1”的成分为
(5)“调pH1”时,不能通入过量的
 ,其原因是
,其原因是(6)若用240kg含7.25%砷化镓的废料回收家,得到纯度为96%的镓7.0kg,则家的回收率为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】 可用于油漆颜料及羊毛处理。工业上以高铁铬铁矿(主要成分为
可用于油漆颜料及羊毛处理。工业上以高铁铬铁矿(主要成分为 ,含
,含 、
、 、
、 等杂质)为原料生产
等杂质)为原料生产 和金属
和金属 的工艺流程如图。
的工艺流程如图。
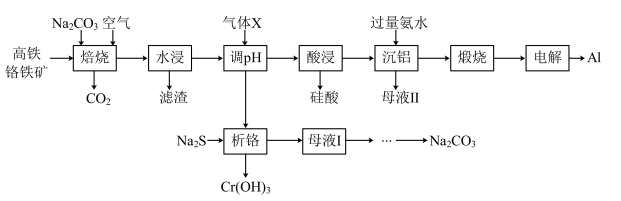
回答下列问题:
(1)基态 原子的价电子排布式为
原子的价电子排布式为___________ 。
(2)为提高焙烧效率,可以采取的措施为___________ (填一种方法即可);已知“焙烧”时, 转化为
转化为 ,请写出该转化过程的化学方程式
,请写出该转化过程的化学方程式___________ 。
(3)“水浸”后滤渣主要成分为___________ (填化学式,下同)。
(4)“调 ”时通入的“气体
”时通入的“气体 ”是
”是___________ 。
(5)用稀硫酸进行“酸浸”后,再进行“沉铝”操作,所得的母液II的主要成分为___________ 。
(6)过滤得到母液I经___________ 、___________ 、过滤、洗涤、干燥得到碳酸钠晶体失去结晶水得到碳酸钠固体。
(7)加入 “析铬”,
“析铬”, 被还原的离子方程式为
被还原的离子方程式为___________ 。
 可用于油漆颜料及羊毛处理。工业上以高铁铬铁矿(主要成分为
可用于油漆颜料及羊毛处理。工业上以高铁铬铁矿(主要成分为 ,含
,含 、
、 、
、 等杂质)为原料生产
等杂质)为原料生产 和金属
和金属 的工艺流程如图。
的工艺流程如图。
回答下列问题:
(1)基态
 原子的价电子排布式为
原子的价电子排布式为(2)为提高焙烧效率,可以采取的措施为
 转化为
转化为 ,请写出该转化过程的化学方程式
,请写出该转化过程的化学方程式(3)“水浸”后滤渣主要成分为
(4)“调
 ”时通入的“气体
”时通入的“气体 ”是
”是(5)用稀硫酸进行“酸浸”后,再进行“沉铝”操作,所得的母液II的主要成分为
(6)过滤得到母液I经
(7)加入
 “析铬”,
“析铬”, 被还原的离子方程式为
被还原的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】研究发现百多种植物富含草酸,尤以菠菜、苋菜、甜菜、马齿苋、芋头、甘薯和大黄等植物中含量最高,由于草酸可降低矿质元素的生物利用率,在人体中容易与钙离子形成草酸钙导致肾结石,草酸往往被认为是一种矿质元素吸收利用的拮抗物。
已知:草酸( )是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。
)是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。
(1)草酸的制备:在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置如图所示。
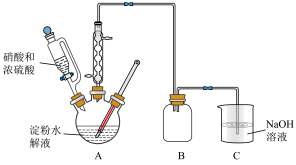
①55~60℃时,装置A中生成 ,同时生成NO。写出该反应的化学方程式:
,同时生成NO。写出该反应的化学方程式:___________ 。
②该实验中催化剂浓硫酸用量不宜过量的原因是___________ 。(答出一点即可)
③装置C的作用是___________ 。
(2)下列事实不能证明草酸是弱电解质的是___________(填字母)。
(3)向10mL
 溶液中加入
溶液中加入 NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
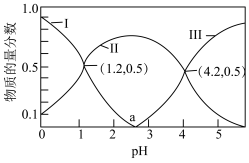
①写出草酸的一级电离方程式:___________ 。
②25℃时,碳酸电离平衡常数分别是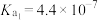 ,
, ,写出少量草酸和过量碳酸钠反应的离子方程式:
,写出少量草酸和过量碳酸钠反应的离子方程式:___________ 。
已知:草酸(
 )是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。
)是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。(1)草酸的制备:在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置如图所示。

①55~60℃时,装置A中生成
 ,同时生成NO。写出该反应的化学方程式:
,同时生成NO。写出该反应的化学方程式:②该实验中催化剂浓硫酸用量不宜过量的原因是
③装置C的作用是
(2)下列事实不能证明草酸是弱电解质的是___________(填字母)。
A.草酸能使酸性 溶液褪色 溶液褪色 |
B.常温下,0.1mol/L的 溶液的pH=2 溶液的pH=2 |
C.相同条件下,浓度均为0.1mol/L的 溶液的导电能力比硫酸的导电能力弱 溶液的导电能力比硫酸的导电能力弱 |
D. 溶液中存在 溶液中存在 分子,呈酸性 分子,呈酸性 |

 溶液中加入
溶液中加入 NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
①写出草酸的一级电离方程式:
②25℃时,碳酸电离平衡常数分别是
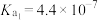 ,
, ,写出少量草酸和过量碳酸钠反应的离子方程式:
,写出少量草酸和过量碳酸钠反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】A、B、C、D四种元素的核电荷数均小于18,A元素原子核外只有1个电子;B是地壳中含量最多的元素;B、C可形成两种化合物CB和CB2,C的最高正价与最低负价绝对值相等,CB有毒,CB2可用于灭火;D+具有与Ne原子相同的电子层结构。
(1)试判断A、B、C、D四种元素的名称。A__________ ,B__________ ,C__________ ,D__________ 。
(2)由B、D两种元素组成的D2B2型化合物的电子式为______________ ,CB2的电子式为_______________ 。
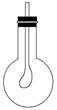
(3)如右图所示,在烧瓶中收集满CB2气体,用带导管(导管一端事先绑好一个气球)的胶塞塞紧,当打开胶塞迅速倒入浓的A、B、D三种元素组成的化合物的溶液后,立即塞紧胶塞振荡,可观察到_____________ ,原因是_________________ 。
(1)试判断A、B、C、D四种元素的名称。A
(2)由B、D两种元素组成的D2B2型化合物的电子式为
(3)如右图所示,在烧瓶中收集满CB2气体,用带导管(导管一端事先绑好一个气球)的胶塞塞紧,当打开胶塞迅速倒入浓的A、B、D三种元素组成的化合物的溶液后,立即塞紧胶塞振荡,可观察到

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】碳酸钴常用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验。
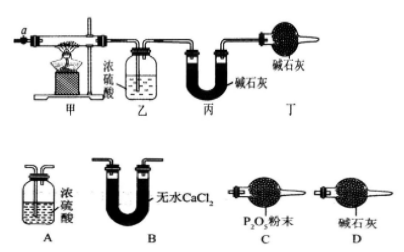
(1)请完成下列实验步骤:
①称取 3. 65 g 样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中_______ (填实验现象),停止加热;
④打开活塞 a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是___________________________________ 。
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的_______ (填字母)连接在_______ (填装置连接位置)。
(4)若按正确装置进行实验,测得如下数据。
则该碱式碳酸钴的化学式为______________ 。

(1)请完成下列实验步骤:
①称取 3. 65 g 样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中
④打开活塞 a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的
(4)若按正确装置进行实验,测得如下数据。
| 乙装置的质量/g | 丙装置的质量/g | |
| 加热前 | 80.00 | 62.00 |
| 加热后 | 80.36 | 62.88 |
您最近一年使用:0次




