请回答下列问题:
(1)在一定条件下氨气可用来将氮氧化物转化为无污染的物质。试写出氨气和二氧化氮在一定条件下反应的化学方程式:_______ ,反应中氧化剂是_______ ,还原剂是_____ 。
(2)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下: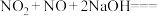
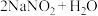 、
、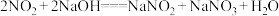 。现有
。现有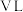 某NaOH溶液,能完全吸收由
某NaOH溶液,能完全吸收由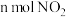 和
和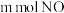 组成的大气污染物。
组成的大气污染物。
①所用烧碱溶液的物质的量浓度至少为______  。
。
②若所得溶液中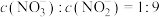 ,则原混合气体中
,则原混合气体中 和NO的物质的量之比
和NO的物质的量之比
_______ 。
(1)在一定条件下氨气可用来将氮氧化物转化为无污染的物质。试写出氨气和二氧化氮在一定条件下反应的化学方程式:
(2)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
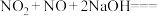
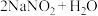 、
、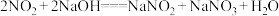 。现有
。现有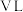 某NaOH溶液,能完全吸收由
某NaOH溶液,能完全吸收由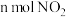 和
和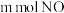 组成的大气污染物。
组成的大气污染物。①所用烧碱溶液的物质的量浓度至少为
 。
。②若所得溶液中
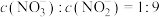 ,则原混合气体中
,则原混合气体中 和NO的物质的量之比
和NO的物质的量之比
19-20高一·全国·单元测试 查看更多[1]
更新时间:2020-10-03 19:11:01
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】硫代硫酸钠(Na2S2O3)俗称海波、大苏打,无色透明晶体,易溶于水,遇强酸反应产生硫单质和二氧化硫气体;具有强还原性,与强氧化剂反应产物为SO42-;
(1)Na2S2O3中S元素的化合价为_________ 。
(2)向Na2S2O3溶液中滴加稀硫酸,其反应的离子方程式为____________________________ 。
(3)Na2S2O3溶液与Cl2反应,可作为绵织物漂白后的脱氧剂。该反应的离子方程式为_______ ,要脱去22.4 L Cl2(标准状况下),需要Na2S2O3________ mol。
(4)工业上常用硫化碱法制备海波。其原理是向碳酸钠和硫化钠物质的量之比为1:2的混合液中通入过量的二氧化硫,经蒸发、结晶,即得硫代硫酸钠。其反应的化学方程式为_____ ,其氧化剂为_____________ 。
(1)Na2S2O3中S元素的化合价为
(2)向Na2S2O3溶液中滴加稀硫酸,其反应的离子方程式为
(3)Na2S2O3溶液与Cl2反应,可作为绵织物漂白后的脱氧剂。该反应的离子方程式为
(4)工业上常用硫化碱法制备海波。其原理是向碳酸钠和硫化钠物质的量之比为1:2的混合液中通入过量的二氧化硫,经蒸发、结晶,即得硫代硫酸钠。其反应的化学方程式为
您最近一年使用:0次
【推荐2】①已知白磷和氯酸溶液可发生如下反应,将该反应进行配平:
______ P4+_______ HClO3+_______ ______ =______ HCl+____ H3PO4
②白磷有毒,有实验室可采用CuSO4溶液进行处理,其反应为:11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4
在该反应中30 mol CuSO4可氧化P4的物质的量是______ mol.
②白磷有毒,有实验室可采用CuSO4溶液进行处理,其反应为:11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4
在该反应中30 mol CuSO4可氧化P4的物质的量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】钾是活泼的碱金属,钾和氧有氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物。
⑴钾和硝酸钾反应可制得氧化钾:K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有___________ g
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。写出超氧化钾与二氧化碳反应的化学方程式______________________ ,为了维持气压稳定,可以使用超氧化钾和过氧化钾的混合物使吸收的CO2与生成的O2体积相同(同温同压),则它们的物质的量之比为n(KO2) :n(K2O2)=____________
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比_______ 。如果产物A只含有两种化合物,写出所有可能的化学式并计算A中两种化合物的物质的量之比_______ 。
⑴钾和硝酸钾反应可制得氧化钾:K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。写出超氧化钾与二氧化碳反应的化学方程式
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在标准状况下,用以下气体做喷泉实验,请根据情况,填写烧瓶中溶液的物质的量浓度(假设烧瓶中溶质不能扩散出来)。
(1)用HCl气体做喷泉实验,喷泉结束后,水充满烧瓶,则溶液的物质的量浓度为_______ ;
(2)用NH3做喷泉实验时,喷泉结束后,水充满烧瓶,则溶液的物质的量浓度为____________ ;
(3)用NO2做喷泉实验时,喷泉结束后,水充至烧瓶的 处,则溶液的物质的量浓度为
处,则溶液的物质的量浓度为____________ ;
(4)用NO2和O2按4∶1体积比混合,喷泉结束后,水充满烧瓶,则溶液的物质的量浓度为________ 。
(1)用HCl气体做喷泉实验,喷泉结束后,水充满烧瓶,则溶液的物质的量浓度为
(2)用NH3做喷泉实验时,喷泉结束后,水充满烧瓶,则溶液的物质的量浓度为
(3)用NO2做喷泉实验时,喷泉结束后,水充至烧瓶的
 处,则溶液的物质的量浓度为
处,则溶液的物质的量浓度为(4)用NO2和O2按4∶1体积比混合,喷泉结束后,水充满烧瓶,则溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】烟气中NOx是NO和NO2的混合物(不含N2O4);
(1)根据废气排放标准,1m3烟气最高允许含400mgNOx.若NOx中NO质量分数为0.85,则lm3烟气中最高允许含NO___________ L(标准状况,保留2位小数);
(2)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度l.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为_______ mol/L(保留2位小数);
(3)已知:
NO+NO2+Na2CO3→2NaNO2+CO2 ①
2NO2+Na2CO3→NaNO2+NaNO3+CO2 ②
1m3含2000mgNOx的烟气用质量分数为0.150的碳酸钠溶液吸收.若吸收率为80%,吸收后的烟气______ 排放标准(填“符合”或“不符合”),理由:___________ ;
(4)加入硝酸可改变烟气中NO和NO2的比,反应为:NO+2HNO3→3NO2+H2O当烟气中n(NO):n(NO2)=2:3时,吸收率最高;
lm3烟气含2000mgNOx,其中n(NO):n(NO2)=9:1;
计算:
(i)为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数)__________ ;
(ii)1m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量_____________ (假设上述吸收反应中,反应①比反应②迅速.计算结果保留1位小数)。
(1)根据废气排放标准,1m3烟气最高允许含400mgNOx.若NOx中NO质量分数为0.85,则lm3烟气中最高允许含NO
(2)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度l.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为
(3)已知:
NO+NO2+Na2CO3→2NaNO2+CO2 ①
2NO2+Na2CO3→NaNO2+NaNO3+CO2 ②
1m3含2000mgNOx的烟气用质量分数为0.150的碳酸钠溶液吸收.若吸收率为80%,吸收后的烟气
(4)加入硝酸可改变烟气中NO和NO2的比,反应为:NO+2HNO3→3NO2+H2O当烟气中n(NO):n(NO2)=2:3时,吸收率最高;
lm3烟气含2000mgNOx,其中n(NO):n(NO2)=9:1;
计算:
(i)为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数)
(ii)1m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上用氨催化氧化法可生产硝酸,其生产过程可表示为:4NH3+5O2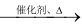 4NO+6H2O --① 4NO+3O2+2H2O→4HNO3---②
4NO+6H2O --① 4NO+3O2+2H2O→4HNO3---②
(1)如果以一定量的氨气在一密闭容器中与足量氧气发生上述反应,冷却后所得溶液中溶质的质量分数是_____ (保留2位小数,下同。)
(2)现以1.70吨液氨为原料生产硝酸,然后加入4.50吨水,得到密度为1.31 g/cm3的硝酸,该硝酸的物质的量浓度是__________ mol/L。( 假设生产过程中反应物和生成物均无损耗)。
(3)把22.40 g铁完全溶解于某浓度的硝酸中,反应只收集到0.30 mol NO2和0.20 mol NO。通过计算推断反应后溶液中溶质的成分及其物质的量______ 。(写出计算过程)
(4)硝酸工业尾气中的NO、NO2属于大气的主要污染物。已知1 m3硝酸工业的尾气中含3160 mg NOx,其中n(NO) :n(NO2)=9:1。
①如果用NaOH溶液完全吸收NOx,至少需要补充标准状况下的富氧空气多少升? (富氧空气中O2的体积分数为0.25) (写出计算过程)___ 。
②如果用氨催化还原法,即用氨作还原剂,将NO、NO2 转化为氮气直接排入空气中,需要氨气的质量为多少克? (写出计算过程)_______ 。
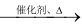 4NO+6H2O --① 4NO+3O2+2H2O→4HNO3---②
4NO+6H2O --① 4NO+3O2+2H2O→4HNO3---②(1)如果以一定量的氨气在一密闭容器中与足量氧气发生上述反应,冷却后所得溶液中溶质的质量分数是
(2)现以1.70吨液氨为原料生产硝酸,然后加入4.50吨水,得到密度为1.31 g/cm3的硝酸,该硝酸的物质的量浓度是
(3)把22.40 g铁完全溶解于某浓度的硝酸中,反应只收集到0.30 mol NO2和0.20 mol NO。通过计算推断反应后溶液中溶质的成分及其物质的量
(4)硝酸工业尾气中的NO、NO2属于大气的主要污染物。已知1 m3硝酸工业的尾气中含3160 mg NOx,其中n(NO) :n(NO2)=9:1。
①如果用NaOH溶液完全吸收NOx,至少需要补充标准状况下的富氧空气多少升? (富氧空气中O2的体积分数为0.25) (写出计算过程)
②如果用氨催化还原法,即用氨作还原剂,将NO、NO2 转化为氮气直接排入空气中,需要氨气的质量为多少克? (写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】已知:① NO + NO2 + 2NaOH 2NaNO2 + H2O;
2NaNO2 + H2O;
② 2NO2 + 2NaOH NaNO3 + NaNO2 + H2O
NaNO3 + NaNO2 + H2O
将51.2 g Cu溶于一定浓度的硝酸中,若生成的气体只含有NO、NO2,且这些气体恰好被500 mL2.0 mol/L的NaOH溶液完全吸收,得到只含NaNO2和NaNO3的溶液。求:气体中NO、NO2的物质的量分别为多少?
 2NaNO2 + H2O;
2NaNO2 + H2O;② 2NO2 + 2NaOH
 NaNO3 + NaNO2 + H2O
NaNO3 + NaNO2 + H2O 将51.2 g Cu溶于一定浓度的硝酸中,若生成的气体只含有NO、NO2,且这些气体恰好被500 mL2.0 mol/L的NaOH溶液完全吸收,得到只含NaNO2和NaNO3的溶液。求:气体中NO、NO2的物质的量分别为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】烟气中NOx是NO和NO2的混合物(不含N2O4);
(1)根据废气排放标准,1m3烟气最高允许含400mgNOx.若NOx中NO质量分数为0.85,则lm3烟气中最高允许含NO___________ L(标准状况,保留2位小数);
(2)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度l.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为_______ mol/L(保留2位小数);
(3)已知:
NO+NO2+Na2CO3→2NaNO2+CO2 ①
2NO2+Na2CO3→NaNO2+NaNO3+CO2 ②
1m3含2000mgNOx的烟气用质量分数为0.150的碳酸钠溶液吸收.若吸收率为80%,吸收后的烟气______ 排放标准(填“符合”或“不符合”),理由:___________ ;
(4)加入硝酸可改变烟气中NO和NO2的比,反应为:NO+2HNO3→3NO2+H2O当烟气中n(NO):n(NO2)=2:3时,吸收率最高;
lm3烟气含2000mgNOx,其中n(NO):n(NO2)=9:1;
计算:
(i)为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数)__________ ;
(ii)1m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量_____________ (假设上述吸收反应中,反应①比反应②迅速.计算结果保留1位小数)。
(1)根据废气排放标准,1m3烟气最高允许含400mgNOx.若NOx中NO质量分数为0.85,则lm3烟气中最高允许含NO
(2)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度l.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为
(3)已知:
NO+NO2+Na2CO3→2NaNO2+CO2 ①
2NO2+Na2CO3→NaNO2+NaNO3+CO2 ②
1m3含2000mgNOx的烟气用质量分数为0.150的碳酸钠溶液吸收.若吸收率为80%,吸收后的烟气
(4)加入硝酸可改变烟气中NO和NO2的比,反应为:NO+2HNO3→3NO2+H2O当烟气中n(NO):n(NO2)=2:3时,吸收率最高;
lm3烟气含2000mgNOx,其中n(NO):n(NO2)=9:1;
计算:
(i)为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数)
(ii)1m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量
您最近一年使用:0次