“神七”登天标志着我国的航天事业进入了新的篇章。
(1)火箭升空需要高能的燃料,经常是用N2O4和N2H4作为燃料,工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等。已知:
N2(g) + 2O2(g) =2NO2(g) △H =+67.7kJ·mol-1
N2H4(g) + O2(g) =N2(g) + 2H2O(g) △H = -534.0 kJ·mol-1
NO2(g)⇌1/2N2O4(g) △H = -26.35 kJ·mol-1
试写出气态联氨在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:______ 。
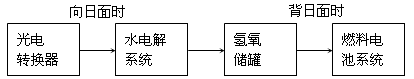
(2)下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,燃料电池放电时的负极反应为:______ 。如果某段时间内氢氧储罐中共收集到33.6L气体(已折算成标况),则该段时间内水电解系统中转移电子的物质的量为______ mol。
(3)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2.某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料。已知该反应的阳极反应为:4OH--4e- = O2↑+2H2O,则阴极反应为:______ 。
有人提出,可以设计反应2CO=2C+O2(△H>0)来消除CO的污染。请你判断上述反应是否能自发进行?______ ,理由是:______ 。
(1)火箭升空需要高能的燃料,经常是用N2O4和N2H4作为燃料,工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等。已知:
N2(g) + 2O2(g) =2NO2(g) △H =+67.7kJ·mol-1
N2H4(g) + O2(g) =N2(g) + 2H2O(g) △H = -534.0 kJ·mol-1
NO2(g)⇌1/2N2O4(g) △H = -26.35 kJ·mol-1
试写出气态联氨在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:
(2)下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,燃料电池放电时的负极反应为:

(3)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2.某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料。已知该反应的阳极反应为:4OH--4e- = O2↑+2H2O,则阴极反应为:
有人提出,可以设计反应2CO=2C+O2(△H>0)来消除CO的污染。请你判断上述反应是否能自发进行?
2012·宁夏银川·三模 查看更多[1]
(已下线)2012届宁夏银川一中高三第三次模拟考试化学试卷
更新时间:2016-12-09 03:14:25
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】环氧乙烷是重要的杀菌剂和工业合成原料。
Ⅰ.乙烯氧化法制环氧乙烷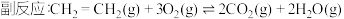

(1)主反应的各基元反应活化能如下:
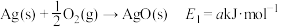 慢
慢
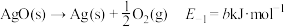 慢
慢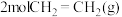 和
和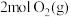 ,达到平衡时
,达到平衡时 的转化率为
的转化率为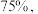
 的选择性为
的选择性为 ,则平衡时用各组分的物质的量分数表示主反应的化学平衡常数
,则平衡时用各组分的物质的量分数表示主反应的化学平衡常数
______ (保留2位有效数字)。已知:环氧乙烷选择性
Ⅱ.电化学合成环氧乙烷
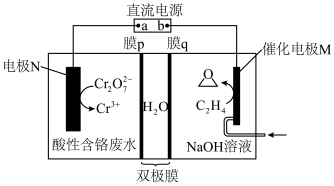
某电化学合成环氧乙烷同时处理酸性含铬废水的原理如图。______ 离子交换膜(填“阴”或“阳”),电极M反应为______ 。
(4)酸性废水质量每增大 ,制得环氧乙烷
,制得环氧乙烷______ g。
Ⅲ.环氧乙烷制乙二醇
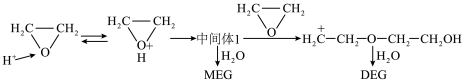
水与环氧乙烷分别在酸性和碱性介质中制乙二醇(MEG)的反应机理如下图,同时生成副产物(DEG)。
酸性条件: 的作用是
的作用是______ ,中间体1结构简式______ ,DEG结构简式______ 。
Ⅰ.乙烯氧化法制环氧乙烷


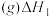
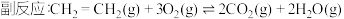

(1)主反应的各基元反应活化能如下:
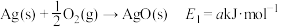 慢
慢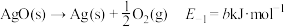 慢
慢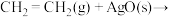

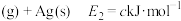 快
快

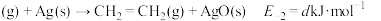 快
快

 (用含a,b,c,d的代数式表示),增大乙烯浓度
(用含a,b,c,d的代数式表示),增大乙烯浓度 的生成速率
的生成速率
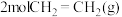 和
和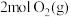 ,达到平衡时
,达到平衡时 的转化率为
的转化率为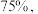
 的选择性为
的选择性为 ,则平衡时用各组分的物质的量分数表示主反应的化学平衡常数
,则平衡时用各组分的物质的量分数表示主反应的化学平衡常数

Ⅱ.电化学合成环氧乙烷
某电化学合成环氧乙烷同时处理酸性含铬废水的原理如图。
(4)酸性废水质量每增大
 ,制得环氧乙烷
,制得环氧乙烷Ⅲ.环氧乙烷制乙二醇
水与环氧乙烷分别在酸性和碱性介质中制乙二醇(MEG)的反应机理如下图,同时生成副产物(DEG)。
酸性条件:

 的作用是
的作用是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】乙醇是一种基本有机化工原料,可用作有机溶剂、制饮料酒以及食品工业。乙醇也可以制备氢气。回答下列问题:
(1)已知:
(a)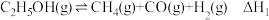
(b)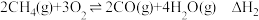
(c)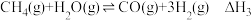
(d)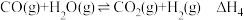
则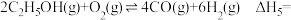
___________ (用代数式表示)。
(2)用平衡分压代替平衡浓度时,平衡常数可表示为 ,各反应的
,各反应的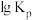 随温度的变化如图所示。
随温度的变化如图所示。

①反应a~d中,属于吸热反应的有___________ (填字母)。
②平衡常数大于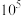 时可认为反应完全,则
时可认为反应完全,则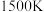 时,反应完全进行的有
时,反应完全进行的有___________ (填字母)。
(3)恒压条件下往反应容器中通入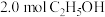 和少量
和少量 ,平衡时体系中各物质(
,平衡时体系中各物质( 、
、 、
、 、
、 、
、 )的物质的量分数随温度的变化如图所示。
)的物质的量分数随温度的变化如图所示。
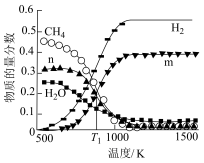
①图中表示 的曲线为
的曲线为___________ (填“m”或“n”)。
②下列说法正确的是___________ (填标号)。
A.当气体密度不再发生变化时,反应达到平衡状态
B.温度升高,反应c的 增大,
增大, 减小
减小
C.达到平衡时分离出部分 ,反应d的平衡常数增大
,反应d的平衡常数增大
D.加入稀有气体,重新达到平衡时 的物质的量增加
的物质的量增加
③ 下达到平衡时
下达到平衡时 和
和 均反应接近完全,
均反应接近完全, 、
、 和
和 的物质的量分数分别为0.20、0.32和0.12,则平衡时
的物质的量分数分别为0.20、0.32和0.12,则平衡时 的物质的量为
的物质的量为___________  ,反应d的平衡常数
,反应d的平衡常数
___________ 。
(1)已知:
(a)
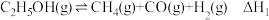
(b)
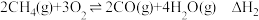
(c)
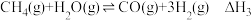
(d)
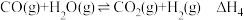
则
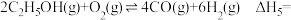
(2)用平衡分压代替平衡浓度时,平衡常数可表示为
 ,各反应的
,各反应的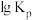 随温度的变化如图所示。
随温度的变化如图所示。
①反应a~d中,属于吸热反应的有
②平衡常数大于
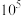 时可认为反应完全,则
时可认为反应完全,则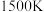 时,反应完全进行的有
时,反应完全进行的有(3)恒压条件下往反应容器中通入
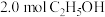 和少量
和少量 ,平衡时体系中各物质(
,平衡时体系中各物质( 、
、 、
、 、
、 、
、 )的物质的量分数随温度的变化如图所示。
)的物质的量分数随温度的变化如图所示。
①图中表示
 的曲线为
的曲线为②下列说法正确的是
A.当气体密度不再发生变化时,反应达到平衡状态
B.温度升高,反应c的
 增大,
增大, 减小
减小C.达到平衡时分离出部分
 ,反应d的平衡常数增大
,反应d的平衡常数增大D.加入稀有气体,重新达到平衡时
 的物质的量增加
的物质的量增加③
 下达到平衡时
下达到平衡时 和
和 均反应接近完全,
均反应接近完全, 、
、 和
和 的物质的量分数分别为0.20、0.32和0.12,则平衡时
的物质的量分数分别为0.20、0.32和0.12,则平衡时 的物质的量为
的物质的量为 ,反应d的平衡常数
,反应d的平衡常数
您最近一年使用:0次
【推荐3】C1(分子中含一个C的物质如CO、CO2、CH4、CH3OH等)分子的选择性催化转化可制备高附加值化学品(如合成气和清洁能源如氢气)。对解决当前日益严峻的能源短缺和气候变化等问题具有积极意义,已知在催化剂的表面可发生如下反应:
(1)甲醇分解:①CH3OH(g) CO(g)+2H2(g) △H1= +90.64 kJ•mol-1;
CO(g)+2H2(g) △H1= +90.64 kJ•mol-1;
水蒸气变换:②CO(g)+H2O(g) CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2
a.对于甲醇分解反应正反应活化能E1与逆反应活化能E2,其E1___ E2(填“>”或“<”)。
b.已知有关物质的摩尔生成熔(由元素最稳定的单质生成l mol纯化合物时的反应热)加如下:CO(g):-110.53 kJ/mol,CO2(g):-393.5 kJ/mol,H2O(g):-241.8 kJ/mol,H2(g):-0 kJ/mol;则△H2=___ 。
(2)573.2 K时,向一恒容密闭容器中按n(CH3OH):n(H2O)=1:1.2充入混合气体,已知CH3OH的起始压强为5.00 MPa,t h后达平衡时,CH3OH的转化率为60%,CO2的选择性为40%(选择性:转化的CH3OH中最终生成CO2和CO的百分比),则t h内v(CH3OH)=___ MPa﹒h-1(用含t的代数式表示),反应①的分压平衡常数Kp=___ (MPa)2。
(3)由于CO分子极难被活化,水煤气变换反应催化转化过程往往受热力学和反应动力学控制,通常工业上要求高温高压等苛刻反应条件,而低温等离子体催化能够在气相中快速活化CO分子,实现低温常压下高选择性地转化CO,下列关于水煤气变换反应的说法正确___ 。
A.催化剂能有效降低反应的活化能,但不能增大反应物中活化分子的百分数
B.相对于通常方法,工业上选择低温等离子体催化剂能有效提高反应速率和CO的平衡转化率
C.选择低温等离子体催化剂能有效的解决高能耗和催化剂易失活等关键问题
D.工业上通入的H2O(g)越多生成物的百分含量越高
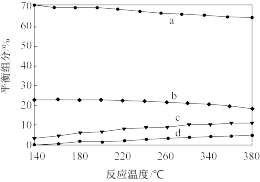
(4)在0.1 MPa下,将总进料量为1 mol且n(CH3OH):n(H2O)=1:1.2的混合气体充入一刚性密闭容器中进行反应。平衡时,测得CH3OH在给定温度范围内含量极小,H2、H2O(g)、CO、CO2四种组分的含量变化与反应温度的关系如图所示,曲线a、d对应物质的化学式分别为___ 、___ 。
(1)甲醇分解:①CH3OH(g)
 CO(g)+2H2(g) △H1= +90.64 kJ•mol-1;
CO(g)+2H2(g) △H1= +90.64 kJ•mol-1;水蒸气变换:②CO(g)+H2O(g)
 CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2a.对于甲醇分解反应正反应活化能E1与逆反应活化能E2,其E1
b.已知有关物质的摩尔生成熔(由元素最稳定的单质生成l mol纯化合物时的反应热)加如下:CO(g):-110.53 kJ/mol,CO2(g):-393.5 kJ/mol,H2O(g):-241.8 kJ/mol,H2(g):-0 kJ/mol;则△H2=
(2)573.2 K时,向一恒容密闭容器中按n(CH3OH):n(H2O)=1:1.2充入混合气体,已知CH3OH的起始压强为5.00 MPa,t h后达平衡时,CH3OH的转化率为60%,CO2的选择性为40%(选择性:转化的CH3OH中最终生成CO2和CO的百分比),则t h内v(CH3OH)=
(3)由于CO分子极难被活化,水煤气变换反应催化转化过程往往受热力学和反应动力学控制,通常工业上要求高温高压等苛刻反应条件,而低温等离子体催化能够在气相中快速活化CO分子,实现低温常压下高选择性地转化CO,下列关于水煤气变换反应的说法正确
A.催化剂能有效降低反应的活化能,但不能增大反应物中活化分子的百分数
B.相对于通常方法,工业上选择低温等离子体催化剂能有效提高反应速率和CO的平衡转化率
C.选择低温等离子体催化剂能有效的解决高能耗和催化剂易失活等关键问题
D.工业上通入的H2O(g)越多生成物的百分含量越高
(4)在0.1 MPa下,将总进料量为1 mol且n(CH3OH):n(H2O)=1:1.2的混合气体充入一刚性密闭容器中进行反应。平衡时,测得CH3OH在给定温度范围内含量极小,H2、H2O(g)、CO、CO2四种组分的含量变化与反应温度的关系如图所示,曲线a、d对应物质的化学式分别为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol ΔS=-200J·K-1·mol-1。
2NH3(g) ΔH=-92.4kJ/mol ΔS=-200J·K-1·mol-1。
回答下列问题:
(1)合成氨反应在常温下___________  填“能”或“不能”
填“能”或“不能” 自发。
自发。
(2)某小组进行工业合成氨N2(g)+3H2(g) 2NH3(g) ΔH<0的模拟研究,在1 L密闭容器中,分别加入0.1 mol N2和0.3 mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。
2NH3(g) ΔH<0的模拟研究,在1 L密闭容器中,分别加入0.1 mol N2和0.3 mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。

与实验①相比,实验②所改变的外界条件可能是___________ ,实验③所改变的外界条件可能为 ___________ 。
(3)400℃时,N2(g)+3H2(g) 2NH3(g) ΔH<0,K1=0.5,则对于反应2NH3(g)
2NH3(g) ΔH<0,K1=0.5,则对于反应2NH3(g)  N2(g)+3H2(g)的化学平衡常数K2=
N2(g)+3H2(g)的化学平衡常数K2=___________ ,若某时刻测得NH3、N2和H2物质的量浓度均为1mol•L-1时,则该反应的v正___________ v逆(填“<”、“>”或“=”)。
(4)某小组往一恒温恒压容器中充入9molN2和23molH2模拟合成氨的反应,如图为不同温度下平衡混合物中氨气的体积分数与总压强(P)的关系图。
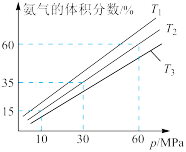
①温度T1、T2、T3中,最大的是___________ 。
②若体系在T2、60MPa下达到平衡如图所示,计算此时N2的平衡转化率为___________ 。
(5)某合成氨速率方程为: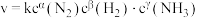 ,根据表中数据,
,根据表中数据,
___________ ;
 2NH3(g) ΔH=-92.4kJ/mol ΔS=-200J·K-1·mol-1。
2NH3(g) ΔH=-92.4kJ/mol ΔS=-200J·K-1·mol-1。 回答下列问题:
(1)合成氨反应在常温下
 填“能”或“不能”
填“能”或“不能” 自发。
自发。(2)某小组进行工业合成氨N2(g)+3H2(g)
 2NH3(g) ΔH<0的模拟研究,在1 L密闭容器中,分别加入0.1 mol N2和0.3 mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。
2NH3(g) ΔH<0的模拟研究,在1 L密闭容器中,分别加入0.1 mol N2和0.3 mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。
与实验①相比,实验②所改变的外界条件可能是
(3)400℃时,N2(g)+3H2(g)
 2NH3(g) ΔH<0,K1=0.5,则对于反应2NH3(g)
2NH3(g) ΔH<0,K1=0.5,则对于反应2NH3(g)  N2(g)+3H2(g)的化学平衡常数K2=
N2(g)+3H2(g)的化学平衡常数K2=(4)某小组往一恒温恒压容器中充入9molN2和23molH2模拟合成氨的反应,如图为不同温度下平衡混合物中氨气的体积分数与总压强(P)的关系图。

①温度T1、T2、T3中,最大的是
②若体系在T2、60MPa下达到平衡如图所示,计算此时N2的平衡转化率为
(5)某合成氨速率方程为:
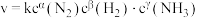 ,根据表中数据,
,根据表中数据,
| 实验 | c(N2)/mol/L | c(H2)/mol/L | c(NH3)/mol/L | v/mol·L-1·s-1 |
| 1 | m | n | p | q |
| 2 | 2m | n | p | 2q |
| 3 | m | n | 0.1p | 10q |
| 4 | m | 2n | p | 2.828q |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】我国在应对气候变化工作中取得显著成效,并向国际社会承诺2030年“碳达峰”,2060年实现“碳中和”。因此将CO2转化为高附加值化学品成为科学家研究的重要课题。
Ⅰ.研究表明CO2与CH4在催化剂存在下可发生反应制得合成气: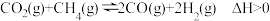
(1)此反应的活化能Ea(正)___________ Ea(逆)(填“>”、“=”或“<”),利于反应自发进行的条件是___________ (填“高温”或“低温”)。
(2)某温度下,向一恒容密闭容器中充入CO2和CH4发生上述反应,初始时CO2和CH4的分压分别为15kPa、20kPa,一段时间达到平衡后,测得体系压强增加了10kPa,则该反应的平衡常数Kp=___________ (kPa)2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅱ.CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应A: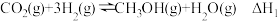
反应B: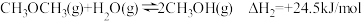
反应C: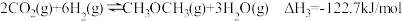
(3) =
=___________ kJ/mol。
(4)已知:某温度下,反应B的平衡常数的值为4,向密闭容器中加入CH3OCH3(g)和H2O(g)各2mol,则平衡时CH3OCH3的转化率为___________ 。
(5)恒压下将CO2和H2按体积比1:3混合,在不同催化剂作用下发生反应A和反应C,在相同的时间段内CH3OH的产率、选择性随温度的变化如图所示。
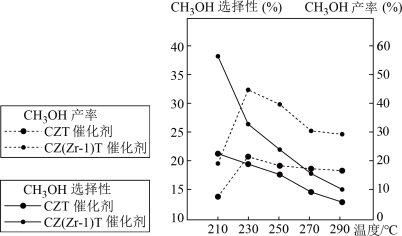
其中的CH3OH选择性
①当温度高于230℃时,CH3OH产率下降的可能原因是___________ 。
②在上述条件下合成甲醇的工业条件是___________ (填序号)。
A.210℃ B.230℃ C.CZT催化剂 D.CZ(Zr-1)T催化剂
Ⅲ.以铅蓄电池为电源可将CO2转化为乙烯,其原理如图所示,电解所用电极材料均为惰性电极。已知铅蓄电池总反应式为: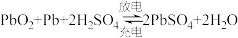

(6)理论上每消耗铅蓄电池中0.3mol硫酸,生成乙烯质量为___________ g。
Ⅰ.研究表明CO2与CH4在催化剂存在下可发生反应制得合成气:
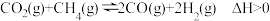
(1)此反应的活化能Ea(正)
(2)某温度下,向一恒容密闭容器中充入CO2和CH4发生上述反应,初始时CO2和CH4的分压分别为15kPa、20kPa,一段时间达到平衡后,测得体系压强增加了10kPa,则该反应的平衡常数Kp=
Ⅱ.CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应A:
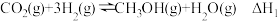
反应B:
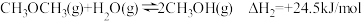
反应C:
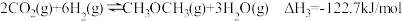
(3)
 =
=(4)已知:某温度下,反应B的平衡常数的值为4,向密闭容器中加入CH3OCH3(g)和H2O(g)各2mol,则平衡时CH3OCH3的转化率为
(5)恒压下将CO2和H2按体积比1:3混合,在不同催化剂作用下发生反应A和反应C,在相同的时间段内CH3OH的产率、选择性随温度的变化如图所示。

其中的CH3OH选择性

①当温度高于230℃时,CH3OH产率下降的可能原因是
②在上述条件下合成甲醇的工业条件是
A.210℃ B.230℃ C.CZT催化剂 D.CZ(Zr-1)T催化剂
Ⅲ.以铅蓄电池为电源可将CO2转化为乙烯,其原理如图所示,电解所用电极材料均为惰性电极。已知铅蓄电池总反应式为:
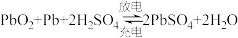

(6)理论上每消耗铅蓄电池中0.3mol硫酸,生成乙烯质量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) △H=41kJ•mol-1
②CO(g)+2H2(g)= CH3OH(g) △H=-90kJ•mol-1
回答下列问题:
(1)总反应的△H=_______ kJ•mol-1。
(2)若反应①为慢反应,下列示意图中能体现上述反应能量变化的是_______ 。
(3)根据以上信息判断CO2与H2制取甲醇的反应自发进行的条件是_______ 。
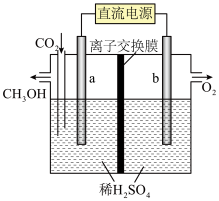
(4)使用惰性电极通过电解原理也可以制取甲醇,其反应装置如图所示,则电极a应该接在电源的_______ 极(填“正”或“负”);生成甲醇的电极反应式为_______ 。
(5)在城市中常会在道路边缘看到有“煤气管道阳极检测桩”,如图所示。这个检测桩可能检测煤气管道上连接的金属_______ 。

①CO2(g)+H2(g)=CO(g)+H2O(g) △H=41kJ•mol-1
②CO(g)+2H2(g)= CH3OH(g) △H=-90kJ•mol-1
回答下列问题:
(1)总反应的△H=
(2)若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
A. | B.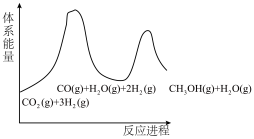 |
C.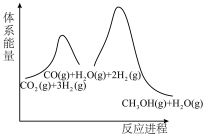 | D.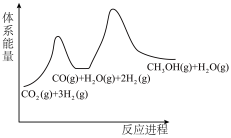 |
(3)根据以上信息判断CO2与H2制取甲醇的反应自发进行的条件是
| A.高温 | B.低温 |
| C.任何温度 | D.任何条件下均不能自发 |
(4)使用惰性电极通过电解原理也可以制取甲醇,其反应装置如图所示,则电极a应该接在电源的

(5)在城市中常会在道路边缘看到有“煤气管道阳极检测桩”,如图所示。这个检测桩可能检测煤气管道上连接的金属

| A.Mg | B.Na | C.Cu | D.Fe |
您最近一年使用:0次
【推荐1】 、
、 是大气污染物,有效去除这些污染物是一项重要课题。
是大气污染物,有效去除这些污染物是一项重要课题。
(1) 、
、 可以先氧化,后用碱吸收。其氧化过程的反应原理如下:
可以先氧化,后用碱吸收。其氧化过程的反应原理如下:
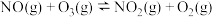 ;
;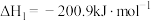
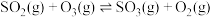 ;
;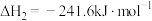
 ;
;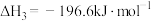
则反应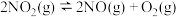 的
的
_______  。
。
一定温度下固定容器中能表明该反应已达到平衡状态的是_______ (填序号)。
A.混合气体的颜色不变 B.体系的压强不变
C.混合气体中 与
与 的比例不变 D.
的比例不变 D.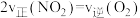
(2)向恒容密闭容器中充入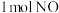 和
和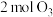 ,发生如下反应:
,发生如下反应: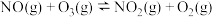 ;
;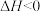 。不同温度下反应相同时间后,体系中
。不同温度下反应相同时间后,体系中 转化率随温度变化曲线如图。温度低于
转化率随温度变化曲线如图。温度低于 时,
时, 转化率随温度升高而增大的主要原因是
转化率随温度升高而增大的主要原因是_______ ;当温度高时, 分解生成活性极高的氧原子,
分解生成活性极高的氧原子, 转化率随温度升高而降低,可能的原因有:①
转化率随温度升高而降低,可能的原因有:①_______ ,②_______ 。
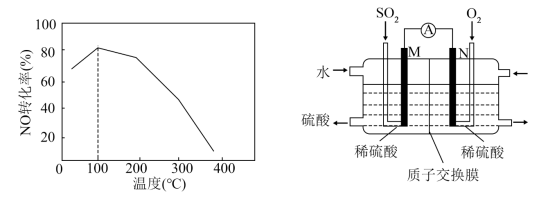
(3)用电化学法模拟工业处理 。将硫酸工业尾气中的
。将硫酸工业尾气中的 通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能:
通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能:
①M极发生的电极反应式为_______ 。
②当外电路通过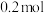 电子时,质子交换膜左侧的溶液质量
电子时,质子交换膜左侧的溶液质量_______ (填“增大”或“减小”)_______ 克。
 、
、 是大气污染物,有效去除这些污染物是一项重要课题。
是大气污染物,有效去除这些污染物是一项重要课题。(1)
 、
、 可以先氧化,后用碱吸收。其氧化过程的反应原理如下:
可以先氧化,后用碱吸收。其氧化过程的反应原理如下: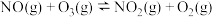 ;
;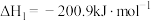
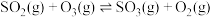 ;
;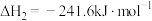
 ;
;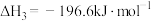
则反应
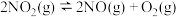 的
的
 。
。一定温度下固定容器中能表明该反应已达到平衡状态的是
A.混合气体的颜色不变 B.体系的压强不变
C.混合气体中
 与
与 的比例不变 D.
的比例不变 D.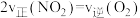
(2)向恒容密闭容器中充入
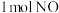 和
和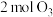 ,发生如下反应:
,发生如下反应: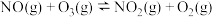 ;
;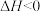 。不同温度下反应相同时间后,体系中
。不同温度下反应相同时间后,体系中 转化率随温度变化曲线如图。温度低于
转化率随温度变化曲线如图。温度低于 时,
时, 转化率随温度升高而增大的主要原因是
转化率随温度升高而增大的主要原因是 分解生成活性极高的氧原子,
分解生成活性极高的氧原子, 转化率随温度升高而降低,可能的原因有:①
转化率随温度升高而降低,可能的原因有:①
(3)用电化学法模拟工业处理
 。将硫酸工业尾气中的
。将硫酸工业尾气中的 通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能:
通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能:①M极发生的电极反应式为
②当外电路通过
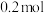 电子时,质子交换膜左侧的溶液质量
电子时,质子交换膜左侧的溶液质量
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氯乙烯是制备塑料的重要中间体,可通过乙炔选择性催化制备。已知:
I.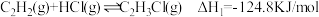
II.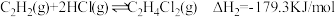
(1) 正反应的活化能为25.8KJ/mol,则其逆反应的活化能为
正反应的活化能为25.8KJ/mol,则其逆反应的活化能为_______ 。
(2)在体积可变的密闭容器中以物质的量之比为1:1充入C2H2(g)和HCl(g),分别在不同压强下发生反应,实验测得乙炔的平衡转化率与温度的关系如图所示。P1、P2、P3由大到小的顺序为_______ ,判断的理由是_______ 。
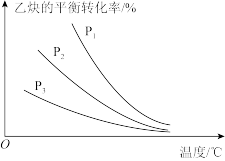
(3)一定温度下,向盛放催化剂的恒容密闭容器中以物质的量之比为1:1充入C2H2(g)和HCl(g),假设只发生反应I和II。实验测得反应前容器内压强为p0Pa,5min达到平衡时C2H4Cl2(g)、HCl(g)的分压分别为p1Pa、p2Pa。
①0~5min内,反应I和反应II中HCl的总的消耗速率v(HCl)=_______ 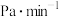 。
。
②反应II的平衡常数Kp=_______ (用含P0、P1、P2的代数式表示)。
(4)电化学腐蚀法可有效将废水中的三氯乙烯转化为乙烯。利用活性纳米Fe电化学腐蚀处理酸性三氯乙烯(C2HCl3)废水的过程如图。定义单位时间内纳米Fe释放的总电子的物质的量为nt,其中用于有效腐蚀的电子的物质的量为ne。
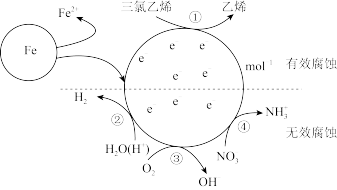
①上述电化学腐蚀过程①的电极反应为_______ 。
②在处理过程中,当消耗amol纳米Fe时,产生bL的乙烯气体(标准状况),则该电化学腐蚀过程的电流效率η=_______ (用含a、b的代数式表示)。[已知: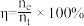 ]
]
I.
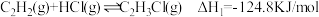
II.
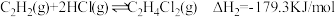
(1)
 正反应的活化能为25.8KJ/mol,则其逆反应的活化能为
正反应的活化能为25.8KJ/mol,则其逆反应的活化能为(2)在体积可变的密闭容器中以物质的量之比为1:1充入C2H2(g)和HCl(g),分别在不同压强下发生反应,实验测得乙炔的平衡转化率与温度的关系如图所示。P1、P2、P3由大到小的顺序为

(3)一定温度下,向盛放催化剂的恒容密闭容器中以物质的量之比为1:1充入C2H2(g)和HCl(g),假设只发生反应I和II。实验测得反应前容器内压强为p0Pa,5min达到平衡时C2H4Cl2(g)、HCl(g)的分压分别为p1Pa、p2Pa。
①0~5min内,反应I和反应II中HCl的总的消耗速率v(HCl)=
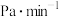 。
。②反应II的平衡常数Kp=
(4)电化学腐蚀法可有效将废水中的三氯乙烯转化为乙烯。利用活性纳米Fe电化学腐蚀处理酸性三氯乙烯(C2HCl3)废水的过程如图。定义单位时间内纳米Fe释放的总电子的物质的量为nt,其中用于有效腐蚀的电子的物质的量为ne。

①上述电化学腐蚀过程①的电极反应为
②在处理过程中,当消耗amol纳米Fe时,产生bL的乙烯气体(标准状况),则该电化学腐蚀过程的电流效率η=
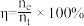 ]
]
您最近一年使用:0次
【推荐3】I.高铁电池作为新型可充电电池,具有放电曲线平坦,高能高容量,原料丰富,绿色无污染等优点。如图为简易的高铁电池的工作装置。已知:放电后,两极都产生红褐色悬浮物。
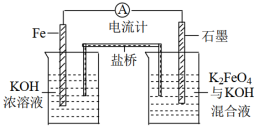
请回答下列问题:
(1)该电池放电时的总反应的离子方程式为_______ 。
(2)该电池充电时阳极反应的电极反应式为_______ 。
(3)放电时,此盐桥中阴离子的运动方向是_______ 。(填“从左向右”或“从右向左”)
II.现用蓄电池Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾。反应装置如图所示:
Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾。反应装置如图所示:
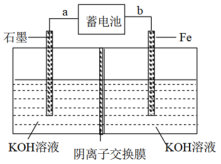
(4)电解时,石墨电极连接的a极上放电的物质为_______ 。(填“Fe”或“NiO2”)
(5)写出电解池中铁电极发生的电极反应式_______ 。
(6)当消耗掉0.1mol NiO2时,生成高铁酸钾_______ g。
III.图中甲池的总反应式为N2H4+O2=N2+2H2O。
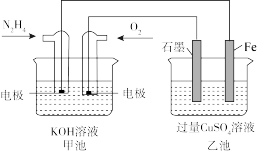
(7)甲池中负极上的电极反应式为_______ 。
(8)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中两个电极质量差为_______ g。

请回答下列问题:
(1)该电池放电时的总反应的离子方程式为
(2)该电池充电时阳极反应的电极反应式为
(3)放电时,此盐桥中阴离子的运动方向是
II.现用蓄电池Fe+NiO2+2H2O
 Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾。反应装置如图所示:
Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾。反应装置如图所示:
(4)电解时,石墨电极连接的a极上放电的物质为
(5)写出电解池中铁电极发生的电极反应式
(6)当消耗掉0.1mol NiO2时,生成高铁酸钾
III.图中甲池的总反应式为N2H4+O2=N2+2H2O。

(7)甲池中负极上的电极反应式为
(8)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中两个电极质量差为
您最近一年使用:0次
【推荐1】含氮物质等被广泛应用于化工、轻工、化肥、制药、合成纤维、塑料等行业中,是最重要的化工产品之一。
(一)发射卫星时可用N2H4为燃料,若用氟作氧化剂,已知:
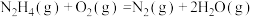
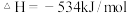
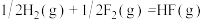
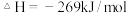
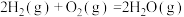
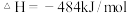
则N2H4与F2反应的热化学方程式为:________ 。
(二)汽车尾气净化反应: △H
△H
(1)该反应的逆反应速率随时间变化的关系如图:
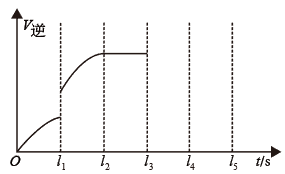
反应在t2时达平衡,在t1时改变了某种条件,改变的条件不可能是________ 。
A. 升温 B. 加压
C. 使用催化剂 D. 增大NO的浓度
(2)某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率及CO2的体积分数变化图如下:
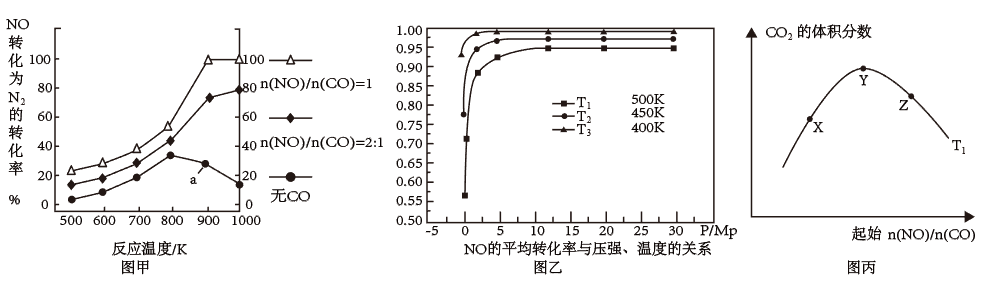
下列说法正确的是________ 。
A. 由图乙可得△H<0,反应低温自发
B. 为达到NO转化为N2的最佳转化率,应该选择的温度为900K,n(NO)/n(CO)=1
C. 图甲中对应的a点一定处于平衡状态
D. 图丙中X、Y、Z三点,CO的转化率由大到小的关系为Z>Y>X
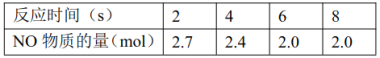
(3)向初始体积为4.5L的密闭容器中通入3molNO、1.5molCO,在恒压条件下发生反应: ,平衡体系中NO的物质的量变化见下表。此温度下,该反应的平衡常数K=
,平衡体系中NO的物质的量变化见下表。此温度下,该反应的平衡常数K=________ 。
(三)尿素被广泛用作氮肥。
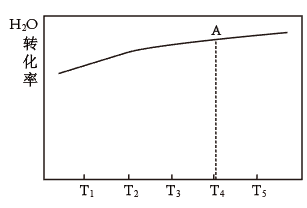
(1)在恒容的密闭容器中,发生反应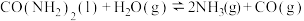 。测得H2O的平衡转化率随温度的变化关系如图所示,已知T4时达平衡所需时间为t。请在图中画出反应经相同时间t时,H2O的转化率随温度变化的曲线。
。测得H2O的平衡转化率随温度的变化关系如图所示,已知T4时达平衡所需时间为t。请在图中画出反应经相同时间t时,H2O的转化率随温度变化的曲线。______________
(2)工业上可通过电解的方法处理尿素 的碱性溶液,产物中无污染物,试写出电解时阳极的电极反应式
的碱性溶液,产物中无污染物,试写出电解时阳极的电极反应式________ 。
(一)发射卫星时可用N2H4为燃料,若用氟作氧化剂,已知:
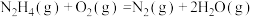
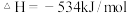
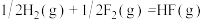
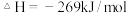
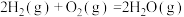
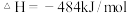
则N2H4与F2反应的热化学方程式为:
(二)汽车尾气净化反应:
 △H
△H(1)该反应的逆反应速率随时间变化的关系如图:

反应在t2时达平衡,在t1时改变了某种条件,改变的条件不可能是
A. 升温 B. 加压
C. 使用催化剂 D. 增大NO的浓度
(2)某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率及CO2的体积分数变化图如下:

下列说法正确的是
A. 由图乙可得△H<0,反应低温自发
B. 为达到NO转化为N2的最佳转化率,应该选择的温度为900K,n(NO)/n(CO)=1
C. 图甲中对应的a点一定处于平衡状态
D. 图丙中X、Y、Z三点,CO的转化率由大到小的关系为Z>Y>X
(3)向初始体积为4.5L的密闭容器中通入3molNO、1.5molCO,在恒压条件下发生反应:
 ,平衡体系中NO的物质的量变化见下表。此温度下,该反应的平衡常数K=
,平衡体系中NO的物质的量变化见下表。此温度下,该反应的平衡常数K=
(三)尿素被广泛用作氮肥。
(1)在恒容的密闭容器中,发生反应
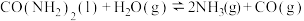 。测得H2O的平衡转化率随温度的变化关系如图所示,已知T4时达平衡所需时间为t。请在图中画出反应经相同时间t时,H2O的转化率随温度变化的曲线。
。测得H2O的平衡转化率随温度的变化关系如图所示,已知T4时达平衡所需时间为t。请在图中画出反应经相同时间t时,H2O的转化率随温度变化的曲线。
(2)工业上可通过电解的方法处理尿素
 的碱性溶液,产物中无污染物,试写出电解时阳极的电极反应式
的碱性溶液,产物中无污染物,试写出电解时阳极的电极反应式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料、防腐等工业,它不溶于H2SO4、HNO3和醇,微溶于水,可溶于盐酸和氨水。在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu2(OH)3Cl]。以海绵铜(主要成分是Cu和少量CuO)为原料。采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
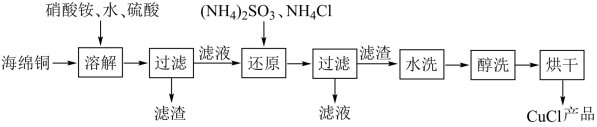
(1)流程中滤液中的主要溶质为_______ (化学式);
(2)写出溶解过程中发生的氧化还原反应的离子方程式:_______ ;
(3)还原过程中发生的主要反应的离子方程式:_______ ;
(4)析出的CuCl晶体水洗后要立即用无水乙醇洗涤,在真空干燥机内于70℃干燥2h,冷却密封包装。70℃真空干燥、密封包装的原因是_ ;
(5)写出氯化亚铜在空气中被氧化的化学方程式_______ ;
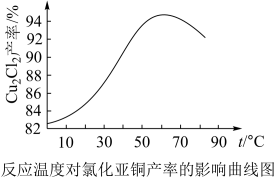
(6)如图是各反应物在最佳配比条件下,反应温度对CuCl产率影响。由图可知,溶液温度控制在60℃时,CuCl产率能达到94%,当温度高于65℃时,CuCl产率会下降,其原因可能是_______ (写两条);
(7)以碳棒为电极电解CuCl2溶液也可得到CuCl,写出电解时阴极上发生的电极反应式:_______ 。

(1)流程中滤液中的主要溶质为
(2)写出溶解过程中发生的氧化还原反应的离子方程式:
(3)还原过程中发生的主要反应的离子方程式:
(4)析出的CuCl晶体水洗后要立即用无水乙醇洗涤,在真空干燥机内于70℃干燥2h,冷却密封包装。70℃真空干燥、密封包装的原因是
(5)写出氯化亚铜在空气中被氧化的化学方程式
(6)如图是各反应物在最佳配比条件下,反应温度对CuCl产率影响。由图可知,溶液温度控制在60℃时,CuCl产率能达到94%,当温度高于65℃时,CuCl产率会下降,其原因可能是

(7)以碳棒为电极电解CuCl2溶液也可得到CuCl,写出电解时阴极上发生的电极反应式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】研究人员研制利用低品位软锰矿浆(主要成分是MnO2)吸收硫酸厂的尾气SO2,制备硫酸锰的生产流程下:

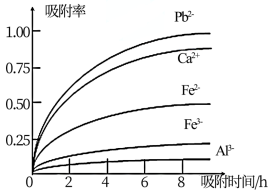
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子.PbO2的氧化性大于MnO2.有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见图2.
(1)浸出过程中生成Mn2+反应的化学方程式为____________ ,
(2)Fe2+被氧化的过程中主要反应的离子方程式_____________ .
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至_______ 范围.
(4)阳离子吸附剂可用于除去杂质金属离子.请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有_____________ 等(写二点).
(5)吸附步骤除去的主要离子为______ .
(6)电解MnSO4、ZnSO4和H2SO4的混合溶液可制备MnO2和Zn,写出阳极的电极反应方程式__________________ .

已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子.PbO2的氧化性大于MnO2.有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见图2.
| 离子 | 离子半径(pm) | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |

(1)浸出过程中生成Mn2+反应的化学方程式为
(2)Fe2+被氧化的过程中主要反应的离子方程式
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至
(4)阳离子吸附剂可用于除去杂质金属离子.请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有
(5)吸附步骤除去的主要离子为
(6)电解MnSO4、ZnSO4和H2SO4的混合溶液可制备MnO2和Zn,写出阳极的电极反应方程式
您最近一年使用:0次



