过氧化氢是用途很广的绿色氧化剂,它的水溶液俗称双氧水,常用于消毒、杀菌、漂白等。试回答下列问题:
(1)写出酸性高锰酸钾和H2O2反应的离子方程式___ 。
(2)Na2O2、K2O2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,然后过滤。则上述最适合的过氧化物是___ 。
(3)甲酸钙[Ca(HCOO)2]广泛用于食品工业生产上,实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛 溶液加入质量分数为30%~70%的过氧化氢溶液中,则该反应的化学方程式为
溶液加入质量分数为30%~70%的过氧化氢溶液中,则该反应的化学方程式为___ 。
(1)写出酸性高锰酸钾和H2O2反应的离子方程式
(2)Na2O2、K2O2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,然后过滤。则上述最适合的过氧化物是
(3)甲酸钙[Ca(HCOO)2]广泛用于食品工业生产上,实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛
 溶液加入质量分数为30%~70%的过氧化氢溶液中,则该反应的化学方程式为
溶液加入质量分数为30%~70%的过氧化氢溶液中,则该反应的化学方程式为
更新时间:2020/10/16 12:11:33
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如下:

(1)步骤(I)中生成的气体是___________ ,溶液A和沉淀分离的操作名称是___________ 。
(2)步骤(II)中加入H2O2溶液后,反应生成Fe2(SO4)3,该反应___________ (填“属于”或“不属于”)氧化还原反应。
(3)步骤(III)中生成Fe(OH)3沉淀的颜色是___________ (填“白色”或“红褐色”)。
(4)步骤(IV)中Fe(OH)3受热分解生成Fe2O3和H2O的化学方程式为___________ 。

(1)步骤(I)中生成的气体是
(2)步骤(II)中加入H2O2溶液后,反应生成Fe2(SO4)3,该反应
(3)步骤(III)中生成Fe(OH)3沉淀的颜色是
(4)步骤(IV)中Fe(OH)3受热分解生成Fe2O3和H2O的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知砒霜As2O3与Zn可以发生如下反应:As2O3+6Zn + 6H2SO4 = 2AsH3↑+ 6ZnSO4+ 3H2O (AsH3中As为-3价)
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目_______ 。
(2)As2O3在上述反应中显示出来的性质是_______。
(3)该反应的还原剂是_______ ,还原产物是_______ 。
(4)若生成0.2 mol AsH3,则转移的电子为_______ mol。
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目
(2)As2O3在上述反应中显示出来的性质是_______。
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
(4)若生成0.2 mol AsH3,则转移的电子为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】大气臭氧层可以保护地球生物免受紫外线的伤害,但低空臭氧的浓度过高时对人体有害。
(1)在紫外线作用下,氧气可转化臭氧:3O2=2O3
①该反应所属类型为___ (填“氧化还原”或“非氧化还原”)。
②若在上述反应中有60%的氧气转化为臭氧,所得混合气体的平均摩尔质量为___ 。
③某区域收集到O2和O3混合气体0.96g,标准状况下体积为0.56L,其中O2与O3的体积之比为___ 。
(2)复印机工作时易产生臭氧,会使湿润的KI淀粉试纸变蓝,其中臭氧部分转化为氧气。写出反应的化学方程式___ 。
(3)实验室中常用碘量法检测臭氧,其中以淀粉为指示剂,将臭氧通入碘化钾溶液中进行反应。现需450mL0.2mol/L的KI溶液,用KI固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒、细口试剂瓶。
①还缺少的仪器有___ (写名称),所需KI固体的质量为___ 。
②在配制过程中,下列操作会导致所配制溶液的浓度偏小的是___ 。
A.未洗涤烧杯和玻璃棒
B.使用前,容量瓶中有少量蒸馏水
C.定容时俯视凹液面
D.定容摇匀后静置,液面低于刻度线,继续加水至刻度线
(1)在紫外线作用下,氧气可转化臭氧:3O2=2O3
①该反应所属类型为
②若在上述反应中有60%的氧气转化为臭氧,所得混合气体的平均摩尔质量为
③某区域收集到O2和O3混合气体0.96g,标准状况下体积为0.56L,其中O2与O3的体积之比为
(2)复印机工作时易产生臭氧,会使湿润的KI淀粉试纸变蓝,其中臭氧部分转化为氧气。写出反应的化学方程式
(3)实验室中常用碘量法检测臭氧,其中以淀粉为指示剂,将臭氧通入碘化钾溶液中进行反应。现需450mL0.2mol/L的KI溶液,用KI固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒、细口试剂瓶。
①还缺少的仪器有
②在配制过程中,下列操作会导致所配制溶液的浓度偏小的是
A.未洗涤烧杯和玻璃棒
B.使用前,容量瓶中有少量蒸馏水
C.定容时俯视凹液面
D.定容摇匀后静置,液面低于刻度线,继续加水至刻度线
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】化学用语是化学学科的特色语言,化学用语可以准确表述化学现象、变化以及本质。完成下列有关方程式。
(1)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO ,常用作脱氯剂,该反应的离子方程式为:
,常用作脱氯剂,该反应的离子方程式为:_______ 。
(2)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:_______ 、_______ 。
(1)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO
 ,常用作脱氯剂,该反应的离子方程式为:
,常用作脱氯剂,该反应的离子方程式为:(2)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】硫化氢气体在资源利用和环境保护等方面均有重要应用。
(1)工业可采用分解 的方法制取氢气。在容积为
的方法制取氢气。在容积为 的恒容密闭容器中,控制不同温度进行此反应。
的恒容密闭容器中,控制不同温度进行此反应。 的起始物质的量均为
的起始物质的量均为 ,在相同时间内,
,在相同时间内, 的实际转化率和平衡转化率与温度的关系如图所示。(曲线a表示
的实际转化率和平衡转化率与温度的关系如图所示。(曲线a表示 的平衡转化率,曲线b表示
的平衡转化率,曲线b表示 的实际转化率)
的实际转化率)
则 分解产生
分解产生 和
和 的热化学方程式为
的热化学方程式为_______ 。
②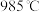 时,反应经过
时,反应经过 达到平衡状态,此时
达到平衡状态,此时 的转化率为
的转化率为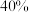 ,则用
,则用 表示的反应速率为
表示的反应速率为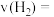
_______ 。
③随着 分解温度的升高,曲线b向曲线a逐渐靠近,其原因是
分解温度的升高,曲线b向曲线a逐渐靠近,其原因是_______ 。
(2)将 和空气的混合气体通入
和空气的混合气体通入 、
、 、
、 的混合溶液中反应回收S,其物质转化如图所示。
的混合溶液中反应回收S,其物质转化如图所示。_______ 。
②图示中反应Ⅲ的离子方程式为_______ 。
③在温度一定和不补加 溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含 ,可采取的措施有
,可采取的措施有_______ 。(写出一条即可)
(1)工业可采用分解
 的方法制取氢气。在容积为
的方法制取氢气。在容积为 的恒容密闭容器中,控制不同温度进行此反应。
的恒容密闭容器中,控制不同温度进行此反应。 的起始物质的量均为
的起始物质的量均为 ,在相同时间内,
,在相同时间内, 的实际转化率和平衡转化率与温度的关系如图所示。(曲线a表示
的实际转化率和平衡转化率与温度的关系如图所示。(曲线a表示 的平衡转化率,曲线b表示
的平衡转化率,曲线b表示 的实际转化率)
的实际转化率)
| 化学键 |  |  |  |
键能( ) ) | 436 | 425 | 347 |
 分解产生
分解产生 和
和 的热化学方程式为
的热化学方程式为②
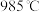 时,反应经过
时,反应经过 达到平衡状态,此时
达到平衡状态,此时 的转化率为
的转化率为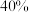 ,则用
,则用 表示的反应速率为
表示的反应速率为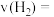
③随着
 分解温度的升高,曲线b向曲线a逐渐靠近,其原因是
分解温度的升高,曲线b向曲线a逐渐靠近,其原因是(2)将
 和空气的混合气体通入
和空气的混合气体通入 、
、 、
、 的混合溶液中反应回收S,其物质转化如图所示。
的混合溶液中反应回收S,其物质转化如图所示。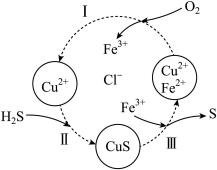
②图示中反应Ⅲ的离子方程式为
③在温度一定和
 ,可采取的措施有
,可采取的措施有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】请将下列五种物质:KMnO4、MnSO4、FeSO4、Fe2(SO4)3、K2SO4分别填入下列对应的横线上,组成一个未配平的化学方程式:
(1)______ +______ + H2SO4→______ +______ +______ +H2O ;
(2)该反应中的氧化产物是_______ (填写化学式),被还原的是_______ (填写化学式)中的____ (填写元素符号)元素;
(3)有1mol氧化剂参与反应,转移电子数为_________ 。
(1)
(2)该反应中的氧化产物是
(3)有1mol氧化剂参与反应,转移电子数为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】“人生有酒须当醉,一滴何曾到九泉”这是关于酒的诗句,酒在我国历史上有着非常悠久的文化蕴涵,自古以来文人大多对酒也情有独钟。乙醇俗名又叫酒精,已知乙醇(C2H5OH)能与K2Cr2O7和H2SO4的混合溶液在一定条件下发生反应:2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O。Cr2O 和Cr3+和在溶液中分别显橙色和绿色,回答下列问题:
和Cr3+和在溶液中分别显橙色和绿色,回答下列问题:
1.该反应_______ (填“是”或“不是”)离子反应。
2.写出Cr2(SO4)3的电离方程式:_______ 。
3.该反应__________ (填“是”或“不是”)氧化还原反应,判断的依据是________ 。
4.你认为能否用这一反应来检测司机是否酒驾_______ (填“能”或“不能”),简述其原理:_______ 。
 和Cr3+和在溶液中分别显橙色和绿色,回答下列问题:
和Cr3+和在溶液中分别显橙色和绿色,回答下列问题:1.该反应
2.写出Cr2(SO4)3的电离方程式:
3.该反应
4.你认为能否用这一反应来检测司机是否酒驾
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】氧化还原反应在工农业生产和日常生活中有广泛的应用,回答下列问题:
(1)罐头厂在装食品罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质,此类食物防腐剂应具有________ (填“氧化性”或“还原性”)。
(2)氯气是一种重要的工业原料且HCl遇NH3会产生NH4Cl,NH4Cl为白色固体。工业上利用反应3Cl2+2NH3===N2+6HCl检查氯气管道是否漏气。下列说法错误的是________ 。
A.若管道漏气遇NH3就会产生白烟
B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应
D.生成1分子N2有6个电子转移
(3)菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有+5价砷,西红柿中含有比较多的维生素C,两者同时食用会生成有毒的+3价砷。下列说法中,正确的是(________ )
A.在该反应中维生素C作催化剂
B.由上述信息可推知砒霜中含有的砷是+3价
C.上述反应中维生素C作氧化剂
D.因为河虾中含有砷元素,所以不能食用
(1)罐头厂在装食品罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质,此类食物防腐剂应具有
(2)氯气是一种重要的工业原料且HCl遇NH3会产生NH4Cl,NH4Cl为白色固体。工业上利用反应3Cl2+2NH3===N2+6HCl检查氯气管道是否漏气。下列说法错误的是
A.若管道漏气遇NH3就会产生白烟
B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应
D.生成1分子N2有6个电子转移
(3)菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有+5价砷,西红柿中含有比较多的维生素C,两者同时食用会生成有毒的+3价砷。下列说法中,正确的是(
A.在该反应中维生素C作催化剂
B.由上述信息可推知砒霜中含有的砷是+3价
C.上述反应中维生素C作氧化剂
D.因为河虾中含有砷元素,所以不能食用
(4)在酸性条件下,Fe2O 容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O
容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O 、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中氧化剂的是
、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中氧化剂的是
您最近一年使用:0次



