某硫铁矿厂开采的黄铁矿(主要成分是FeS2),是生产H2SO4的重要原料。利用黄铁矿生产H2SO4的第一步反应为:4FeS2+11O2=2Fe2O3+8X。所得产物Fe2O3是冶炼铁的重要原料。回答下列问题:
(1)已知FeS2中Fe的化合价为+2,则S的化合价为_____ 。
(2)X的化学式是_____ 。
(3)写出高炉中Fe2O3转化成铁的化学方程式_____ 。
(1)已知FeS2中Fe的化合价为+2,则S的化合价为
(2)X的化学式是
(3)写出高炉中Fe2O3转化成铁的化学方程式
21-22高一上·浙江·阶段练习 查看更多[1]
(已下线)【2021】【高一上】【分班考】【65】
更新时间:2023-03-09 17:31:32
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】“神舟六号”宇宙飞船是靠长征Ⅱ(F)型运载火箭发射升空的。该火箭所用的燃料是偏二甲肼[(CH3)2NNH2],氧化剂是N2O4,产物是氮气、二氧化碳和水。
(1)火箭点火瞬间,逸出的红棕色气体是________ ,产生该气体的化学反应方程式为________________________________ 。
(2)偏二甲肼在N2O4中燃烧的化学方程式为____________________ ,当有1 mol 偏二甲肼燃烧时,转移电子的物质的量为________________________________ 。
(1)火箭点火瞬间,逸出的红棕色气体是
(2)偏二甲肼在N2O4中燃烧的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】元素周期表中第ⅦA 族元素的单质及其化合物的用途广泛。
(1)能作为氯、溴、碘元素非金属性递变规律的判断依据是_______ (填序号)
a.Cl2、Br2、I2的熔点 b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI 的热稳定性 d.HCl、HBr、HI 的酸性
(2)工业上,通过如下转化可制得 KClO3 晶体:
NaCl溶液 NaClO3
NaClO3
_____ KClO3晶体
①完成 I 中反应的总化学方程式:_______ NaCl+________ H2O =_______ NaClO3+_______ 。
②反应Ⅰ中 NaClO3是_______ 极(选填“阴”或“阳”极)产物。
③Ⅱ中转化的基本反应类型是_________ ,该反应过程能析出 KClO3晶体而无其它晶体析出的原因是_______ 。
(3)一定条件,在水溶液中 1 mol Cl-、ClOX-(x=1,2,3,4)的能量(kJ)相对大小如图所示。
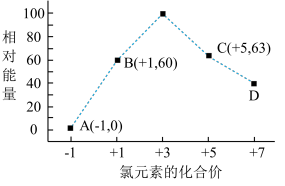
①D 是_______ (填离子符号)。
②B→A+C 反应的离子方程式为_______ ;生成 1mol C 时,________ (填吸收或放热)________ kJ 的能量
(1)能作为氯、溴、碘元素非金属性递变规律的判断依据是
a.Cl2、Br2、I2的熔点 b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI 的热稳定性 d.HCl、HBr、HI 的酸性
(2)工业上,通过如下转化可制得 KClO3 晶体:
NaCl溶液
 NaClO3
NaClO3
①完成 I 中反应的总化学方程式:
②反应Ⅰ中 NaClO3是
③Ⅱ中转化的基本反应类型是
(3)一定条件,在水溶液中 1 mol Cl-、ClOX-(x=1,2,3,4)的能量(kJ)相对大小如图所示。

①D 是
②B→A+C 反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答下列小题。
(1)有下列四个反应:
①SO3+H2O=H2SO4 ②Cl2+H2O=HCl+HClO ③2F2+2H2O=4HF+O2 ④SO2+2NaOH=Na2SO3+H2O上述反应中不属于氧化还原反应的是___________ (填序号,下同);H2O只作还原剂的是___________ ;属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是___________ 。
(2)为治理汽车尾气中的NO和CO对环境的污染,可利用反应
①用单线桥标出电子转移的方向和数目___________ ;
②若消耗3g的NO得到氧化产物的质量为___________ g。
(3)我国古代炼丹术中用的铅丹与硝酸反应方程式是:X(铅丹)+4HNO3=PbO2+2Pb(NO3)2+2H2O,则铅丹的化学式为___________ ,铅丹可以由一氧化铅(PbO)在空气中加热至500℃制备,制备铅丹的化学方程式为___________ 。
(4)写出SO3和NaOH溶液反应的离子方程式___________ 。
(1)有下列四个反应:
①SO3+H2O=H2SO4 ②Cl2+H2O=HCl+HClO ③2F2+2H2O=4HF+O2 ④SO2+2NaOH=Na2SO3+H2O上述反应中不属于氧化还原反应的是
(2)为治理汽车尾气中的NO和CO对环境的污染,可利用反应

①用单线桥标出电子转移的方向和数目
②若消耗3g的NO得到氧化产物的质量为
(3)我国古代炼丹术中用的铅丹与硝酸反应方程式是:X(铅丹)+4HNO3=PbO2+2Pb(NO3)2+2H2O,则铅丹的化学式为
(4)写出SO3和NaOH溶液反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】请按要求填空(有序号均填序号):
(1)下列五组物质,互为同分异构体的是_____________ ,互为同素异形体是_____________ ,互为同位素的是_____________ 。
①金刚石和石墨 ② 和
和 ③
③ 和
和 ④
④ 和
和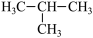 ⑤
⑤ 和
和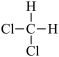
(2)下述过程中有离子键断裂的是_____________ ,有共价键断裂的_____________ ,仅克服分子间作用力的是_____________ 。
①氯化钠晶体熔化 ②碘升华 ③电解水 ④干冰汽化
(3)常用的金属冶炼方法有:①热分解法 ②高温还原法 ③电解法等;
工业上冶炼铁的主要方法是_____________ ,冶炼铝的主要方法是_____________ ;利用铝热反应可焊接铁轨,反应的化学反应方程式为____________________________________________________ 。
(1)下列五组物质,互为同分异构体的是
①金刚石和石墨 ②
 和
和 ③
③ 和
和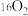 ④
④ 和
和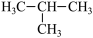 ⑤
⑤ 和
和
(2)下述过程中有离子键断裂的是
①氯化钠晶体熔化 ②碘升华 ③电解水 ④干冰汽化
(3)常用的金属冶炼方法有:①热分解法 ②高温还原法 ③电解法等;
工业上冶炼铁的主要方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】化学与生活密切相关.
(1)下列生活用品中,其主要材料属于天然纤维的是_________ (填字母序号);
A.塑料保鲜薄 B.橡胶手套 C.棉布围裙
(2)我们常用的洗涤剂清洗餐具上的油污,这是因为洗涤剂具有_________ 的功能;
(3)食用水果、蔬菜主要补充人体所需的_________ ;
(4)国家禁止在面粉中添加增白剂过氧化钙CaO2,过氧化钙中氧元素的化合价为_______ ;
(5)农业上降低土壤酸性的是_________ (填化学式);
(6)生活中要用到大量的钢铁,写出赤铁矿(主要成分Fe2O3)冶炼成铁的化学方程式______ 。
(1)下列生活用品中,其主要材料属于天然纤维的是
A.塑料保鲜薄 B.橡胶手套 C.棉布围裙
(2)我们常用的洗涤剂清洗餐具上的油污,这是因为洗涤剂具有
(3)食用水果、蔬菜主要补充人体所需的
(4)国家禁止在面粉中添加增白剂过氧化钙CaO2,过氧化钙中氧元素的化合价为
(5)农业上降低土壤酸性的是
(6)生活中要用到大量的钢铁,写出赤铁矿(主要成分Fe2O3)冶炼成铁的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】硫是一种黄色晶体。硫元素有多种化合价。仔细观察下列物质中硫的化合价及排列顺序:H2S(Na2S)、S、SO2(X、Na2SO3)、Y(H2SO4、Na2SO4)。回答下列问题:
(1)在Na2S中,硫元素的化合价是____ 。
(2)参考Y后边的表述,X是一种含氧酸,X的化学式为____ 。
(3)Y+____ =H2SO4。
(4)在反应2H2S+SO2=3S+2H2O中,氧化产物和还原产物都是S,则氧化产物和还原产物的个数比是____ 。
(5)SO2能使酸性高锰酸钾溶液紫色褪去。发生的反应如下:5SO2+2 +2H2O=2Mn2++5Z+4H+。实验室检验Z离子常用的试剂是
+2H2O=2Mn2++5Z+4H+。实验室检验Z离子常用的试剂是____ 。
(1)在Na2S中,硫元素的化合价是
(2)参考Y后边的表述,X是一种含氧酸,X的化学式为
(3)Y+
(4)在反应2H2S+SO2=3S+2H2O中,氧化产物和还原产物都是S,则氧化产物和还原产物的个数比是
(5)SO2能使酸性高锰酸钾溶液紫色褪去。发生的反应如下:5SO2+2
 +2H2O=2Mn2++5Z+4H+。实验室检验Z离子常用的试剂是
+2H2O=2Mn2++5Z+4H+。实验室检验Z离子常用的试剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】请利用原子结构的知识回答下列问题。
(1)预测:金属钠和金属铝哪一种更容易与氟气反应_______ ?为什么_______ ?
(2)元素的化合价与原子的电子层结构,特别是最外层电子数有关。请尝试概括核电荷数为1~20的元素的化合价与元素原子最外层电子数之间的关系_______ 。
(1)预测:金属钠和金属铝哪一种更容易与氟气反应
(2)元素的化合价与原子的电子层结构,特别是最外层电子数有关。请尝试概括核电荷数为1~20的元素的化合价与元素原子最外层电子数之间的关系
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
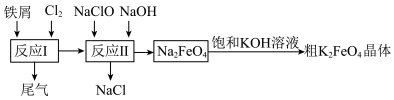
【推荐3】高铁酸钾(K2FeO4)有强氧化性,是一种环保、高效、多功能饮用水处理剂,受热易分解,酸性环境中易变质。制备流程如图所示:
(1)K2FeO4中铁的化合价为______ ,提纯K2FeO4的实验方法是______ 。
(2)铁屑需事先用Na2CO3溶液洗涤,目的是______ 。
(3)K2FeO4处理饮用水的原理是______ 。
(4)已知K2FeO4难溶于乙醇,可溶于水,故洗涤K2FeO4晶体时,先使用冷水洗涤,再使用乙醇洗涤,简述用乙醇洗涤K2FeO4晶体的操作______ 。
(1)K2FeO4中铁的化合价为
(2)铁屑需事先用Na2CO3溶液洗涤,目的是
(3)K2FeO4处理饮用水的原理是
(4)已知K2FeO4难溶于乙醇,可溶于水,故洗涤K2FeO4晶体时,先使用冷水洗涤,再使用乙醇洗涤,简述用乙醇洗涤K2FeO4晶体的操作
您最近一年使用:0次



