“神舟六号”宇宙飞船是靠长征Ⅱ(F)型运载火箭发射升空的。该火箭所用的燃料是偏二甲肼[(CH3)2NNH2],氧化剂是N2O4,产物是氮气、二氧化碳和水。
(1)火箭点火瞬间,逸出的红棕色气体是________ ,产生该气体的化学反应方程式为________________________________ 。
(2)偏二甲肼在N2O4中燃烧的化学方程式为____________________ ,当有1 mol 偏二甲肼燃烧时,转移电子的物质的量为________________________________ 。
(1)火箭点火瞬间,逸出的红棕色气体是
(2)偏二甲肼在N2O4中燃烧的化学方程式为
更新时间:2018-08-05 11:18:09
|
相似题推荐
【推荐1】在下列括号中填上系数,并完成相应空格:
(1)( ) CO + ( ) NO = ( ) N2 + ( ) CO2在此反应中属于氧化剂的是 _____ ,CO在反应中表现出 ____ 性。
(2)( ) ClO— + ( ) Fe3+ + 10 OH— = ( ) FeO +
+ ( ) Cl— + 5H2O在此反应中属于还原剂的是 _____ ,属于氧化产物的是 ____ 。
(1)
(2)
 +
+
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】已知氮元素及其化合物的转化关系如下图所示,回答下列问题。_______ 。
(2)反应④的离子方程式为_______ 。理论上如图N2合成1mol硝酸,至少需要氧气共_______ mol。
(3)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示,该过程的总反应化学方程式为_______ 。
①根据上图得知_______ (填字母)。
A.NaOH溶液浓度越大,氮氧化物的吸收率越大
B.NO2含量越大,氮氧化物的吸收率越大
②当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是_______ 。

(2)反应④的离子方程式为
(3)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示,该过程的总反应化学方程式为
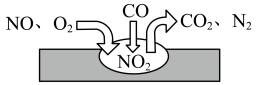

①根据上图得知
A.NaOH溶液浓度越大,氮氧化物的吸收率越大
B.NO2含量越大,氮氧化物的吸收率越大
②当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】硅单质及其化合物应用范围很广。
(1)制备硅半导体材料必须先得到高纯硅,工业上可以按如下步骤制备高纯硅。
Ⅰ.高温下用碳还原二氧化硅制得粗硅;
Ⅱ.粗硅与干燥的氯气在450~500 ℃条件下反应制得SiCl4;
Ⅲ.SiCl4液体经精馏提纯后与过量H2在1 100~1 200 ℃条件下反应制得高纯硅。
已知SiCl4沸点为57.6 ℃,能与H2O强烈反应。
请回答下列问题:
①第Ⅲ步反应的化学方程式为____________________________________ 。
②整个制备纯硅的过程中必须严格控制在无水无氧的条件下。SiCl4在潮湿的空气中因水解而产生白色烟雾,其生成物是_______ ;H2还原SiCl4过程中若混入O2,可能引起的后果是________________________________________ 。
(2)二氧化硅被大量用于生产玻璃。工业上用SiO2、Na2CO3和CaCO3共283 kg在高温下完全反应时放出CO2 44 kg,生产出的玻璃可用化学式Na2SiO3·CaSiO3·xSiO2表示,则其中x=________ 。
(1)制备硅半导体材料必须先得到高纯硅,工业上可以按如下步骤制备高纯硅。
Ⅰ.高温下用碳还原二氧化硅制得粗硅;
Ⅱ.粗硅与干燥的氯气在450~500 ℃条件下反应制得SiCl4;
Ⅲ.SiCl4液体经精馏提纯后与过量H2在1 100~1 200 ℃条件下反应制得高纯硅。
已知SiCl4沸点为57.6 ℃,能与H2O强烈反应。
请回答下列问题:
①第Ⅲ步反应的化学方程式为
②整个制备纯硅的过程中必须严格控制在无水无氧的条件下。SiCl4在潮湿的空气中因水解而产生白色烟雾,其生成物是
(2)二氧化硅被大量用于生产玻璃。工业上用SiO2、Na2CO3和CaCO3共283 kg在高温下完全反应时放出CO2 44 kg,生产出的玻璃可用化学式Na2SiO3·CaSiO3·xSiO2表示,则其中x=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】足量铜与一定量的浓硝酸反应,得到硝酸铜溶液、 、NO和
、NO和 的混合气体。这些气体与5.6L(标准状况下)的
的混合气体。这些气体与5.6L(标准状况下)的 混合后通入水中,所有气体恰好完全被水吸收生成硝酸。(已知:
混合后通入水中,所有气体恰好完全被水吸收生成硝酸。(已知: )
)
(1)写出上述反应中所涉及到的反应方程式_______ (是离子反应的只写离子方程式)。
(2)消耗的Cu的质量是_______ g,整个实验过程(包括后续气体与 混合通入水中)中消耗的硝酸的物质的量是
混合通入水中)中消耗的硝酸的物质的量是_______ mol。
 、NO和
、NO和 的混合气体。这些气体与5.6L(标准状况下)的
的混合气体。这些气体与5.6L(标准状况下)的 混合后通入水中,所有气体恰好完全被水吸收生成硝酸。(已知:
混合后通入水中,所有气体恰好完全被水吸收生成硝酸。(已知: )
)(1)写出上述反应中所涉及到的反应方程式
(2)消耗的Cu的质量是
 混合通入水中)中消耗的硝酸的物质的量是
混合通入水中)中消耗的硝酸的物质的量是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】化学上用分类法学习化学物质的共性,用比较法学习化学物质的特性,物质的氧化性与还原性尤为重要。回答下列问题:
(1)磷元素的含氧酸有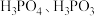 (亚磷酸)、
(亚磷酸)、 (次磷酸)等多种,其中已知:
(次磷酸)等多种,其中已知:
 (过量)
(过量)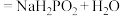 。
。 属于
属于_______ (填“一”、“二”或“三”)元酸。 属于
属于_______ (填“正盐”或“酸式盐”)。
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式,并用单线桥表示电子转移的方向和数目:______

(3)某种钇矿石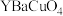 (其中化合价分别为
(其中化合价分别为 )溶于稀盐酸不产生污染,其中
)溶于稀盐酸不产生污染,其中 的价态不变,
的价态不变,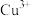 全部被还原为
全部被还原为 ,写出该反应的离子方程式
,写出该反应的离子方程式_______ 。
(4) (B为+3价)、
(B为+3价)、 与相同氧化剂反应时,
与相同氧化剂反应时,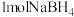 的还原能力相当于
的还原能力相当于_______  的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同)。
的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同)。
(5)已知酸性 ,少量
,少量 与
与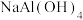 反应的离子方程式为
反应的离子方程式为_______ ,漂白液在空气中放置一段时间后漂白效果更佳的原理的离子方程式为_______ 。
(1)磷元素的含氧酸有
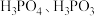 (亚磷酸)、
(亚磷酸)、 (次磷酸)等多种,其中已知:
(次磷酸)等多种,其中已知: (过量)
(过量)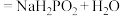 。
。 属于
属于 属于
属于(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式,并用单线桥表示电子转移的方向和数目:

(3)某种钇矿石
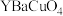 (其中化合价分别为
(其中化合价分别为 )溶于稀盐酸不产生污染,其中
)溶于稀盐酸不产生污染,其中 的价态不变,
的价态不变,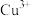 全部被还原为
全部被还原为 ,写出该反应的离子方程式
,写出该反应的离子方程式(4)
 (B为+3价)、
(B为+3价)、 与相同氧化剂反应时,
与相同氧化剂反应时,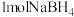 的还原能力相当于
的还原能力相当于 的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同)。
的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同)。(5)已知酸性
 ,少量
,少量 与
与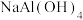 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次

 与
与 在一定条件下可以形成
在一定条件下可以形成 、
、 (两种化合物中F均显-1价)。现有标准状况下的
(两种化合物中F均显-1价)。现有标准状况下的 。
。 氧化成
氧化成 ,并生成
,并生成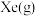 和
和 。将上述标准状况下的混合气体1L通入含过量
。将上述标准状况下的混合气体1L通入含过量


