某工厂废水中含KCN,其浓度为650mg•L-1,现用氯氧化法处理,发生如下反应(化合物中 化合价均为-3):
化合价均为-3):
(1)KCN+2KOH+Cl2=KOCN+2KCl+H2O中被氧化的元素是___ 。
(2)通入过量氯气,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:___ KOCN+___ KOH+___ Cl2=___ CO2+___ N2+___ KCl+___ H2O。
(3)若将5m3含KCN的浓度为650mg•L-1的废水中KCN氧化成N2除去,需要标准状况下的氯气的体积为___ L。
 化合价均为-3):
化合价均为-3):(1)KCN+2KOH+Cl2=KOCN+2KCl+H2O中被氧化的元素是
(2)通入过量氯气,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:
(3)若将5m3含KCN的浓度为650mg•L-1的废水中KCN氧化成N2除去,需要标准状况下的氯气的体积为
更新时间:2020-10-16 12:11:33
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知铅(Pb)与硅同主族且Pb比Si多3个电子层。
(1)难溶物PbSO4溶于CH3COONH4溶液可制得(CH3COO)2Pb[(CH3COO)2Pb易溶于水],发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是______ (填“强”或“弱”)电解质。
(2)将PbO2加入硝酸酸化的Mn(NO3)2溶液中搅拌后溶液显紫红色;则每反应1 mol Mn(NO3)2转移____________ mol电子。
(3)在汽车尾气系统中装置催化转化器,可有效降低尾气中的CO、NO、NO2和碳氢化合物等污染性气体。在催化转换器的前半部,CO和NO在催化剂的作用下发生反应,生成两种无污染的气体,该反应的化学方程式为:___________________________________ 。
(4)①在淀粉碘化钾溶液中,滴加少量次氯酸钠溶液,溶液变蓝色,且反应后溶液呈碱性,发生反应的离子方程式是______________ 。
②在上述碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠溶液,发现蓝色逐渐消失,写出发生反应的离子方程式是______________ 。
(5)处理含Cr2O72-的废水可先用(NH4)2Fe(SO4)2将Cr2O72-转化为Cr3+,再用氨水将Cr3+转变为难溶的Cr(OH)3,在该过程中氧化剂为______________ ,其中氨水转化Cr3+为Cr(OH)3的离子方程式为____________________________________________ ;该方案处理后的废水中因含有大量________ 元素,直接排放会导致水体富营养化。
(1)难溶物PbSO4溶于CH3COONH4溶液可制得(CH3COO)2Pb[(CH3COO)2Pb易溶于水],发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是
(2)将PbO2加入硝酸酸化的Mn(NO3)2溶液中搅拌后溶液显紫红色;则每反应1 mol Mn(NO3)2转移
(3)在汽车尾气系统中装置催化转化器,可有效降低尾气中的CO、NO、NO2和碳氢化合物等污染性气体。在催化转换器的前半部,CO和NO在催化剂的作用下发生反应,生成两种无污染的气体,该反应的化学方程式为:
(4)①在淀粉碘化钾溶液中,滴加少量次氯酸钠溶液,溶液变蓝色,且反应后溶液呈碱性,发生反应的离子方程式是
②在上述碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠溶液,发现蓝色逐渐消失,写出发生反应的离子方程式是
(5)处理含Cr2O72-的废水可先用(NH4)2Fe(SO4)2将Cr2O72-转化为Cr3+,再用氨水将Cr3+转变为难溶的Cr(OH)3,在该过程中氧化剂为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】化合物KaFeb(C2O4)c·dH2O(其中铁为正三价)是重要的光化学试剂。通过下述实验确定该晶体的组成。
步骤a:称取该样品4.91g溶于水中配成250mL溶液,取出25mL溶液,向其中加入过量的NaOH溶液,将沉淀过滤,洗涤,高温灼烧至质量不再改变,称量其固体的质量为0.08g。
步骤b:另取出25mL溶液,加入适量稀H2SO4溶液,用0.050 mol·L-1KMnO4溶液滴定,到达滴定终点时,消耗KMnO4溶液24.00mL。
已知:_____ KMnO4+___ H2C2O4+____ H2SO4=____ MnSO4+____ K2SO4+____ CO2+____ H2O
(1) 配平上述反应方程式
(2) 草酸为二元弱酸,其一级电离的方程式为______________________ 。
(3)滴定终点观察到的现象为_____________________________________ 。
(4)通过计算确定样品的组成(写出计算过程)。______________________
步骤a:称取该样品4.91g溶于水中配成250mL溶液,取出25mL溶液,向其中加入过量的NaOH溶液,将沉淀过滤,洗涤,高温灼烧至质量不再改变,称量其固体的质量为0.08g。
步骤b:另取出25mL溶液,加入适量稀H2SO4溶液,用0.050 mol·L-1KMnO4溶液滴定,到达滴定终点时,消耗KMnO4溶液24.00mL。
已知:
(1) 配平上述反应方程式
(2) 草酸为二元弱酸,其一级电离的方程式为
(3)滴定终点观察到的现象为
(4)通过计算确定样品的组成(写出计算过程)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O,已知:HCl是反应物之一。
①写出配平的该反应的化学方程式:______________________
②被氧化的元素是____________ 。
(2)氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它.CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+=Cu2++Cu.
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
①写出CuH在氯气中燃烧的化学反应方程式:___________________________________ .
②如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:__________________________________________________ .
(3) 在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为________________________________________________
①写出配平的该反应的化学方程式:
②被氧化的元素是
(2)氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它.CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+=Cu2++Cu.
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
①写出CuH在氯气中燃烧的化学反应方程式:
②如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:
(3) 在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一,氰酸盐进一步被氧化为无毒物质。
(1)某厂废水中含KCN,其浓度为650mg/L。现用氯氧化法处理,发生如下反应:KCN+2KOH+Cl2=KOCN+2KCl+H2O。投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平下列化学方程式:KOCN+KOH+Cl2—CO2+N2+KCl+H2O,_______ 。
(2)若处理上述废水100L,使KCN完全转化为无毒物质,至少需要投放液氯多少克?_______
(3)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-。试写出:
①(CN)2与KOH溶液反应的化学方程式:_______ 。
②在NaBr和KSCN的混合溶液中滴加少量(CN)2,反应的离子方程_______ 。
(1)某厂废水中含KCN,其浓度为650mg/L。现用氯氧化法处理,发生如下反应:KCN+2KOH+Cl2=KOCN+2KCl+H2O。投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平下列化学方程式:KOCN+KOH+Cl2—CO2+N2+KCl+H2O,
(2)若处理上述废水100L,使KCN完全转化为无毒物质,至少需要投放液氯多少克?
(3)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-。试写出:
①(CN)2与KOH溶液反应的化学方程式:
②在NaBr和KSCN的混合溶液中滴加少量(CN)2,反应的离子方程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】工业废水中过量的氨氮( 和
和 )会导致水体富营养化,其氨氮总量的检测和去除备受关注。
)会导致水体富营养化,其氨氮总量的检测和去除备受关注。
(1)氨氮总量检测
利用氨气传感器检测水体中氨氮含量的示意图:
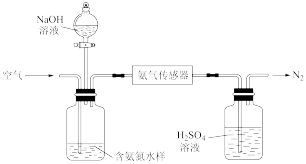
若利用氨气传感器将1L水样中的氨氮完全转化为N2时,转移电子的物质的量为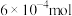 ,则水样中氨氮(以氨气计)含量为
,则水样中氨氮(以氨气计)含量为___________ mg/L。
(2) 氧化法处理氨氮废水
氧化法处理氨氮废水
①写出酸性条件下 氧化
氧化 为氮气的离子反应方程式
为氮气的离子反应方程式___________ 。
②为研究空气对 氧化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是
氧化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是___________ (填字母)。
a. 的氧化性比
的氧化性比 弱 b.
弱 b. 氧化氨氮速率比
氧化氨氮速率比 慢 c.空气中的
慢 c.空气中的 进入溶液中
进入溶液中
(3)传统的生物脱氮机理认为:脱氮过程一般包括氨化[将含氮有机物转化为氨氮( 、
、 )、硝化和反硝化三个过程。
)、硝化和反硝化三个过程。
①硝化过程:废水中的氨氮( 、
、 )在硝化菌(好氧自养型微生物)的作用下被转化为
)在硝化菌(好氧自养型微生物)的作用下被转化为 和
和 的过程。其中硝化过程的主要反应原理有:
的过程。其中硝化过程的主要反应原理有:
反应1
反应2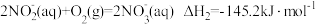
反应3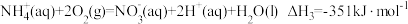
则x=___________ 。
②反硝化过程:若在缺氧环境和反硝化菌的作用下,向某含 的酸性废水中加入适量的甲醇,能实现“反硝化”过程,并产生两种对环境无污染的气体;写出该过程的离子反应方程式:
的酸性废水中加入适量的甲醇,能实现“反硝化”过程,并产生两种对环境无污染的气体;写出该过程的离子反应方程式:___________ 。
(4)新型生物脱氮工艺可将硝化过程中的产物控制在 阶段,防止生成
阶段,防止生成 ,该工艺的优点
,该工艺的优点___________ 。
 和
和 )会导致水体富营养化,其氨氮总量的检测和去除备受关注。
)会导致水体富营养化,其氨氮总量的检测和去除备受关注。(1)氨氮总量检测
利用氨气传感器检测水体中氨氮含量的示意图:

若利用氨气传感器将1L水样中的氨氮完全转化为N2时,转移电子的物质的量为
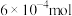 ,则水样中氨氮(以氨气计)含量为
,则水样中氨氮(以氨气计)含量为(2)
 氧化法处理氨氮废水
氧化法处理氨氮废水①写出酸性条件下
 氧化
氧化 为氮气的离子反应方程式
为氮气的离子反应方程式②为研究空气对
 氧化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是
氧化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是a.
 的氧化性比
的氧化性比 弱 b.
弱 b. 氧化氨氮速率比
氧化氨氮速率比 慢 c.空气中的
慢 c.空气中的 进入溶液中
进入溶液中(3)传统的生物脱氮机理认为:脱氮过程一般包括氨化[将含氮有机物转化为氨氮(
 、
、 )、硝化和反硝化三个过程。
)、硝化和反硝化三个过程。①硝化过程:废水中的氨氮(
 、
、 )在硝化菌(好氧自养型微生物)的作用下被转化为
)在硝化菌(好氧自养型微生物)的作用下被转化为 和
和 的过程。其中硝化过程的主要反应原理有:
的过程。其中硝化过程的主要反应原理有:反应1

反应2
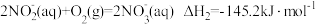
反应3
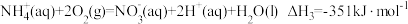
则x=
②反硝化过程:若在缺氧环境和反硝化菌的作用下,向某含
 的酸性废水中加入适量的甲醇,能实现“反硝化”过程,并产生两种对环境无污染的气体;写出该过程的离子反应方程式:
的酸性废水中加入适量的甲醇,能实现“反硝化”过程,并产生两种对环境无污染的气体;写出该过程的离子反应方程式:(4)新型生物脱氮工艺可将硝化过程中的产物控制在
 阶段,防止生成
阶段,防止生成 ,该工艺的优点
,该工艺的优点
您最近一年使用:0次

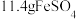 固体,加入足量
固体,加入足量 溶液,使
溶液,使 全部转化成
全部转化成 ,并放出NO气体。
,并放出NO气体。 恰好完全反应时,转移电子的物质的量是
恰好完全反应时,转移电子的物质的量是 ,
,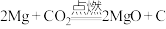 ,
,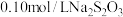 溶液恰好把标准状况下
溶液恰好把标准状况下 完全转化为
完全转化为 ,则
,则 将转化成
将转化成

