铝氢化钠(NaAlH4)是重要的还原剂。以铝土矿(主要成分Al2O3,含少量SiO2、Fe2O3等杂质)为原料制备NaAlH4的一种流程如图:
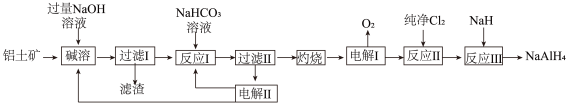
已知:“碱溶”中SiO2转化成难溶的Na2Al2Si2O8
(1)过滤Ⅰ得滤液的主要成分为____ (填化学式)。
(2)过滤Ⅱ得滤液的主要成分为___ (填化学式)。
(3)反应Ⅲ的化学方程式为____ 。
(4)反应Ⅰ的离子方程式为____ 、____ 。
(5)过滤Ⅰ所得滤渣主要成分有Na2Al2Si2O8和Fe2O3,可以采用如图流程进行分离:
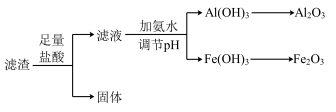
①滤渣溶于盐酸所得的固体物质可能为___ (填化学式)。
②滤渣溶于盐酸的“酸浸率”与温度关系如图所示,试解释温度过高,“酸浸率”降低的原因___ 。
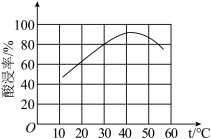

已知:“碱溶”中SiO2转化成难溶的Na2Al2Si2O8
(1)过滤Ⅰ得滤液的主要成分为
(2)过滤Ⅱ得滤液的主要成分为
(3)反应Ⅲ的化学方程式为
(4)反应Ⅰ的离子方程式为
(5)过滤Ⅰ所得滤渣主要成分有Na2Al2Si2O8和Fe2O3,可以采用如图流程进行分离:

①滤渣溶于盐酸所得的固体物质可能为
②滤渣溶于盐酸的“酸浸率”与温度关系如图所示,试解释温度过高,“酸浸率”降低的原因

更新时间:2020-10-16 20:11:33
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】碳、硅及其化合物的开发由来已久,在现代生活中有广泛应用。
(1)SiO2是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是___ (用化学方程式表示)。
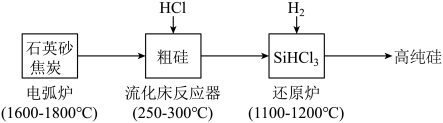
(2)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:
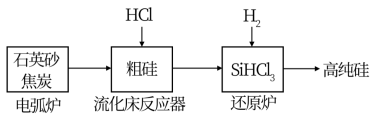
①用石英砂和焦炭在电弧炉中制粗硅,该反应的化学方程式为___ 。
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和___ 。
(3)某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验),实验操作步骤:
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ.A中看到白色沉淀时,关闭弹簧夹1,打开弹簧夹2,关闭活塞a。
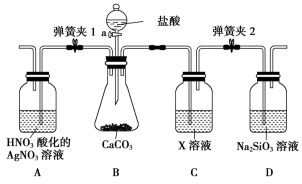
①通过步骤Ⅰ得知盐酸具有的性质是___ (填字母)。
A.挥发性 B.还原性 C.氧化性 D.酸性
②C装置中的试剂X是___ (写化学式)。
③碳、硅的非金属性逐渐减弱的原因:碳和硅___ 。
(1)SiO2是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是
(2)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:

①用石英砂和焦炭在电弧炉中制粗硅,该反应的化学方程式为
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ.A中看到白色沉淀时,关闭弹簧夹1,打开弹簧夹2,关闭活塞a。

①通过步骤Ⅰ得知盐酸具有的性质是
A.挥发性 B.还原性 C.氧化性 D.酸性
②C装置中的试剂X是
③碳、硅的非金属性逐渐减弱的原因:碳和硅
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:___________ 。当有Si+HCl=SiHCl3+H2参与反应时,每产生1 mol H2,该反应转移的电子数是___________ 。
(2)还原炉中发生的化学反应方程式为___________ 。
(3)上述工艺生产中循环使用的物质除Si、SiHCl3外,还有___________ 。
(4)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为___________ 。
(5)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:___________ 。
(6)关于硅及其相关化合物的叙述正确的是___________ (填字母)。
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是+4,由于CO2+H2O=H2CO3,用类比法得知SiO2+H2O=H2SiO3
C.硅元素在金属与非金属的分界线处,因此具有弱导电性,一般可用于作为半导体材料
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.玻璃、水泥、陶瓷都是传统的硅酸盐产品
(2)还原炉中发生的化学反应方程式为
(3)上述工艺生产中循环使用的物质除Si、SiHCl3外,还有
(4)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
(5)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:
(6)关于硅及其相关化合物的叙述正确的是
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是+4,由于CO2+H2O=H2CO3,用类比法得知SiO2+H2O=H2SiO3
C.硅元素在金属与非金属的分界线处,因此具有弱导电性,一般可用于作为半导体材料
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.玻璃、水泥、陶瓷都是传统的硅酸盐产品
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】Ⅰ. 和石英砂(
和石英砂( )在工业上用途广泛,为探究它们的性质,设计如图装置进行实验(省略尾气处理装置)。
)在工业上用途广泛,为探究它们的性质,设计如图装置进行实验(省略尾气处理装置)。_______ 。
(2)若要实现硫元素由 价转化为0价,需在C中加入
价转化为0价,需在C中加入_______ 溶液,可观察到淡黄色沉淀产生。此过程体现了 的
的_______ 性。
Ⅱ.“中国芯”的发展离不开高纯单晶硅。从石英砂(主要成分为 )制取高纯硅涉及的主要反应用流程图表示如图:
)制取高纯硅涉及的主要反应用流程图表示如图:
Ⅲ.习主席在2020年新年贺词中强调“5G商用加速推出,凝结着新时代奋斗者的心血和汗水,彰显了不同凡响的中国风采、中国力量”,制造芯片用到高纯硅,上述反应③的模拟装置如图所示(热源及夹持装置略去)。已知: 遇水
遇水 强烈水解,沸点较低,在空气中易自燃。
强烈水解,沸点较低,在空气中易自燃。_______ ;
(5)装置C中的烧瓶需要加热,其目的是_______ ;
(6)用 和NaOH固体焙烧制备硅酸钠,可采用图中的装置_______(填选项编号)。
和NaOH固体焙烧制备硅酸钠,可采用图中的装置_______(填选项编号)。
 和石英砂(
和石英砂( )在工业上用途广泛,为探究它们的性质,设计如图装置进行实验(省略尾气处理装置)。
)在工业上用途广泛,为探究它们的性质,设计如图装置进行实验(省略尾气处理装置)。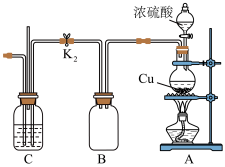
(2)若要实现硫元素由
 价转化为0价,需在C中加入
价转化为0价,需在C中加入 的
的Ⅱ.“中国芯”的发展离不开高纯单晶硅。从石英砂(主要成分为
 )制取高纯硅涉及的主要反应用流程图表示如图:
)制取高纯硅涉及的主要反应用流程图表示如图:
| A.反应①中Si是氧化产物 | B.流程中HCl和 可以循环利用 可以循环利用 |
| C.反应①②③均为氧化还原反应 | D. 是两性氧化物 是两性氧化物 |
Ⅲ.习主席在2020年新年贺词中强调“5G商用加速推出,凝结着新时代奋斗者的心血和汗水,彰显了不同凡响的中国风采、中国力量”,制造芯片用到高纯硅,上述反应③的模拟装置如图所示(热源及夹持装置略去)。已知:
 遇水
遇水 强烈水解,沸点较低,在空气中易自燃。
强烈水解,沸点较低,在空气中易自燃。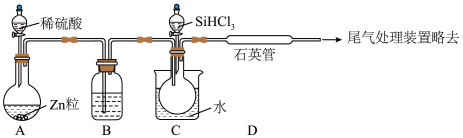
(5)装置C中的烧瓶需要加热,其目的是
(6)用
 和NaOH固体焙烧制备硅酸钠,可采用图中的装置_______(填选项编号)。
和NaOH固体焙烧制备硅酸钠,可采用图中的装置_______(填选项编号)。A. | B. | C. | D. |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E五种化合物,均含有前18号元素中某种常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。

(1)写出化学式:A________ ,B________ ,C________ ,D________ 。
(2)写出下列反应的离子方程式:
B→D___________________ ,C→E_______________________ 。

(1)写出化学式:A
(2)写出下列反应的离子方程式:
B→D
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图所示转化关系中涉及到的物质均由主族元素组成(部分产物已略去),其中C、D为单质,A、B、E、F、G为化合物,除C与D的反应外,其它反应均在溶液中进行。请填写下列空白。
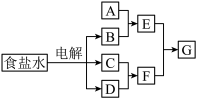
(1) 若A是常见的金属或金属氧化物,当F过量时,G为可溶性盐,则A的化学式为_________ 或_________ 。
(2) 若A是一种常见氧化物,不管F过量与否,G为同一种难溶性物质,则A的名称是________ ,晶体类型是_______ ,A的用途是_________ 。
(3) 若A是一种具有漂白性的气态氧化物,A是___ ;若A是一种无味的气态氧化物,A的电子式为______ 。
(4) 若A为有机化合物,如果A与G为同一物质,请写出两种A(不同类别物质)的结构简式:_____ ;_____ 。

(1) 若A是常见的金属或金属氧化物,当F过量时,G为可溶性盐,则A的化学式为
(2) 若A是一种常见氧化物,不管F过量与否,G为同一种难溶性物质,则A的名称是
(3) 若A是一种具有漂白性的气态氧化物,A是
(4) 若A为有机化合物,如果A与G为同一物质,请写出两种A(不同类别物质)的结构简式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】NH4Al(SO4)2·12H2O(铵明矾)可用作泡沫灭火器的内留剂、石油脱色剂等。某兴趣小组同学用氧化铁、铝粉、镁条和氯酸钾等物质做铝热反应后的铝灰及硫酸铵等为原料制备铵明矾的实验,步骤如下:

(1)下列有关说法中正确的是_________ 。
A.“滤液1”中含有K+、Mg2+、Cl-
B.“滤渣1”和“滤渣2”中含有相同的物质
C.“过滤1”可用倾析法,以缩减实验时间
D.将“滤液3”蒸干并灼烧,可得纯碱
(2)用NaOH溶解“滤渣1”时,可以采用_________ 的方式提高浸出率(写出3条)。
(3)向“滤液2”中通入足量的CO2,写出相应的离子反应方程式__________________ 。
(4)由“滤渣3”制备铵明矾,经过如下步骤:a→g→_________ →h(依次填入正确的序号)
a.加硫酸溶解 b.抽滤
c.加入蒸发皿中
d.降温结晶
e.蒸发至表面出现晶膜
f.配制饱和硫酸铵溶液
g.将硫酸铝溶液转移至蒸发皿
h.洗涤、干燥
(5)①根据各物质的溶解度曲线(见下图),在80℃时,用一定浓度的硫酸溶解“滤渣3”时,最适宜的硫酸浓度为_________ 。

A.3mol/L(1.20g/mL)
B.6mol/L(1.34g/mL)
C.9mol/L(1.49 g/mL)
D.18mol/L (1.84g/mL)
②所需硫酸用量的简便确定方法是__________________ 。

(1)下列有关说法中正确的是
A.“滤液1”中含有K+、Mg2+、Cl-
B.“滤渣1”和“滤渣2”中含有相同的物质
C.“过滤1”可用倾析法,以缩减实验时间
D.将“滤液3”蒸干并灼烧,可得纯碱
(2)用NaOH溶解“滤渣1”时,可以采用
(3)向“滤液2”中通入足量的CO2,写出相应的离子反应方程式
(4)由“滤渣3”制备铵明矾,经过如下步骤:a→g→
a.加硫酸溶解 b.抽滤
c.加入蒸发皿中
d.降温结晶
e.蒸发至表面出现晶膜
f.配制饱和硫酸铵溶液
g.将硫酸铝溶液转移至蒸发皿
h.洗涤、干燥
(5)①根据各物质的溶解度曲线(见下图),在80℃时,用一定浓度的硫酸溶解“滤渣3”时,最适宜的硫酸浓度为

A.3mol/L(1.20g/mL)
B.6mol/L(1.34g/mL)
C.9mol/L(1.49 g/mL)
D.18mol/L (1.84g/mL)
②所需硫酸用量的简便确定方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铝土矿是工业上制备金属铝的主要原料,其主要成分是 ,同时还含有
,同时还含有 、
、 。工业上可使用碱浸法提取铝土矿中的
。工业上可使用碱浸法提取铝土矿中的 ,其工业流程如图所示。根据图示信息,请回答下列问题。(提示:
,其工业流程如图所示。根据图示信息,请回答下列问题。(提示: 不与稀盐酸反应)
不与稀盐酸反应)
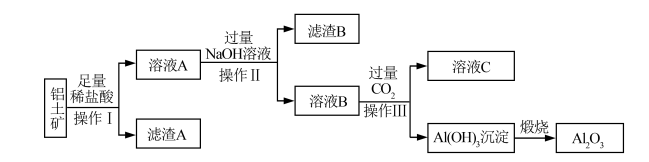
(1)操作I的名称是_______ ,写出溶液A中加入过量NaOH溶液生成溶液B的离子方程式_______ ,滤渣B的主要成分是_______ (填化学式)。
(2)写出溶液B中通入过量 产生沉淀的离子方程式是
产生沉淀的离子方程式是_______ ,该步骤中_______ (填“能”或“不能”)改用盐酸代替通入 ,原因是
,原因是_______ 。
(3)实验室中进行煅烧时最适合用来盛放 固体的实验仪器名称是
固体的实验仪器名称是_______ 。
(4)用 与C、
与C、 在高温条件下反应可制取
在高温条件下反应可制取 ,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是
,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是_______ 。
(5)工业上通过电解熔融氧化铝制备金属铝时,常用石墨作电极,但其在电解过程中易损耗需要定期更换,原因是_______ 。
 ,同时还含有
,同时还含有 、
、 。工业上可使用碱浸法提取铝土矿中的
。工业上可使用碱浸法提取铝土矿中的 ,其工业流程如图所示。根据图示信息,请回答下列问题。(提示:
,其工业流程如图所示。根据图示信息,请回答下列问题。(提示: 不与稀盐酸反应)
不与稀盐酸反应)
(1)操作I的名称是
(2)写出溶液B中通入过量
 产生沉淀的离子方程式是
产生沉淀的离子方程式是 ,原因是
,原因是(3)实验室中进行煅烧时最适合用来盛放
 固体的实验仪器名称是
固体的实验仪器名称是(4)用
 与C、
与C、 在高温条件下反应可制取
在高温条件下反应可制取 ,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是
,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是(5)工业上通过电解熔融氧化铝制备金属铝时,常用石墨作电极,但其在电解过程中易损耗需要定期更换,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】铝是一种应用广泛的金属,工业上用 和冰晶石(
和冰晶石( )混合熔融电解制得。
)混合熔融电解制得。
①铝土矿的主要成分是 和
和 等。从铝土矿中提炼
等。从铝土矿中提炼 的流程如下:
的流程如下:
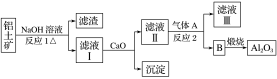
②以萤石( )和纯碱为原料制备冰晶石的流程如下:
)和纯碱为原料制备冰晶石的流程如下:
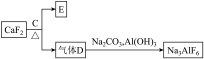
请回答下列问题:
(1)写出反应1的化学方程式____________ 。
(2)滤液1中加入 生成的沉淀是
生成的沉淀是____________ ,反应2的离子方程式为____________ (气体 过量)。
过量)。
(3) 可作为建筑材料,化合物
可作为建筑材料,化合物 是浓硫酸,请写出由
是浓硫酸,请写出由 制备冰晶石的化学方程式
制备冰晶石的化学方程式____________ 。
(4)电解氧化铝制铝时,以石墨为电极,请写出阳极的电极反应式____________ 。
 和冰晶石(
和冰晶石( )混合熔融电解制得。
)混合熔融电解制得。①铝土矿的主要成分是
 和
和 等。从铝土矿中提炼
等。从铝土矿中提炼 的流程如下:
的流程如下:
②以萤石(
 )和纯碱为原料制备冰晶石的流程如下:
)和纯碱为原料制备冰晶石的流程如下:
请回答下列问题:
(1)写出反应1的化学方程式
(2)滤液1中加入
 生成的沉淀是
生成的沉淀是 过量)。
过量)。(3)
 可作为建筑材料,化合物
可作为建筑材料,化合物 是浓硫酸,请写出由
是浓硫酸,请写出由 制备冰晶石的化学方程式
制备冰晶石的化学方程式(4)电解氧化铝制铝时,以石墨为电极,请写出阳极的电极反应式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】富铁铝土矿(主要含有A12O3、Fe2O3、FeO和SiO2)可制备新型净水剂液体聚合硫酸铝铁[AlaFeb(OH)m(SO4)n]。研究发现,当a=b时净水效果最好。工艺流程如下(部分操作和产物略):
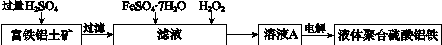
(1)A12O3与H2SO4发生反应的离子方程式是____________ 。
(2)测得滤液中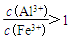 。加入FeSO4·7H2O和H2O2的作用是(结合化学用语说明)
。加入FeSO4·7H2O和H2O2的作用是(结合化学用语说明)____________ 。
(3)将溶液A电解得到液体聚合硫酸铝铁。装置如图所示(阴离子交换膜只允许阴离子通过,电极为惰性电极)
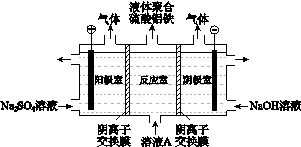
① 阴极室的电极反应式是__________ 。
② 电解过程阳极室溶液pH的变化是____________ (填“增大”、“减小”或“不变”)。
③ 简述在反应室中生成液体聚合硫酸铝铁的原理____________ 。

(1)A12O3与H2SO4发生反应的离子方程式是
(2)测得滤液中
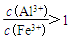 。加入FeSO4·7H2O和H2O2的作用是(结合化学用语说明)
。加入FeSO4·7H2O和H2O2的作用是(结合化学用语说明)(3)将溶液A电解得到液体聚合硫酸铝铁。装置如图所示(阴离子交换膜只允许阴离子通过,电极为惰性电极)

① 阴极室的电极反应式是
② 电解过程阳极室溶液pH的变化是
③ 简述在反应室中生成液体聚合硫酸铝铁的原理
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:

(1)灼烧海带时需要用到的实验仪器是_____ (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.蒸发皿 C.表面皿 D.铁架台(带铁圈) E.酒精灯 F.干燥器
(2)指出提取碘的过程中有关的实验操作名称:①___________ ,③___________ 。
(3)过程②中充入适量Cl2的目的是________________________________ ,反应的离子方程式为_________________________________ 。
(4)操作③中所用的有机试剂可以是_____________________ (只填一种)。
(5)操作过程③可以分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50 mL碘水和15 mL有机溶剂(你所选的)加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
①上述G步操作的目的是_________________________________ ;
②最后碘的有机溶液是通过___________ 获得(填“漏斗上口”或“漏斗下口”)。
(6)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:___________________ 。
(7)从含碘的有机溶液中提取碘和回收有机溶液,还需要经过蒸馏,观察下图所示实验装置,指出其错误之处并加以改正:_________________________________ 。
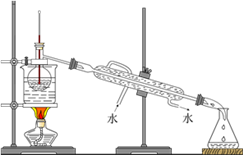
(8)进行上述蒸馏操作时,使用水浴的原因是________________ ,最后晶态碘在__________ 里聚集。

(1)灼烧海带时需要用到的实验仪器是
A.烧杯 B.蒸发皿 C.表面皿 D.铁架台(带铁圈) E.酒精灯 F.干燥器
(2)指出提取碘的过程中有关的实验操作名称:①
(3)过程②中充入适量Cl2的目的是
(4)操作③中所用的有机试剂可以是
(5)操作过程③可以分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50 mL碘水和15 mL有机溶剂(你所选的)加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
①上述G步操作的目的是
②最后碘的有机溶液是通过
(6)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
(7)从含碘的有机溶液中提取碘和回收有机溶液,还需要经过蒸馏,观察下图所示实验装置,指出其错误之处并加以改正:

(8)进行上述蒸馏操作时,使用水浴的原因是
您最近一年使用:0次
【推荐2】工业上从电解精炼铜的阳极泥(含金、银、铜、硒等单质)中提取硒的湿法工艺流程如下:
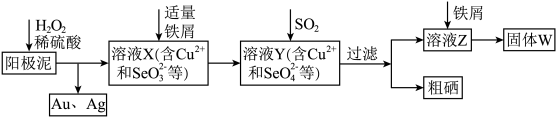
(1)向溶液X中加入铁屑的作用是______ ,此操作中不能加入过量铁粉的原因是______ 。
(2)检验溶液Z中阴离子的操作方法是______ 。
(3)过滤操作中要用到玻璃棒,请另举两例用到玻璃棒的实验或操作:______ 。
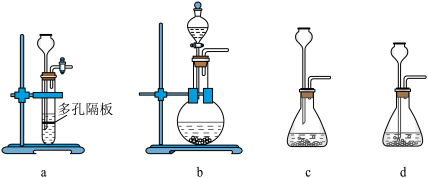
(4)实验室中制取SO2的原理为:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑,此处应使用______ (填“较浓的硫酸”或“稀硫酸”),原因是 ______ 。制取SO2的装置,最好选用下图中的______ 。
(5)粗硒中硒的含量可用如下方法测定:
①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O
②SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O
③I2+2Na2S2O3=Na2S4O6+2NaI
通过用Na2S2O3标准溶液(显碱性)滴定反应②中生成的I2来计算硒的含量。滴定操作中用到的玻璃仪器有_______ 。实验中准确称量0.1200g粗硒样品,滴定中消耗0.2000mol/L的Na2S2O3溶液27.60mL,则粗硒样品中硒的质量分数为_______ 。

(1)向溶液X中加入铁屑的作用是
(2)检验溶液Z中阴离子的操作方法是
(3)过滤操作中要用到玻璃棒,请另举两例用到玻璃棒的实验或操作:
(4)实验室中制取SO2的原理为:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑,此处应使用

(5)粗硒中硒的含量可用如下方法测定:
①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O
②SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O
③I2+2Na2S2O3=Na2S4O6+2NaI
通过用Na2S2O3标准溶液(显碱性)滴定反应②中生成的I2来计算硒的含量。滴定操作中用到的玻璃仪器有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】镀镍生产过程中产生的酸性硫酸镍废液(含有Fe2+、Zn2+、Mg2+、Ca2+等杂质离子),通过精制提纯可制备高纯硫酸镍,部分流程如图:

资料1:25℃时,生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol/L
资料2:25℃时,Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9,ZnF2易溶于水。
资料3:P204(二乙基己基磷酸)萃取金属离子的反应为:x[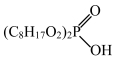 ]+Mx+
]+Mx+ [
[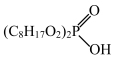 ]xM+xH+
]xM+xH+
(1)操作1、2的名称是____ ,操作3的名称是____ 。
(2)操作1中加入Cl2的主要目的是____ 。
(3)NiF2溶液参与反应的离子方程式是Mg2++2F-=MgF2和____ 。杂质离子沉淀完全时,溶液中c(F-)=____ mol/L(c(杂质离子)<10-5mol/L即可视为沉淀完全)。
(4)滤液b中含有的微粒主要有____ 。
(5)在硫酸盐溶液中P204对某些金属离子的萃取率与pH关系如图所示,在一定范围内,随着pH升高,萃取率升高的原因是____ 。

(6)在母液中加入其它物质,可制备操作1中所需Ni(OH)2浆液,写出制备的化学方程式____ 。

资料1:25℃时,生成氢氧化物沉淀的pH
| Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Mg(OH)2 | Ca(OH)2 | Ni(OH)2 | |
| 开始沉淀时 | 6.3 | 1.5 | 6.2 | 9.1 | 11.8 | 6.9 |
| 完全沉淀时 | 8.3 | 2.8 | 8.2 | 11.1 | 13.8 | 8.9 |
资料2:25℃时,Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9,ZnF2易溶于水。
资料3:P204(二乙基己基磷酸)萃取金属离子的反应为:x[
 ]+Mx+
]+Mx+ [
[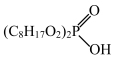 ]xM+xH+
]xM+xH+(1)操作1、2的名称是
(2)操作1中加入Cl2的主要目的是
(3)NiF2溶液参与反应的离子方程式是Mg2++2F-=MgF2和
(4)滤液b中含有的微粒主要有
(5)在硫酸盐溶液中P204对某些金属离子的萃取率与pH关系如图所示,在一定范围内,随着pH升高,萃取率升高的原因是

(6)在母液中加入其它物质,可制备操作1中所需Ni(OH)2浆液,写出制备的化学方程式
您最近一年使用:0次



