下列关于两个反应的△H的判断,正确的是
S(s)+O2(g)=SO2(g) △H1;2S(s)+3O2(g)=2SO3(g) △H2
S(s)+O2(g)=SO2(g) △H1;2S(s)+3O2(g)=2SO3(g) △H2
| A.△H1>0,△H2>0 | B.2△H1>△H2 |
| C.△H1<0,△H2>0 | D.△H2>△H1 |
更新时间:2020-10-24 09:01:31
|
相似题推荐
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】已知: ,
,
 ,
,
 ,
,
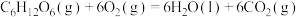 ,
,
下列说法错误的是
 ,
,
 ,
,
 ,
,
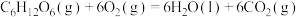 ,
,
下列说法错误的是
A. , , | B.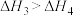 |
C.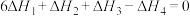 | D. |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】已知:298K时,相关物质的相对能量如下表所示:
下列说法不正确的是
| 物质 |  |  |  |  |  |  |  |
| 相对能量/(kJ/mol) | 0 | 0 | 0 | -110 | -393 | -242 | -286 |
A.1  完全燃烧生成 完全燃烧生成 放出的热量为286 放出的热量为286 |
B. 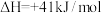 |
C.已知  , ,  ,则 ,则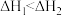 |
| D.将碳先与水蒸气作用转化成水煤气再燃烧,与直接燃烧等质量的碳,反应后都恢复至室温,两个过程的热效应是一样的 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐3】环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。
已知: (g)=
(g)= (g)+H2(g) ΔH1= +100.3 kJ·mol-1 ①
(g)+H2(g) ΔH1= +100.3 kJ·mol-1 ①
 (g)+I2(g)=
(g)+I2(g)= (g)+2HI(g) ΔH2= +89.3 kJ·mol-1 ②
(g)+2HI(g) ΔH2= +89.3 kJ·mol-1 ②
则氢气和碘蒸气反应生成碘化氢气体的热化学方程式为
 )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。已知:
 (g)=
(g)= (g)+H2(g) ΔH1= +100.3 kJ·mol-1 ①
(g)+H2(g) ΔH1= +100.3 kJ·mol-1 ① (g)+I2(g)=
(g)+I2(g)= (g)+2HI(g) ΔH2= +89.3 kJ·mol-1 ②
(g)+2HI(g) ΔH2= +89.3 kJ·mol-1 ②则氢气和碘蒸气反应生成碘化氢气体的热化学方程式为
| A.H2(g)+I2(s)=2HI(g) ΔH= -11.0 kJ·mol-1 |
| B.H2(g)+I2(g)=2HI(g) ΔH= -11.0 kJ·mol-1 |
| C.H2+I2=2HI ΔH= -11.0 kJ·mol-1 |
| D.H2(g)+I2(g)=2HI(g) ΔH= +11.0 kJ·mol-1 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】已知下列热化学方程式:
①C(s)+O2(g)==CO2(g)△H= —393.5kJ/mol
②CO(g)+ 1/2 O2(g)== CO2(g)△H= —283.0kJ/mol
③2Fe(s)+3CO(g)==Fe2O3(s)+3C(s) △H= —489.0kJ/mol
则4Fe(s)+3O2(g)==2Fe2O3(s)的反应热ΔH为
①C(s)+O2(g)==CO2(g)△H= —393.5kJ/mol
②CO(g)+ 1/2 O2(g)== CO2(g)△H= —283.0kJ/mol
③2Fe(s)+3CO(g)==Fe2O3(s)+3C(s) △H= —489.0kJ/mol
则4Fe(s)+3O2(g)==2Fe2O3(s)的反应热ΔH为
| A.-1641.0kJ/mol | B.+3081kJ/mol |
| C.+663.5kJ/mol | D.-2507.0kJ/mol |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】已知:弱碱MOH(aq)与H2SO4(aq)反应生成1mol正盐的△H=-24.2kJ/mol,强酸与强碱的稀溶液的中和热为△H=-57.3kJ/mol。则MOH在水溶液中电离的△H为
| A.+45.2kJ/mol | B.+69.4kJ/mol | C.-69.4kJ/mol | D.-45.2kJ/mol |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐3】煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaSO4(s)+4CO(g) CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
下列有关说法正确的是
CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)CaSO4(s)+4CO(g)
 CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)下列有关说法正确的是
| A.反应I在较低的温度下可自发进行 |
| B.反应II在较低的温度下可自发进行 |
C.用生石灰固硫的反应为:4CaO(s)+4SO2(g)  3CaSO4(s)+CaS(s) △H3,则△H3>△H2 3CaSO4(s)+CaS(s) △H3,则△H3>△H2 |
D.由反应I和反应II可计算出反应CaSO4(s)  CaO(s)+SO3(g)的焓变 CaO(s)+SO3(g)的焓变 |
您最近一年使用:0次



