下列说法不正确的是
| A.测得 0.1 mol·L−1 的一元酸 HA 溶液 pH=3.0,则 HA 一定为弱电解质 |
| B.25℃时,将 0.1 mol·L−1 的NaOH 溶液加水稀释 100 倍,所得溶液的 pH=11.0 |
| C.25℃时,将 0.1 mol·L−1 的 HA 溶液加水稀释至 pH=4.0,所得溶液 c(OH-)=1×10−10 mol·L−1 |
| D.pH=2.0 的HA 溶液与 0.01 mol·L−1 的 NaOH 溶液等体积反应,能恰好中和 |
更新时间:2020/10/31 15:46:26
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】常温下,为证明NH3•H2O是弱电解质。下列方法不正确的是
| A.测定0.01mol•L-1氨水的pH |
| B.测定0.01mol•L-1NH4Cl溶液的酸碱性 |
| C.测定pH为10的氨水稀释十倍后的pH |
| D.比较0.01mol•L-1的氨水和1mol•L-1NaOH溶液的导电能力 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列溶液一定呈中性的是
A.等物质的量的HCl、 、 、 混合后的溶液 混合后的溶液 |
B. 盐酸和 盐酸和 的氢氧化钡溶液等体积混合得到的溶液 的氢氧化钡溶液等体积混合得到的溶液 |
C.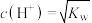 的溶液 的溶液 |
| D.部分非电解质溶于水得到的溶液 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】常温下,二氯乙酸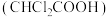 的电离常数为
的电离常数为 ,
, 。下列说法错误的是
。下列说法错误的是
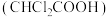 的电离常数为
的电离常数为 ,
, 。下列说法错误的是
。下列说法错误的是A.同浓度乙酸溶液的pH大于二氯乙酸溶液,则 的 的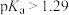 |
B.随温度升高 溶液的pH会减小,(在该温度范围内, 溶液的pH会减小,(在该温度范围内, 始终不逸出) 始终不逸出) |
C.加水稀释二氯乙酸溶液,溶液中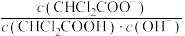 逐渐增大 逐渐增大 |
| D.二氟乙酸的酸性比二氯乙酸强的原因是氟的电负性比氯大 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】关于化学平衡常数、电离平衡常数、水的离子积常数和溶解平衡常数,下列说法正确的是
| A.化学平衡常数反映了在一定温度下可逆反应可能进行的限度 |
| B.四种平衡常数都是温度的函数,温度升高其数值都增大 |
| C.一个可逆反应的化学平衡常数和参与反应的每种物质的化学计量数都有关系 |
| D.纯水中加入强酸或强碱,水的离子积常数都会减小 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐3】常温下,在一定浓度的草酸溶液中滴加一定浓度的NaOH溶液,混合溶液中 和
和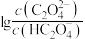 与溶液pH的关系如图所示。
与溶液pH的关系如图所示。
 和
和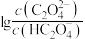 与溶液pH的关系如图所示。
与溶液pH的关系如图所示。
A.直线甲代表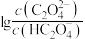 与溶液pH的关系 与溶液pH的关系 |
B.草酸的电离常数之比: |
C.d点溶液中: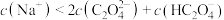 |
| D.若滴加NaOH的物质的量等于开始时草酸的物质的量,所得溶液显碱性 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列酸溶液的pH相同时,其物质的量浓度最小的是
| A.H2SO3 | B.H2SO4 | C.CH3COOH | D.HNO3 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】pH=1的两种酸溶液A、B各1mL,分别加水稀释至1000mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是
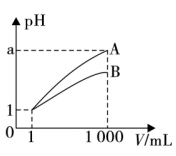

| A.稀释后,A溶液中c(H+)比B溶液中c(H+)大 |
| B.A、B两种酸溶液的物质的量浓度一定相等 |
| C.若a<4,则A、B都是弱酸 |
| D.若a=4,则A、B都是强酸 |
您最近半年使用:0次

 ,则100℃下
,则100℃下 的
的 溶液pH为13
溶液pH为13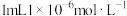 的稀盐酸稀释至1000mL,所得溶液的pH为9
的稀盐酸稀释至1000mL,所得溶液的pH为9 为
为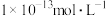 时,此溶液的pH可能为1或13
时,此溶液的pH可能为1或13 的盐酸与
的盐酸与

