按要求写出化学方程式或离子方程式
(1)碳酸氢钠溶液与氢氧化钠溶液反应的离子方程式_________ 。
(2)氢氧化钙溶液与过量碳酸氢钠溶液反应的离子方程式_______ 。
(3)钠与硫酸铜溶液反应的化学方程式____________ 。
(4)制漂白粉的原理的化学方程式____________ 。
(1)碳酸氢钠溶液与氢氧化钠溶液反应的离子方程式
(2)氢氧化钙溶液与过量碳酸氢钠溶液反应的离子方程式
(3)钠与硫酸铜溶液反应的化学方程式
(4)制漂白粉的原理的化学方程式
更新时间:2020-11-03 06:05:26
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】小明在家里阅读84消毒液的说明书时发现有以下信息(见图1):
(1)消毒液不能与洁厕灵(主要成分是盐酸)混用,是因为___ (用离子方程式表示)
(2)请用离子方程式表示消毒液要密封保存的原因__ (已知产物之一为酸式盐),遮光是为了防止__ 分解。
(3)小明利用所学知识,拟用图2装置自制家用消毒液,试写出有关化学方程式:①__ 、②__ 。

 说明书 | 药品名称 | 84消毒液 |
| 主要成分 |  ,有效氯含量50.0 g/L~60.0 g/L ,有效氯含量50.0 g/L~60.0 g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷 白色衣物,浴缸等  水溶液 水溶液餐饮具,瓜果等  水溶液 水溶液 |
图1
(1)消毒液不能与洁厕灵(主要成分是盐酸)混用,是因为
(2)请用离子方程式表示消毒液要密封保存的原因
(3)小明利用所学知识,拟用图2装置自制家用消毒液,试写出有关化学方程式:①

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)配平下列离子方程式:______
Ce3++ H2O2+ H2O === Ce(OH)4↓+_______H+
(2)已知某待测液由Ag+、Mg2+、K+、Ba2+、NH4+、NO3-中的若干种离子组成,进行如下实验:
第一步:加入过量的稀盐酸,有白色沉淀生成。
第二步:过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
第三步:再过滤,取少量滤液,逐渐滴入NaOH溶液至溶液呈碱性,在此过程中没有沉淀和气体产生,加热该溶液,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:
①写出第三步加热该溶液后,有气体生成的反应的离子方程式:_________________ ;
②待测液中一定含有_______ 和NO3-离子,一定不含有_________ 离子,还有一种离子不能确定其是否存在,要检验这种离子的实验方法是(填写实验名称)___________ 。
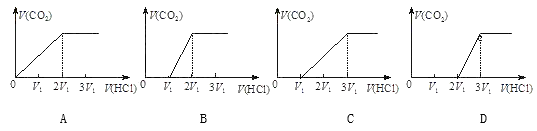
③往含等物质的量CO32-和HCO3-的溶液中滴入HCl溶液,下列表示产生的气体在标准状况下的体积与加入的HCl溶液体积关系图正确的是_________ 。
Ce3++ H2O2+ H2O === Ce(OH)4↓+_______H+
(2)已知某待测液由Ag+、Mg2+、K+、Ba2+、NH4+、NO3-中的若干种离子组成,进行如下实验:
第一步:加入过量的稀盐酸,有白色沉淀生成。
第二步:过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
第三步:再过滤,取少量滤液,逐渐滴入NaOH溶液至溶液呈碱性,在此过程中没有沉淀和气体产生,加热该溶液,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:
①写出第三步加热该溶液后,有气体生成的反应的离子方程式:
②待测液中一定含有
③往含等物质的量CO32-和HCO3-的溶液中滴入HCl溶液,下列表示产生的气体在标准状况下的体积与加入的HCl溶液体积关系图正确的是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知,常温下几种物质的电离常数如下:
(1)(NH4)2CO3溶液的pH_______ (填“大于”或“小于”)7
(2)物质的量浓度均为0.1mol·L-1的4种溶液:① 、②
、② 、③
、③ 、④
、④ ,按要求从大到小排序。
,按要求从大到小排序。 :
:_______ ; :
:_______ 。(用序号填空)
①少量 通入到过量的
通入到过量的 溶液中:
溶液中:_______ 。
②少量 通入到过量的NaClO溶液中:
通入到过量的NaClO溶液中:_______ 。
(3)25℃时,若氨水的浓度为2.0mol·L-1,溶液中的c(OH−)=_______ mol·L−1。将SO2通入该氨水中,当c(OH−)降至1.0×10−7mol·L−1时,溶液中的 =
=_______ 。SO2可用足量小苏打溶液吸收,反应的离子方程式是_______ 。
| 化学式 | H2CO3 | CH3COOH | NH3·H2O | H2SO3 | HClO |
| 电离平衡常数 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=1.8×10-5 | Kb=1.8×10-5 | Ka1=1.4×10-2 Ka2=6.0×10-8 | 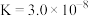 |
(2)物质的量浓度均为0.1mol·L-1的4种溶液:①
 、②
、② 、③
、③ 、④
、④ ,按要求从大到小排序。
,按要求从大到小排序。 :
: :
:①少量
 通入到过量的
通入到过量的 溶液中:
溶液中:②少量
 通入到过量的NaClO溶液中:
通入到过量的NaClO溶液中:(3)25℃时,若氨水的浓度为2.0mol·L-1,溶液中的c(OH−)=
 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Cl2、SO2、CO2均是中学化学常见的气体,减少Cl2、SO2的排放可以防止污染空气,减少CO2的排放,有利于保护环境,实现碳中和。回答下列问题:
(1)化工厂可用浓氨水来检验Cl2是否泄漏,当有少量Cl2泄漏时,可以观察到的现象是________ 。
(2)用热烧碱溶液吸收Cl2反应后的混合溶液,若含NaCl、NaClO和NaClO3物质的量比值为n∶1∶2,则n=________ 。
(3)常温下,可用NaOH溶液作CO2的捕捉剂。若经测定某次捕捉所得溶液中,Na和C两种元素物质的量比值为3:1,则所得溶液中溶质成分为________ (填化学式)。
(4)①除品红外,鉴别SO2、CO2两种气体还可以采用________ (填试剂名称),SO2、Cl2均有漂白性,若将两者1∶1通入品红溶液中,不能使品红褪色,理由是________ (写离子方程式),除去SO2中的HCl可采用________ (填试剂名称)。
②用硫酸酸化的K2Cr2O7溶液处理SO2气体,会析出铬钾矾[KCr(SO4)2·12H2O]晶体。写出该反应的化学方程式:________ 。
(1)化工厂可用浓氨水来检验Cl2是否泄漏,当有少量Cl2泄漏时,可以观察到的现象是
(2)用热烧碱溶液吸收Cl2反应后的混合溶液,若含NaCl、NaClO和NaClO3物质的量比值为n∶1∶2,则n=
(3)常温下,可用NaOH溶液作CO2的捕捉剂。若经测定某次捕捉所得溶液中,Na和C两种元素物质的量比值为3:1,则所得溶液中溶质成分为
(4)①除品红外,鉴别SO2、CO2两种气体还可以采用
②用硫酸酸化的K2Cr2O7溶液处理SO2气体,会析出铬钾矾[KCr(SO4)2·12H2O]晶体。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、农药的生产、药物的合成等领域都有着重要的应用。
(1)Ca(ClO)2中Cl的化合价为___________ ,Ca(ClO)2具有较强的_________ (填“氧化”或“还原”)性,是常用的漂白粉的有效成分。
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为 ,该反应的离子方程式为:
,该反应的离子方程式为:___________ 。
②NaClO可将酸性废水中的Fe2+氧化为Fe3+,本身被还原为NaCl,该反应过程中氧化剂与还原剂的物质的量之比为___________ 。
Ⅱ.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应为放热反应),回答下列问题(消石灰为氢氧化钙):
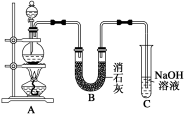
(3)在A装置中用固体二氧化锰与浓盐酸在加热条件下反应制取氯气,写出该反应的化学方程式:___ 。
(4)C装置的作用是(用离子方程式表示)_____________ 。
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是将U型管置于________ 中(填“冰水浴还是热水浴”)。
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,装置的改进措施为______ 。
(1)Ca(ClO)2中Cl的化合价为
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为
 ,该反应的离子方程式为:
,该反应的离子方程式为:②NaClO可将酸性废水中的Fe2+氧化为Fe3+,本身被还原为NaCl,该反应过程中氧化剂与还原剂的物质的量之比为
Ⅱ.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应为放热反应),回答下列问题(消石灰为氢氧化钙):

(3)在A装置中用固体二氧化锰与浓盐酸在加热条件下反应制取氯气,写出该反应的化学方程式:
(4)C装置的作用是(用离子方程式表示)
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是将U型管置于
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,装置的改进措施为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】次氯酸钠(NaClO)是漂白液的主要成分,次氯酸钠溶液可用于消毒、杀菌及水处理。一种生产次氯酸钠的工艺如图所示。
-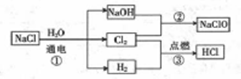
(1)Cl 元素位于元素周期表第______ 周期___ 族。
(2)写出NaOH的电子式:__________ 。
(3)写出反应②的化学方程式:_______________ 。该反应中每生成1mol NaClO时,转移______ mol 电子。
(4)“84”消毒液( 主要成分为NaClO)和洁厕灵( 主要成分为浓盐酸)不能混在一起使用,原因是_____________________ (用离子方程式表示)。
-

(1)Cl 元素位于元素周期表第
(2)写出NaOH的电子式:
(3)写出反应②的化学方程式:
(4)“84”消毒液( 主要成分为NaClO)和洁厕灵( 主要成分为浓盐酸)不能混在一起使用,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】钠具有很活泼的化学性质,易与很多物质反应。钠与水的反应(水中滴有酚酞溶液)实验现象和结论如下表,请同学们完成填空。
(5)钠与水反应方程式是__________________ 。实验室中金属钠通常保存在_______ 。
(6)实验室常用氢氧化钠溶液来吸收多余的氯气以防止污染空气,请写出发生反应的方程式_______________ 。漂白粉长时期露置在空气中会失效,用方程式表示其失效的原因_________________________ ;______________________ 。
| 实验现象 | 解释与结论 |
| (1) | 密度比水小 |
| (2)熔化成闪亮的小球 | |
| (3)四处游动、嘶嘶作响 | |
| (4)反应后溶液呈红色 |
(5)钠与水反应方程式是
(6)实验室常用氢氧化钠溶液来吸收多余的氯气以防止污染空气,请写出发生反应的方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列方程式
(1)Na2O2+CO2_______
(2)Na2O2+H2O_______
(3)Fe+H2O(高温)_______
(4)Na+H2O_______
(5)NaOH和过量的二氧化碳_______
(6)氯化铁溶液中通入硫化氢气体_______
(7)氢氧化亚铁和氧气和水反应生成氢氧化铁_______
(8)饱和食盐水中通入氨气和二氧化碳(工业制碱法)_______
(1)Na2O2+CO2
(2)Na2O2+H2O
(3)Fe+H2O(高温)
(4)Na+H2O
(5)NaOH和过量的二氧化碳
(6)氯化铁溶液中通入硫化氢气体
(7)氢氧化亚铁和氧气和水反应生成氢氧化铁
(8)饱和食盐水中通入氨气和二氧化碳(工业制碱法)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学反应方程式书写
(1)钠和水反应的离子反应方程式___________
(2)碳酸氢钠加热分解的化学反应方程式___________
(3)铝片投入氢氧化钠溶液中的离子反应方程式___________
(4)刻蚀印刷电路板的离子反应方程式___________
(5)氯气和水反应化学反应方程式___________
(6)实验室制备氨气的化学反应方程式___________
(7)实验室制备溴苯的化学反应方程式___________
(8)乙醇和金属钠的化学反应方程式___________
(9)铜和稀硝酸反应的化学反应方程式___________
(10)一氧化氮和氧气的化学方程式___________
(1)钠和水反应的离子反应方程式
(2)碳酸氢钠加热分解的化学反应方程式
(3)铝片投入氢氧化钠溶液中的离子反应方程式
(4)刻蚀印刷电路板的离子反应方程式
(5)氯气和水反应化学反应方程式
(6)实验室制备氨气的化学反应方程式
(7)实验室制备溴苯的化学反应方程式
(8)乙醇和金属钠的化学反应方程式
(9)铜和稀硝酸反应的化学反应方程式
(10)一氧化氮和氧气的化学方程式
您最近一年使用:0次



