下下列反应均可用于实验室制备氯气:
①MnO2+4HCl (浓) MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。
②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
回答下列问题:
(1)请将反应①改写为离子方程式:____________ 。
(2)用双线桥标出反应②的电子转移方向和数目:__________ 。
(3)用单线桥标出反应③的电子转移方向和数目:___________
(4)比较反应①②中氧化剂的氧化性强弱____________ 。
(5)上述反应中浓盐酸显示出来的性质是_________ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(6)若反应①中有17.4 g纯MnO2被还原,则反应①中被氧化的氯化氢的质量为______ 。
(7)当反应①中生成3.01×1023个氯气分子时,则转移的电子数为_____ 。
(8)工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式__________ ,其反应中被氧化的原子与被还原的原子个数之比为_____ 。
①MnO2+4HCl (浓)
 MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
回答下列问题:
(1)请将反应①改写为离子方程式:
(2)用双线桥标出反应②的电子转移方向和数目:
(3)用单线桥标出反应③的电子转移方向和数目:
(4)比较反应①②中氧化剂的氧化性强弱
(5)上述反应中浓盐酸显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(6)若反应①中有17.4 g纯MnO2被还原,则反应①中被氧化的氯化氢的质量为
(7)当反应①中生成3.01×1023个氯气分子时,则转移的电子数为
(8)工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式
19-20高一·浙江·阶段练习 查看更多[2]
更新时间:2020-11-08 08:28:07
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度___________ mol/L。
(2)标准状况下,33.6L的NH3所具有的物质的量为___________ mol,将其溶解于水配成1L的溶液,则溶液的物质的量浓度为___________ mol/L,在Cl2+2NaOH=NaCl+NaClO+H2O的反应中,写出反应的离子方程式___________ 。氧化产物是___________ ,还原产物是___________ ;氧化剂与还原剂的物质的量的比是___________ 。
(3)用双线桥表示出电子转移的方向和数目___________ 。
Cl2+2NaOH=NaCl+NaClO+H2O
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度
(2)标准状况下,33.6L的NH3所具有的物质的量为
(3)用双线桥表示出电子转移的方向和数目
Cl2+2NaOH=NaCl+NaClO+H2O
您最近一年使用:0次
【推荐2】NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
(1)在催化剂作用下,NH3可与NO2发生如下反应:8NH3+6NO2 7N2+12H2O
7N2+12H2O
①该反应的氧化剂是____ 。
②用单线桥表示该反应中电子转移的方向和数目:____ 。
③为研究哪些物质能将NOx转化为N2以消除污染,根据氧化还原反应的知识可知,下列物质中不适宜选用的是_______ (填序号)。
A.CO B.H2 C.CO2
(2)水体中含有较多的硝酸盐会污染水质。一种用铁粉处理水体中的硝酸盐的反应如下:Fe+ +H+-Fe2++
+H+-Fe2++ +H2O(未配平)
+H2O(未配平)
①配平后的反应中H+前的化学计量数为_________ 。
②由反应可知酸性条件下粒子的氧化性大小:____ >____ 。
(1)在催化剂作用下,NH3可与NO2发生如下反应:8NH3+6NO2
 7N2+12H2O
7N2+12H2O①该反应的氧化剂是
②用单线桥表示该反应中电子转移的方向和数目:
③为研究哪些物质能将NOx转化为N2以消除污染,根据氧化还原反应的知识可知,下列物质中不适宜选用的是
A.CO B.H2 C.CO2
(2)水体中含有较多的硝酸盐会污染水质。一种用铁粉处理水体中的硝酸盐的反应如下:Fe+
 +H+-Fe2++
+H+-Fe2++ +H2O(未配平)
+H2O(未配平)①配平后的反应中H+前的化学计量数为
②由反应可知酸性条件下粒子的氧化性大小:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4(Cr元素的化合价为+6价)、Cr(OH)3(Cr元素的化合价为+3价)、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是__________ 。
(2)该反应中,发生还原反应的过程是__________ →__________ 。
(3)写出该反应的化学方程式__________ 。
(4)如反应转移了0.5mol电子,则产生的气体在标准状况下体积为__________ 。
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式
(4)如反应转移了0.5mol电子,则产生的气体在标准状况下体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氯化镁;⑦ ;⑧氨水;⑨
;⑧氨水;⑨ ;⑩硫酸铁溶液。
;⑩硫酸铁溶液。
(1)上述十种物质中,属于电解质的有___________ ,属于非电解质的有___________ 。
(2)④的电子式为___________ 。
(3)用电子式表示⑥的形成过程___________ 。
(4)除去③中少量②的操作是___________ ,化学方程式为___________ 。
(5)⑦中含有的化学键为___________ 。
(6)⑨在水溶液中的电离方程式为___________ 。
Ⅱ.写出下列反应的离子方程式(已知还原性: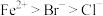 ):
):
(7)向 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 )
)___________ ;
(8)向 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为1∶l∶
的化学计量数之比为1∶l∶___________ 。
 ;⑧氨水;⑨
;⑧氨水;⑨ ;⑩硫酸铁溶液。
;⑩硫酸铁溶液。(1)上述十种物质中,属于电解质的有
(2)④的电子式为
(3)用电子式表示⑥的形成过程
(4)除去③中少量②的操作是
(5)⑦中含有的化学键为
(6)⑨在水溶液中的电离方程式为
Ⅱ.写出下列反应的离子方程式(已知还原性:
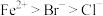 ):
):(7)向
 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 )
)(8)向
 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为1∶l∶
的化学计量数之比为1∶l∶
您最近一年使用:0次
【推荐2】氧化还原反应在物质的制备和转化中有重要的应用。
(1)碘酸钾(KIO3)是一种重要的食品添加剂,可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另一种化合物。
①写出该反应的化学方程式:_____ 。
②该反应中被氧化的I原子与被还原的I原子的物质的量之比为_____ 。
③每生成2molKIO3,该反应中转移电子的物质的量为_____ mol。
(2)一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”能快速溶于水,放出大量CO2,得到ClO2溶液.生成ClO2的化学方程式为5NaClO2+4NaHSO4=4ClO2+NaCl+4Na2SO4+2H2O。
①该反应的离子方程式为_____ 。
②该反应中氧化剂为_____ (填化学式,下同),还原剂为_____ 。
③用双线桥法表示该反应中电子转移的方向和数目:_____ 。
④产生CO2的离子方程式为_____ 。
(1)碘酸钾(KIO3)是一种重要的食品添加剂,可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另一种化合物。
①写出该反应的化学方程式:
②该反应中被氧化的I原子与被还原的I原子的物质的量之比为
③每生成2molKIO3,该反应中转移电子的物质的量为
(2)一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”能快速溶于水,放出大量CO2,得到ClO2溶液.生成ClO2的化学方程式为5NaClO2+4NaHSO4=4ClO2+NaCl+4Na2SO4+2H2O。
①该反应的离子方程式为
②该反应中氧化剂为
③用双线桥法表示该反应中电子转移的方向和数目:
④产生CO2的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.下图为一“链状连环”图案,图案上由左到右分别写了Cl2、NO2、Na2O2、Na2CO3、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分由左到右用A、B、C、D代替。
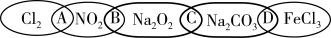
请回答下列问题:
(1)请将上述字母代号填入相应的横线上。(填A、B、C、D)
①两种物质都不属于电解质_______
②两种物质都属于盐类_______
Ⅱ.不同的分类标准可将化学反应分为四种基本反应类型、离子反应和氧化还原反应。
(2)如图为离子反应、氧化还原反应、复分解反应和置换反应之间的关系,其中表示离子反应的是_______ (填字母)。

(3)新冠肺炎期间,化学工业为疫情防控提供了强有力的物质支撑。高铁酸钾是一种高效多功能的绿色消毒剂,工业制备高铁酸钾的方法,主要有湿法和干法两种。
①湿法制备高铁酸钾(K2FeO4)的流程如下:
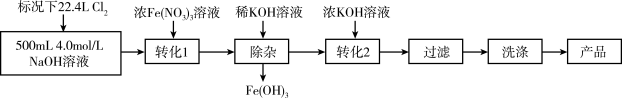
该流程的转化1和转化2反应类型分别属于上图中的_______ 和_______ (填字母)。转化2反应能发生的原因是_______ 。
②干法制备高铁酸钾的第一步反应为: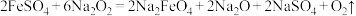 ,该反应中氧化剂和还原剂的物质的量之比为
,该反应中氧化剂和还原剂的物质的量之比为_______ 。
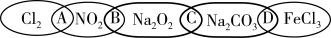
请回答下列问题:
(1)请将上述字母代号填入相应的横线上。(填A、B、C、D)
①两种物质都不属于电解质
②两种物质都属于盐类
Ⅱ.不同的分类标准可将化学反应分为四种基本反应类型、离子反应和氧化还原反应。
(2)如图为离子反应、氧化还原反应、复分解反应和置换反应之间的关系,其中表示离子反应的是

(3)新冠肺炎期间,化学工业为疫情防控提供了强有力的物质支撑。高铁酸钾是一种高效多功能的绿色消毒剂,工业制备高铁酸钾的方法,主要有湿法和干法两种。
①湿法制备高铁酸钾(K2FeO4)的流程如下:

该流程的转化1和转化2反应类型分别属于上图中的
②干法制备高铁酸钾的第一步反应为:
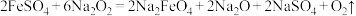 ,该反应中氧化剂和还原剂的物质的量之比为
,该反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次



