Ⅰ.某温度时,在2 L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得:
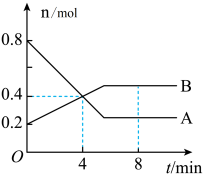
(1)在4 min末时,A、B的物质的量浓度c(A)___ c(B),从0~4 min内A、B的物质的量浓度变化量Δc(A)____ Δc(B)(以上填“>”“<”或“=”)。
(2)从反应开始至4 min时,A的平均反应速率为_____________ 。
(3)该反应的化学方程式为___________________________________ 。
Ⅱ.将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应:2A(g)+B(g)===x C(g)+2D(g),经5 min后,测得D的浓度为0.4 mo·L-1,c(A)∶c(B)=3∶4,C的平均反应速率为0.04 mol·L-1·min-1。求:
(1)5min时,A的体积分数=______ 。
(2)前5 min内B的转化率=______ 。
(3)化学反应方程式中x的值为_________

(1)在4 min末时,A、B的物质的量浓度c(A)
(2)从反应开始至4 min时,A的平均反应速率为
(3)该反应的化学方程式为
Ⅱ.将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应:2A(g)+B(g)===x C(g)+2D(g),经5 min后,测得D的浓度为0.4 mo·L-1,c(A)∶c(B)=3∶4,C的平均反应速率为0.04 mol·L-1·min-1。求:
(1)5min时,A的体积分数=
(2)前5 min内B的转化率=
(3)化学反应方程式中x的值为
更新时间:2020-10-12 20:08:51
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】在2L带气压计的恒容密闭容器中通入2 molX(g)和1molY(g),发生反应:2X(g)+Y(g) 2Z(g) ΔH<0。若达到平衡时气体总物质的量变为原来的0.85倍,请回答下列问题。
2Z(g) ΔH<0。若达到平衡时气体总物质的量变为原来的0.85倍,请回答下列问题。
(1)若反应经历5min达到平衡,则Y的平均反应速率为__ 。
(2)相同条件下进行反应,在t1时刻,只改变下列某一种条件,其曲线图象如图甲。
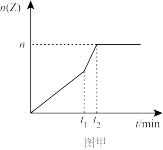
若n=0.9mol,t1时刻改变的条件是__ (填选项编号,A.升温 B.降温 C.加压 D.减压 E.加催化剂),t2__ 5min(填“>”“<”或“=”,下同)。
(3)若其他条件不变,原容器为恒压容器,达到平衡后Z的物质的量__ 0.9mol。
(4)若将物质的量均为3mol的物质X、Y混合于5L容器中发生反应,在反应过程中Z的物质的量分数随温度变化如图乙。
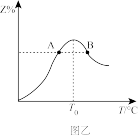
①A、B两点Z物质正反应速率的大小关系是__ ;(速率用A、B表示)
②温度T<T0时,Z%逐渐增大的原因是___ 。
 2Z(g) ΔH<0。若达到平衡时气体总物质的量变为原来的0.85倍,请回答下列问题。
2Z(g) ΔH<0。若达到平衡时气体总物质的量变为原来的0.85倍,请回答下列问题。(1)若反应经历5min达到平衡,则Y的平均反应速率为
(2)相同条件下进行反应,在t1时刻,只改变下列某一种条件,其曲线图象如图甲。

若n=0.9mol,t1时刻改变的条件是
(3)若其他条件不变,原容器为恒压容器,达到平衡后Z的物质的量
(4)若将物质的量均为3mol的物质X、Y混合于5L容器中发生反应,在反应过程中Z的物质的量分数随温度变化如图乙。

①A、B两点Z物质正反应速率的大小关系是
②温度T<T0时,Z%逐渐增大的原因是
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】Ⅰ.在2.0L的密闭容器中,充入1.0molN2和3.0molH2,在一定的条件下反应,2.0分钟后达到平衡状态,相同温度下,测得平衡时混合气体的总物质的量比反应前混合气体的总物质的量减小了 ,填写下列空白:
,填写下列空白:
(1)平衡时混合气体中三种气体的物质的量比为__ 。
(2)N2的转化率为__ 。
(3)2.0分钟内,NH3的平均反应速率为___ 。
Ⅱ.(4)4g硫粉完全燃烧时放出37kJ热量,该反应的热化学方程式是__ 。
(5)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3熔融盐混合物作电解质,CO为负极燃气,空气与CO2混合气体为正极助燃气,制得在650℃下工作的燃料电池,负极反应式:2CO-4e-+2CO =4CO2,正极反应式为
=4CO2,正极反应式为___ 。
 ,填写下列空白:
,填写下列空白:(1)平衡时混合气体中三种气体的物质的量比为
(2)N2的转化率为
(3)2.0分钟内,NH3的平均反应速率为
Ⅱ.(4)4g硫粉完全燃烧时放出37kJ热量,该反应的热化学方程式是
(5)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3熔融盐混合物作电解质,CO为负极燃气,空气与CO2混合气体为正极助燃气,制得在650℃下工作的燃料电池,负极反应式:2CO-4e-+2CO
 =4CO2,正极反应式为
=4CO2,正极反应式为
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】在一个容积为0.5 L的密闭容器中,将2 mol CO和6 mol H2O混合加热到800 ℃,发生反应:CO(g)+H2O(g) CO2(g)+H2(g),经过5 min后达到平衡状态。若此时测得H2的浓度为3 mol·L-1,求:
CO2(g)+H2(g),经过5 min后达到平衡状态。若此时测得H2的浓度为3 mol·L-1,求:
(1)以CO的浓度变化表示的该反应的速率________ 。
(2)达平衡时H2O的转化率。________ 。
(3)已知:在一定温度下,该反应达平衡时,各物质的平衡浓度之间存在以下关系:K= 且当温度不变时K为常数,K不随反应物、生成物浓度的改变而改变。求:
且当温度不变时K为常数,K不随反应物、生成物浓度的改变而改变。求:
①在800℃下,该反应的平衡常数是多少?________
②在800℃下,当投入1 mol CO和4 mol H2O混合加热到平衡时,H2浓度是多少?________
 CO2(g)+H2(g),经过5 min后达到平衡状态。若此时测得H2的浓度为3 mol·L-1,求:
CO2(g)+H2(g),经过5 min后达到平衡状态。若此时测得H2的浓度为3 mol·L-1,求:(1)以CO的浓度变化表示的该反应的速率
(2)达平衡时H2O的转化率。
(3)已知:在一定温度下,该反应达平衡时,各物质的平衡浓度之间存在以下关系:K=
 且当温度不变时K为常数,K不随反应物、生成物浓度的改变而改变。求:
且当温度不变时K为常数,K不随反应物、生成物浓度的改变而改变。求:①在800℃下,该反应的平衡常数是多少?
②在800℃下,当投入1 mol CO和4 mol H2O混合加热到平衡时,H2浓度是多少?
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】T℃时,向5 L密闭容器中充入2 molN2和6 molH2,在10 min时反应达到平衡状态,此时容器中NH3的物质的量是2 mol,则10 min内该反应的平均速率v(N2)=_______ ;N2的平衡转化率为_______ ;平衡时体系内的压强与开始时的压强之比为_______ 。
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】将化合物A的蒸气1 mol通入0.5 L 的容器中加热,发生反应:2A(g) B(g)+nC(g)。反应到3 min时,容器内A的浓度为0.8 mol·L-1,通过测定得这段时间内的平均速率v(C)=0.6 mol·L-1·min-1,则化学方程式中的n值为
B(g)+nC(g)。反应到3 min时,容器内A的浓度为0.8 mol·L-1,通过测定得这段时间内的平均速率v(C)=0.6 mol·L-1·min-1,则化学方程式中的n值为________________ ,用物质B表示这段时间的平均速率v(B)=___________ 。
 B(g)+nC(g)。反应到3 min时,容器内A的浓度为0.8 mol·L-1,通过测定得这段时间内的平均速率v(C)=0.6 mol·L-1·min-1,则化学方程式中的n值为
B(g)+nC(g)。反应到3 min时,容器内A的浓度为0.8 mol·L-1,通过测定得这段时间内的平均速率v(C)=0.6 mol·L-1·min-1,则化学方程式中的n值为
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】一定温度下,将 3molA 气体和 1molB 气体通过一密闭容器中,发生反应: ,若容器体积固定为 2L,反应 1min 时测得剩余1.8molA,C 的浓度为0.4mol·L-1 。
,若容器体积固定为 2L,反应 1min 时测得剩余1.8molA,C 的浓度为0.4mol·L-1 。
①1min内,B 的平均反应速率为_______ ;x=_______ ;此时容器中压强与起始压强之比为_______ ;
②若经反应 2min 达到平衡,平衡时 C 的浓度_______ 0.8mol·L-1 (“大于”、“等于”或“小于” );
③平衡混合物中,C 的体积分数为 30%,则 A 的转化率是_______ (保留 2 位有效数字)。
 ,若容器体积固定为 2L,反应 1min 时测得剩余1.8molA,C 的浓度为0.4mol·L-1 。
,若容器体积固定为 2L,反应 1min 时测得剩余1.8molA,C 的浓度为0.4mol·L-1 。①1min内,B 的平均反应速率为
②若经反应 2min 达到平衡,平衡时 C 的浓度
③平衡混合物中,C 的体积分数为 30%,则 A 的转化率是
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)⇌2NH3(g)。
(1)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,计算a的值:_____ 。
(2)反应达到平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量:_ 。
(3)原混合气体中,a∶b=_____ 。
(4)达到平衡时,N2和H2的转化率之比α(N2)∶α(H2)=____ 。
(1)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,计算a的值:
(2)反应达到平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量:
(3)原混合气体中,a∶b=
(4)达到平衡时,N2和H2的转化率之比α(N2)∶α(H2)=
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)⇌3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,D的化学反应速率v(D)=0.2mol/(L·min)。请回答:
(1)5min末A的物质的量浓度为_______ ;
(2)前5min内用B表示的化学反应速率v(B)为_______ ;
(3)前5min内A的转化率为_______ ;(转化率是指某一反应物的转化百分率)
(4)化学方程式中n的值为_______ ;
(5)此反应在四种不同情况下的反应速率分别为:
①v(A)=5mol/(L·min) ②v(B)=6mol/(L·min)
③v(C)=4.5mol/(L·min) ④v(D)=8mol/(L·min)
其中反应速率最快的是_______ (填编号)。
(1)5min末A的物质的量浓度为
(2)前5min内用B表示的化学反应速率v(B)为
(3)前5min内A的转化率为
(4)化学方程式中n的值为
(5)此反应在四种不同情况下的反应速率分别为:
①v(A)=5mol/(L·min) ②v(B)=6mol/(L·min)
③v(C)=4.5mol/(L·min) ④v(D)=8mol/(L·min)
其中反应速率最快的是
您最近半年使用:0次



