下列各项叙述中,正确的是
| A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| B.外围电子排布式为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
| C.24Cr原子的核外电子排布式是1s22s22p63s23p63d44s2 |
| D.所有原子任一电子层的s电子云轮廓图都是球形,但球的半径大小不同 |
20-21高二上·江苏扬州·期中 查看更多[8]
福建省南平市浦城县2022-2023学年高二下学期期中考试化学试题黑龙江省肇东市第四中学2022-2023学年高二上学期期末考试化学试题山东省烟台市华夏学校2021-2022学年高二上学期期中考试化学试题广东省佛山市顺德区李兆基中学2021-2022学年高二下学期期中考试化学试题(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记(已下线)1.1 原子结构(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)(已下线)第1章 原子结构与元素性质(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)江苏省邗江中学2020-2021学年高二上学期期中考试(2018级新疆班)化学试题
更新时间:2020-11-18 16:27:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法中,正确的是
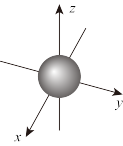

| A.1s电子云轮廓图呈球形,处在该轨道上的电子只能在球壳内运动 |
| B.电子云轮廓图中的小黑点密度大,说明该原子核外空间电子数目多 |
| C.ns能级的原子轨道的电子云轮廓图如图所示 |
| D.3d6表示3d能级有6个原子轨道 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
A.钠原子由 时,原子释放能量,由基态转化成激发态 时,原子释放能量,由基态转化成激发态 |
| B.1s电子云呈球形,表示电子绕原子核做圆周运动 |
| C.电子云轮廓图是把电子在原子核外空间出现概率P=80%的空间圈出来得到的图形 |
| D.同一原子中,2p、3d、4f能级的原子轨道数依次增多 |
您最近一年使用:0次
【推荐1】X、Y、Z、W、R为原子序数依次增大的前四周期元素,X是宇宙中含量最多的元素,Y的最外层有3个未成对电子,Z元素原子的价层电子排布式为 ,W的单质是重要的半导体材料,R属于过渡元素,基态
,W的单质是重要的半导体材料,R属于过渡元素,基态 有电子填充的轨道无成单电子。下列说法正确的是
有电子填充的轨道无成单电子。下列说法正确的是
 ,W的单质是重要的半导体材料,R属于过渡元素,基态
,W的单质是重要的半导体材料,R属于过渡元素,基态 有电子填充的轨道无成单电子。下列说法正确的是
有电子填充的轨道无成单电子。下列说法正确的是| A.R在周期表的d区 | B.第一电离能: |
C.电负性: | D.X与Y形成的化合物一定只含极性共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】现有四种元素基态原子的电子排布式如下。则下列有关比较中不正确的是
①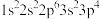 ②
②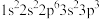 ③
③ ④
④
①
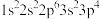 ②
②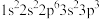 ③
③ ④
④
| A.第一电离能:④>③>②>① | B.原子半径:②>①>③>④ |
| C.电负性:④>①>②>③ | D.最高正化合价:①>③=② |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法或有关化学用语的表达正确的是( )
| A.在基态多电子原子中,d轨道电子能量一定高于s轨道电子能量 |
| B.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 |
| C.基态Cu原子的外围电子排布为3d104s1 |
| D.根据原子核外电子排布的特点,Cu在元素周期表中位于s区 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列关于原子核外电子排布与元素在周期表中位置关系的表述中,正确的是
| A.基态原子的N层上只有一个电子的元素,一定是s区元素 |
| B.原子的价层电子排布式为(n-1)d6-8ns2的元素一定是ds区元素 |
| C.最外层有三个未成对电子的元素一定属于主族元素 |
| D.基态原子的价层电子排布式为(n-1)dxnsy的元素的族序数一定为x+y |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中正确的是
①充有氖气的霓虹灯管通电时会发出红色光的主要原因是电子由基态向激发态跃迁时吸收除红光以外的光线
②常利用原子光谱上的特征谱线来鉴定元素
③增大压强,活化分子百分数增大,单位时间内有效碰撞次数增多,化学反应速率加快
④原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质相似
⑤钠离子的最高能级为3s
⑥25℃时,将V1L pH=2的盐酸与V2 LPH=13的氢氧化钠溶液混合后pH=4,则V1:V2=1001:99
⑦相同温度下,AgCl在相同物质的量浓度的MgCl2和NaCl溶液中溶解度、溶度积常数相同
⑧使用铁触媒能加快合成氨的反应速率实验事实能用勒夏特列原理解释
⑨测定中和反应的反应热时,若将碱分批倒入酸中,则所测得放出的热量偏小
①充有氖气的霓虹灯管通电时会发出红色光的主要原因是电子由基态向激发态跃迁时吸收除红光以外的光线
②常利用原子光谱上的特征谱线来鉴定元素
③增大压强,活化分子百分数增大,单位时间内有效碰撞次数增多,化学反应速率加快
④原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质相似
⑤钠离子的最高能级为3s
⑥25℃时,将V1L pH=2的盐酸与V2 LPH=13的氢氧化钠溶液混合后pH=4,则V1:V2=1001:99
⑦相同温度下,AgCl在相同物质的量浓度的MgCl2和NaCl溶液中溶解度、溶度积常数相同
⑧使用铁触媒能加快合成氨的反应速率实验事实能用勒夏特列原理解释
⑨测定中和反应的反应热时,若将碱分批倒入酸中,则所测得放出的热量偏小
| A.①②③⑦ | B.②④⑥⑨ | C.②⑥⑨ | D.①②③⑦⑧ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各项叙述中,正确的是
| A.镁原子由1s22s22p63s13p1→1s22s22p63p2时,原子吸收能量,由基态转化成激发态 |
| B.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
| C.所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同 |
| D.Cu原子的电子排布图是3d104s1 |
您最近一年使用:0次

 和
和 可形成
可形成 型离子化合物,则
型离子化合物,则 和
和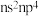
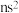 和
和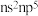
 和
和

