主族元素 和
和 可形成
可形成 型离子化合物,则
型离子化合物,则 和
和 两元素原子的最外层电子排布式分别为( )
两元素原子的最外层电子排布式分别为( )
 和
和 可形成
可形成 型离子化合物,则
型离子化合物,则 和
和 两元素原子的最外层电子排布式分别为( )
两元素原子的最外层电子排布式分别为( )A. 和 和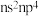 | B.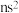 和 和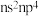 |
C.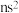 和 和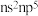 | D. 和 和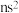 |
19-20高二·全国·课时练习 查看更多[1]
更新时间:2020-03-04 20:56:00
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示的两种化合物可应用于阻燃材料和生物材料的合成,其中W、X、Y、Z为原子序数依次增大的短周期元素,Y与W同主族。下列说法正确的是


| A.X的最高正价为+7 |
| B.原子半径:Y<Z |
| C.简单氢化物的沸点:W>X |
| D.H与W、X三种元素可形成离子化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】X、Y、Z、W、M均为短周期元素,X、Y同主族,X的氢化物和最高价氧化物的水化物能反应生成一种离子化合物,其水溶液显酸性;Z、W、M是第3周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M.下列叙述正确的是
| A.Z是海水中含量最高的金属元素,W是地壳中含量最多的金属元素 |
| B.X、M两元素氢化物的稳定性:X<M |
| C.Z和W的氧化物均可做耐高温材料,M的氧化物可做太阳能电池 |
| D.X、W的最高价氧化物的水化物间反应生成一种可净水的化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】随着原子序数的递增,八种短周期元素(用字母x等表示)原子半径的相对大小,最高正价或最低负价的变化如图所示,下列说法错误的是


| A.常见离子半径:g>h>d>e |
| B.上述元素组成的ZX4f(gd4)2溶液中,离子浓度:c(f3+)>c(zx4+) |
| C.由d、e、g三种元素组成的盐溶液和稀硫酸反应可能生成沉淀 |
| D.f的最高价氧化物的水化物可以分别与e和h的最高价氧化物的水化物发生反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】短周期元素X、Y、Z、W原子序数依次增大,X原子最外层电子数是其电子层数的3倍,Y与X可形成Y2X2和Y2X两种离子化合物,Y、Z均是来自海水的活泼金属,X原子的核外最外层电子数是Z原子的最外层电子数的3倍,W与X同主族。下列说法正确的是
| A.X分别与Y、Z形成的化合物中化学键类型完全相同 |
| B.原子半径:Y<Z<W |
| C.气态氢化物的稳定性:X>W |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】血红蛋白结合 后的结构如图所示,
后的结构如图所示, 也可与血红蛋白结合。下列说法错误的是
也可与血红蛋白结合。下列说法错误的是
 后的结构如图所示,
后的结构如图所示, 也可与血红蛋白结合。下列说法错误的是
也可与血红蛋白结合。下列说法错误的是
A.血红蛋白中心离子 与卟啉环形成6个螯合键 与卟啉环形成6个螯合键 |
B. 与血红蛋白结合时, 与血红蛋白结合时, 原子提供孤电子对 原子提供孤电子对 |
C.第一电离能: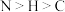 |
D.基态 含有4个未成对电子 含有4个未成对电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】研究笼形包合物结构和性质具有重要意义,化学式为Ni(CN)x•Zn(NH3)y•zC6H6的笼形包合物四方晶胞结构如图所示(H原子未画出)。每个苯环只有一半属于该晶胞,晶胞参数为a=b≠c,α=β=γ=90°。晶胞中N原子均参与形成配位键。下列说法不正确的是
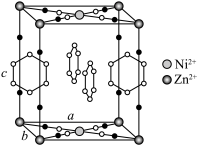

| A.基态Ni原子的价电子排布式为3d84s2 |
| B.Ni2+与Zn2+的配位数之比为2:3 |
| C.x:y:z=2:1:1 |
| D.晶胞中有d轨道参与杂化的金属离子是Zn2+ |
您最近一年使用:0次


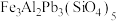 ,其组成也可写成的氧化物形式:
,其组成也可写成的氧化物形式: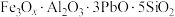 。下列说法正确的是
。下列说法正确的是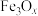 中Fe(II)与Fe(III)的个数比为2:1
中Fe(II)与Fe(III)的个数比为2:1

