下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)非金属性最强的元素是______ (填元素符号,下同),形成化合物种类最多的元素是________________________ 。
(2)第三周期元素除⑩外原子半径最小的是______ (填元素符号),
(3)这些元素的最高价氧化物对应水化物中碱性最强的是__________ (填化学式,下同),具有两性的是____________ 。
(4)⑤、⑧两种元素的最高价氧化物对应的水化物相互反应的离子方程式为__________ 。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)非金属性最强的元素是
(2)第三周期元素除⑩外原子半径最小的是
(3)这些元素的最高价氧化物对应水化物中碱性最强的是
(4)⑤、⑧两种元素的最高价氧化物对应的水化物相互反应的离子方程式为
更新时间:2020-11-30 17:06:39
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】胃舒平主要成分是氢氧化铝,同时含有三硅酸镁(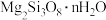 )等化合物。
)等化合物。
(1)铝单质与同周期中非金属性最强的元素的气态氢化物的水溶液之间发生反应的离子方程式为:____________
(2)某元素与铝元素同周期且原子半径比镁原子半径大,写出该元素符号______ ,该元素的最高价氧化物的水化物与铝元素的最高价氧化物的水化物之间发生反应的离子方程式为:______________
(3) 、MgO和
、MgO和 都可以制耐火材料,其原因是
都可以制耐火材料,其原因是______
a. 、MgO和
、MgO和 都是白色固体
都是白色固体
b. 、MgO和
、MgO和 都是氧化物
都是氧化物
c. 、MgO和
、MgO和 都有很高的熔点
都有很高的熔点
(4)氢氧化铝在强酸溶液中的电离方程式________ 。
(5)明矾常用作净水剂,结合相关理论解释其净水原理__________ 。
(6)用于治疗胃酸过多的药物还有多种,请写出其中一种的化学式_____________ 。
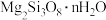 )等化合物。
)等化合物。(1)铝单质与同周期中非金属性最强的元素的气态氢化物的水溶液之间发生反应的离子方程式为:
(2)某元素与铝元素同周期且原子半径比镁原子半径大,写出该元素符号
(3)
 、MgO和
、MgO和 都可以制耐火材料,其原因是
都可以制耐火材料,其原因是a.
 、MgO和
、MgO和 都是白色固体
都是白色固体 b.
 、MgO和
、MgO和 都是氧化物
都是氧化物c.
 、MgO和
、MgO和 都有很高的熔点
都有很高的熔点(4)氢氧化铝在强酸溶液中的电离方程式
(5)明矾常用作净水剂,结合相关理论解释其净水原理
(6)用于治疗胃酸过多的药物还有多种,请写出其中一种的化学式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)M能层上有________ 个能级,有________ 个轨道,作为内层最多可容纳________ 个电子,作为最外层时,最多可含有________ 个未成对电子。
(2)E原子核外电子占有9个轨道,且具有1个未成对电子,E离子结构示意图是____________ 。
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,则G元素的原子序数是________ ,F2-的电子排布式是______________ 。
(2)E原子核外电子占有9个轨道,且具有1个未成对电子,E离子结构示意图是
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,则G元素的原子序数是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】有H、C、O、Na、Mg、Al、P、Cl、Ar等9种元素或它们的原子。如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:(1)原子核对核外电子的吸引力(2)形成稳定结构的倾向。下表是一些气态原子失去核外不同电子所需的能量( ):
):
(1)通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量_______ 。
(2)表中X可能为以上9种元素中的_______ (填写元素符号)元素。用元素符号表示X和地壳中含量占第一位的元素形成化合物的化学式_______ 。
(3)Y是周期表中_______ 族元素。
(4)以上9种元素中,_______ (填写字母)元素原子失去核外第一个电子需要的能量最多。
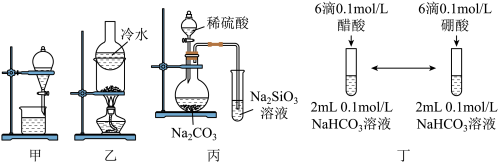
(5)下列实验装置符合题意且能达到相应实验目的的是_______。
 ):
):| 锂 | X | Y | |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7296 | 4570 | 1820 |
| 失去第三个电子 | 11799 | 6920 | 2750 |
| 失去第四个电子 | 9550 | 11600 |
(2)表中X可能为以上9种元素中的
(3)Y是周期表中
(4)以上9种元素中,
(5)下列实验装置符合题意且能达到相应实验目的的是_______。

A.装置甲利用 提取苯中溶解的 提取苯中溶解的 |
B.装置乙分离 和 和 固体 固体 |
| C.装置丙验证非金属性S>C>Si(已知硅酸不溶于水) |
| D.装置丁比较醋酸与硼酸酸性(已知酸性醋酸>碳酸) |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下面是元素周期表的一部分,表中的每个字母表示一种短周期元素,请回答下列问题:
(1)D的最高价氧化物对应的水化物的化学式是__________ 。
(2)A、E两种元素中非金属较强的是___________ (填元素符号)。
(3)B、C两元素的原子半径较小的是___________ (填元素符号)。
(4)在盛有水的小烧杯中加入元素B的单质,发生反应的化学方程式为:_____________ 。
| A | ||||||||
| B | C | D | E | |||||
(1)D的最高价氧化物对应的水化物的化学式是
(2)A、E两种元素中非金属较强的是
(3)B、C两元素的原子半径较小的是
(4)在盛有水的小烧杯中加入元素B的单质,发生反应的化学方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】分子筛是一类具有规整孔道结构的多孔材料,能够选择性吸附空间结构各异和不同尺寸的分子,在化学工业中有着广泛的应用。近年来,我国科学家在分子筛研究领域不断取得新的突破。这些研究中涉及的部分元素在周期表中位置如下:
(1)近期我国科学家制备了一种无缺陷的分子筛膜,可高效分离CH4与CO2两种气体。下列有关分子空间结构的描述正确的是_______
(2)传统的分子筛主要含有O、Na、Al和Si元素,通过调控这 4种元素的比例,可获得不同性能的分子筛产品。这4种元素描述中正确的是_______ 。
(3)通过将分子筛中的元素Na替换为K或Ca,可改变分子筛的孔径大小。这3种元素中说法正确的是_______
(4)N2常用于分子筛的孔结构测试,H、O和N元素可形成多种物质。下列说法正确的是_______
(5)某些分子筛可以选择性吸附Ar。Ar位于元素周期表的_______
| 周期 | 族 | ||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 1 | H | ||||||
| 2 | C | N | O | ||||
| 3 | Na | Al | Si | ||||
| 4 | K | Ca | |||||
| A.CH4是平面结构 | B.CO2是V形结构 |
| C.CH4是正四面体结构 | D.CO2是直线形结构 |
| A.非金属性最强的是O |
| B.核外电子数最少的是 Na |
| C.金属性最强的是Al |
| D.原子半径最大的是Si |
| A.仅Na可与Cl2反应 |
| B.K的单质与水的反应最剧烈 |
| C.Na的氧化物与水的反应均为化合反应 |
| D.Ca的最高价氧化物的水化物碱性最强 |
| A.N2中含有共价三键 |
| B.NO可由NH3催化氧化得到 |
| C.NH3的水溶液呈碱性 |
| D.稀HNO3与Cu反应产生H2 |
| A.第二周期 | B.Ⅷ族 | C.第三周期 | D.0族 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期表的重要性。下表列出了a-j 10种元素在周期表中的位置:
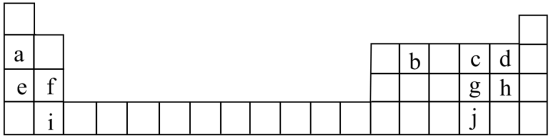
(1)元泰a的原于结构示意图为__________ 。
(2)元素b可以形成多种单质,写出其中的两种____________________ (填名称)。
(3)元素a~j中非金属性最强的是___________ (填元素符号)。
(4)若e单质着火,可用于灭火的物质是___________ (填字母)
A 自来水 B CO2. C 干沙子 D 湿抹布
(5)元素h和i形成的化合物中化学键的类型是___________ 键。h单质与NaOH溶液反应的离子方程式为____________ 。
(6)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法正确的有___________ (填字母)。
A a的金属性比e弱 B 自然界中,e的储量比a高
B a的原子半径比e大 D 基于a的电池质量轻、易携带

(1)元泰a的原于结构示意图为
(2)元素b可以形成多种单质,写出其中的两种
(3)元素a~j中非金属性最强的是
(4)若e单质着火,可用于灭火的物质是
A 自来水 B CO2. C 干沙子 D 湿抹布
(5)元素h和i形成的化合物中化学键的类型是
(6)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法正确的有
A a的金属性比e弱 B 自然界中,e的储量比a高
B a的原子半径比e大 D 基于a的电池质量轻、易携带
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)补充完成下表:
①____________ 、②____________ 、③____________ 、④____________
(2)甲元素最高价氧化物对应的水化物呈_________ 性(填“酸、碱”),氧化性最强的单质为___________ ,乙和丙氢化物稳定性___________ >___________ (填分子式)
(3)甲与乙两元素的单质反应生成物的电子式为__________ ,
(4)比较这四种元素的原子半径大小:_____ >_____ >_____ >______ (填元素符号)
(5)甲单质与丙的氢化物反应的离子方程式为_________________________________
(6)甲元素最高价氧化物对应水化物与丁元素最高价氧化物反应的化学方程式为__________
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 元素符号 | ① | F | O | Al |
| 原子结构示意图 | 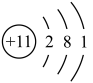 | ② | 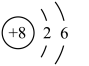 |  |
| 周期 | 三 | 二 | 二 | ④ |
| 族 | IA | VIIA | ③ | IIIA |
①
(2)甲元素最高价氧化物对应的水化物呈
(3)甲与乙两元素的单质反应生成物的电子式为
(4)比较这四种元素的原子半径大小:
(5)甲单质与丙的氢化物反应的离子方程式为
(6)甲元素最高价氧化物对应水化物与丁元素最高价氧化物反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)请从原子结构角度解释硅元素与碳元素非金属性强弱的原因___________ 。
(2)醋酸可通过分子间氢键双聚形成八元环,画出该结构___________ 。(以O…H—O表示氢键)
(3)已知碳化镁Mg2C3可与水反应生成丙炔,画出Mg2C3的电子式___________ 。
(2)醋酸可通过分子间氢键双聚形成八元环,画出该结构
(3)已知碳化镁Mg2C3可与水反应生成丙炔,画出Mg2C3的电子式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】对于周期表中下列位置的①~⑩十种元素,根据有关要求回答:
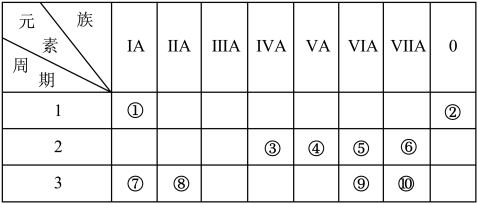
(1)写出⑥形成简单离子的结构示意图___________ 。
(2)用电子式表示⑧与⑩形成化合物的形成过程___________ 。
(3)⑦的最高价氧化物的水化物与⑩的单质反应的离子方程式___________ 。
(4)写出①与⑤形成原子个数比为1:1的化合物的结构式___________ 。
(5)④⑤⑥形成简单气态氢化物的稳定性(用化学式表示)___________ 。
(6)⑥⑦⑨形成简单离子半径由大到小的顺序为(用微粒符号表示)___________ 。
(7)写出③的单质与⑨的最高价氧化物的水化物反应的化学方程式___________ 。写出鉴别产物中两种气态氧化物的化学方法(任写一种):___________ 。

(1)写出⑥形成简单离子的结构示意图
(2)用电子式表示⑧与⑩形成化合物的形成过程
(3)⑦的最高价氧化物的水化物与⑩的单质反应的离子方程式
(4)写出①与⑤形成原子个数比为1:1的化合物的结构式
(5)④⑤⑥形成简单气态氢化物的稳定性(用化学式表示)
(6)⑥⑦⑨形成简单离子半径由大到小的顺序为(用微粒符号表示)
(7)写出③的单质与⑨的最高价氧化物的水化物反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
(2)近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为FeSmAsFO组成的化合物。回答下列问题:
①Fe成为阳离子时首先失去___________ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___________ 。
②比较离子半径:F___________ O2-(填“大于”“等于”或“小于”)。
(3)在周期表中,与Li的化学性质最相似的邻族元素是___________ ,该元素基态原子核外M层电子的自旋状态___________ (填“相同”或“相反”)。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
A.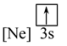 | B.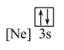 | C.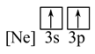 | D.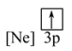 |
①Fe成为阳离子时首先失去
②比较离子半径:F
(3)在周期表中,与Li的化学性质最相似的邻族元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增加。回答下列问题:
(1)2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”。元素Mc可由反应: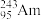 +
+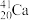 =
=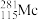 +3
+3 得到。该元素在周期表中的位置是
得到。该元素在周期表中的位置是___________ 。
(2)元素N的一种氢化物为N2H4,写出该化合物分子的电子式___________ ;该分子内存在的共价键类型有___________ 。
(3)铍、铝二者的单质、化合物均具有相似的化学性质,写出BeO溶液与NaOH的水溶液混合的化学方程式___________ 。
(1)2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”。元素Mc可由反应:
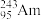 +
+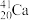 =
=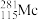 +3
+3 得到。该元素在周期表中的位置是
得到。该元素在周期表中的位置是(2)元素N的一种氢化物为N2H4,写出该化合物分子的电子式
(3)铍、铝二者的单质、化合物均具有相似的化学性质,写出BeO溶液与NaOH的水溶液混合的化学方程式
您最近一年使用:0次

 中心原子价层电子对互斥模型为
中心原子价层电子对互斥模型为 的空间结构为
的空间结构为 ,该分子中含有
,该分子中含有

