完成下列问题。
I.海带中含有丰富的碘,从海带中提取碘,某学习小组设计并进行以下实验:
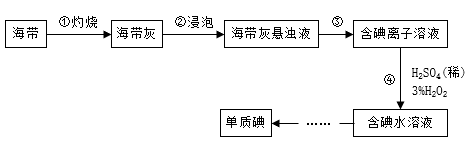
(1)步骤③的实验操作为______ (填实验名称),此过程使用玻璃棒,玻璃棒的作用是____________ 。
(2)步骤④的离子反应方程式为:H2O2+2H++2I-=I2+2H2O。该离子反应中的氧化剂是________ ,还原剂是_______ 。
(3)步骤④得到的含碘水溶液中滴加淀粉溶液,溶液呈现_______ 色,说明有碘单质产生。
II.碘称为“智力元素”。过去食盐中KI作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失,I-被氧气氧化成碘单质(I2),同时得到强碱性物质。
(4)写出潮湿环境下KI与氧气反应的化学方程式:_______ 。
现在的食盐里改添加性质稳定的KIO3,以满足人们需要。几种粒子之间有如图所示关系:
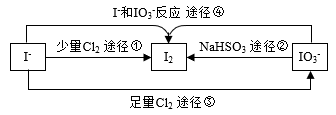
(5)四个途径中属于氧化还原反应的是______ (填序号)。
(6)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(KIO4),反应方程式为:Cl2+KIO3+2KOH=2KCl+KIO4+H2O,写出该反应的离子方程式:________ 。
(7)比较I2、 和Cl2的氧化性强弱:
和Cl2的氧化性强弱:_________ 。
I.海带中含有丰富的碘,从海带中提取碘,某学习小组设计并进行以下实验:

(1)步骤③的实验操作为
(2)步骤④的离子反应方程式为:H2O2+2H++2I-=I2+2H2O。该离子反应中的氧化剂是
(3)步骤④得到的含碘水溶液中滴加淀粉溶液,溶液呈现
II.碘称为“智力元素”。过去食盐中KI作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失,I-被氧气氧化成碘单质(I2),同时得到强碱性物质。
(4)写出潮湿环境下KI与氧气反应的化学方程式:
现在的食盐里改添加性质稳定的KIO3,以满足人们需要。几种粒子之间有如图所示关系:

(5)四个途径中属于氧化还原反应的是
(6)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(KIO4),反应方程式为:Cl2+KIO3+2KOH=2KCl+KIO4+H2O,写出该反应的离子方程式:
(7)比较I2、
 和Cl2的氧化性强弱:
和Cl2的氧化性强弱:
更新时间:2020-12-01 14:17:32
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】工业以软锰矿(主要成分是 ,含有
,含有 、
、 等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(
等少量杂质)为主要原料制备高性能的磁性材料碳酸锰( )。其工业流程如下:
)。其工业流程如下:

(1)浸锰过程中 与
与 反应的离子方程式为
反应的离子方程式为 ,该反应是经历以下两步反应实现的。
,该反应是经历以下两步反应实现的。
i.
ii.……
写出ii的离子方程式:_______ 。
(2)氧化过程中被 氧化的物质主要有(写化学式):
氧化的物质主要有(写化学式):_______ 。
(3)“浸锰”反应中往往有副产物 生成,温度对“浸锰”反应的影响如图所示:
生成,温度对“浸锰”反应的影响如图所示:

为减少 的生成,“浸锰”的适宜温度是
的生成,“浸锰”的适宜温度是_______ ,向过滤II所得的滤液中加入 溶液时温度不宜太高的原因是
溶液时温度不宜太高的原因是_______ 。
(4)加入 溶液后,生成
溶液后,生成 沉淀,同时还有气体生成,写出反应的离子方程式:
沉淀,同时还有气体生成,写出反应的离子方程式:_____ 。
(5)滴定法测产品纯度
I.取固体产品1.160g于烧杯中,加入过量稀 充分振荡,再加入NaOH溶液至碱性,发生反应:
充分振荡,再加入NaOH溶液至碱性,发生反应: ;
;
II.加入过量KI溶液和适量稀 ,沉淀溶解,溶液变黄;
,沉淀溶解,溶液变黄;
III.取上述混合液的 于锥形瓶中,加入淀粉溶液作指示剂,用0.1000mol/L
于锥形瓶中,加入淀粉溶液作指示剂,用0.1000mol/L  溶液进行滴定,发生反应:
溶液进行滴定,发生反应: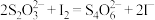 ,滴定终点时消耗
,滴定终点时消耗 溶液20.00mL。
溶液20.00mL。
①写出II中反应的离子方程式_______ ;
②判断滴定终点的方法是_______ ;
③假设杂质不参与反应,则产品纯度为_______ 。(保留四位有效数字)
 ,含有
,含有 、
、 等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(
等少量杂质)为主要原料制备高性能的磁性材料碳酸锰( )。其工业流程如下:
)。其工业流程如下:
(1)浸锰过程中
 与
与 反应的离子方程式为
反应的离子方程式为 ,该反应是经历以下两步反应实现的。
,该反应是经历以下两步反应实现的。i.

ii.……
写出ii的离子方程式:
(2)氧化过程中被
 氧化的物质主要有(写化学式):
氧化的物质主要有(写化学式):(3)“浸锰”反应中往往有副产物
 生成,温度对“浸锰”反应的影响如图所示:
生成,温度对“浸锰”反应的影响如图所示:
为减少
 的生成,“浸锰”的适宜温度是
的生成,“浸锰”的适宜温度是 溶液时温度不宜太高的原因是
溶液时温度不宜太高的原因是(4)加入
 溶液后,生成
溶液后,生成 沉淀,同时还有气体生成,写出反应的离子方程式:
沉淀,同时还有气体生成,写出反应的离子方程式:(5)滴定法测产品纯度
I.取固体产品1.160g于烧杯中,加入过量稀
 充分振荡,再加入NaOH溶液至碱性,发生反应:
充分振荡,再加入NaOH溶液至碱性,发生反应: ;
;II.加入过量KI溶液和适量稀
 ,沉淀溶解,溶液变黄;
,沉淀溶解,溶液变黄;III.取上述混合液的
 于锥形瓶中,加入淀粉溶液作指示剂,用0.1000mol/L
于锥形瓶中,加入淀粉溶液作指示剂,用0.1000mol/L  溶液进行滴定,发生反应:
溶液进行滴定,发生反应: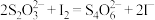 ,滴定终点时消耗
,滴定终点时消耗 溶液20.00mL。
溶液20.00mL。①写出II中反应的离子方程式
②判断滴定终点的方法是
③假设杂质不参与反应,则产品纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下:

(1)为加快工业废碱渣中Na2CO3的溶解,可采取的措施是___________ (写出一种即可)。
(2)过程①进行的操作是___________ 。
(3)上述流程中的SO2是酸性氧化物,原因是:___________ 。(用化学方程式表示)
(4)加入NaOH后,发生反应的离子方程式为___________ 。
(5)亚硫酸钠粗品中含有少量Na2SO4,原因是___________ 。
(6)设计实验证明亚硫酸钠粗品含有少量Na2SO4的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,___________ ,出现白色沉淀,则证明含有Na2SO4。

(1)为加快工业废碱渣中Na2CO3的溶解,可采取的措施是
(2)过程①进行的操作是
(3)上述流程中的SO2是酸性氧化物,原因是:
(4)加入NaOH后,发生反应的离子方程式为
(5)亚硫酸钠粗品中含有少量Na2SO4,原因是
(6)设计实验证明亚硫酸钠粗品含有少量Na2SO4的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】海洋化学资源的综合利用对人类的发展意义重大。
Ⅰ.以海水为原料获得的粗盐中含有 、
、 、
、 和难溶性杂质。
和难溶性杂质。
(1)除去粗盐中可溶性杂质,加入试剂的顺序是_______ (填标号),过滤,滴加稀盐酸调节溶液呈中性。
A.


B.


C.


Ⅱ.从海藻中提取碘:
步骤一:制备含碘离子的溶液

(2)实验室焙烧海藻的装置如图,仪器A的名称是_______ 。

步骤二:活性炭吸附法提取碘,其流程如下:
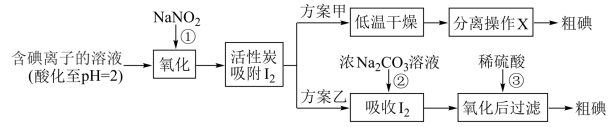
资料显示: 时,
时, 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO。
,同时生成NO。
(3)写出反应①的离子方程式:_______ 。
(4)方案甲中,根据 的特性,分离操作X应为
的特性,分离操作X应为_______ 、_______ 。
(5)方案乙中, 浓溶液吸收
浓溶液吸收 有
有 生成,写出反应②的离子方程式:
生成,写出反应②的离子方程式:_______ 。
(6)方案乙中,已知:反应③充分进行后,过滤,滤液中仍存在少量的 、
、 。为检验滤液中的
。为检验滤液中的 ,请将下列实验方案补充完整。实验中可供选择的试剂:稀
,请将下列实验方案补充完整。实验中可供选择的试剂:稀 、淀粉溶液、
、淀粉溶液、 溶液、
溶液、 。
。
A.将滤液_______ ,直到水层用淀粉溶液检验不出碘单质存在。
B.从水层取少量溶液于试管中,_______ 。
Ⅰ.以海水为原料获得的粗盐中含有
 、
、 、
、 和难溶性杂质。
和难溶性杂质。(1)除去粗盐中可溶性杂质,加入试剂的顺序是
A.



B.



C.



Ⅱ.从海藻中提取碘:
步骤一:制备含碘离子的溶液

(2)实验室焙烧海藻的装置如图,仪器A的名称是

步骤二:活性炭吸附法提取碘,其流程如下:

资料显示:
 时,
时, 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO。
,同时生成NO。(3)写出反应①的离子方程式:
(4)方案甲中,根据
 的特性,分离操作X应为
的特性,分离操作X应为(5)方案乙中,
 浓溶液吸收
浓溶液吸收 有
有 生成,写出反应②的离子方程式:
生成,写出反应②的离子方程式:(6)方案乙中,已知:反应③充分进行后,过滤,滤液中仍存在少量的
 、
、 。为检验滤液中的
。为检验滤液中的 ,请将下列实验方案补充完整。实验中可供选择的试剂:稀
,请将下列实验方案补充完整。实验中可供选择的试剂:稀 、淀粉溶液、
、淀粉溶液、 溶液、
溶液、 。
。A.将滤液
B.从水层取少量溶液于试管中,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氯化亚铜(CuCl)是一种难溶于水的白色粉末,不溶于乙醇,可溶于浓盐酸和氨水,在潮湿空气中被氧化成绿色的碱式氯化铜[Cu2(OH)3Cl]。工业上常以海绵铜(主要成分是 Cu,含有少量CuO)为原料生产CuCl,其工艺流程如下:
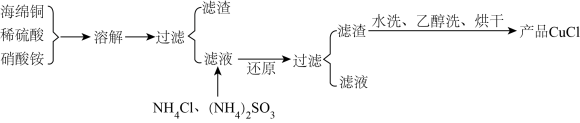
(1)配平“溶解”过程中发生的氧化还原反应的离子方程式:
____ Cu+___ +____  =
= _____ Cu2++____ NO↑ +___ H2O
(2)还原“”过程中,作还原剂的是_________ (填化学式);写出“还原”过程中发生反应的离子方程式:_________ 。
(3)写出氯化亚铜在潮湿的空气中被氧化的化学方程式:______ 。
(4)析出的CuCl晶体水洗后要立即用无水乙醇洗涤,并在真空干燥机内于70℃下干燥2 h,冷却密封包装。密封包装的原因是______ 。

(1)配平“溶解”过程中发生的氧化还原反应的离子方程式:
 =
= (2)还原“”过程中,作还原剂的是
(3)写出氯化亚铜在潮湿的空气中被氧化的化学方程式:
(4)析出的CuCl晶体水洗后要立即用无水乙醇洗涤,并在真空干燥机内于70℃下干燥2 h,冷却密封包装。密封包装的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
真题
解题方法
【推荐2】铜及其化合物在生产生活中有重要作用。
(1)基态Cu原子的价层电子排布式是______ , 与
与 相比较,离子半径较大的是
相比较,离子半径较大的是______ 。
(2)铜的一种化合物的晶胞如图所示,其化学式为______ 。 ,写出该反应化学方程式:
,写出该反应化学方程式:______ 。反应中,H2O2实际消耗量大于理论用量的原因是______ 。H2O2电子式为______ 。
(4)上述制备反应中,下列物质均可替代H2O2作氧化剂,最适合的是是______ (填序号)。
a.硝酸 b. c.
c.
(5)Cu2+和I-的反应可用于Cu含量的定量分析。向CuCl2溶液中滴入KI溶液,生成一种碘化物白色沉淀,且上层溶液可使淀粉溶液变蓝。该白色沉淀的化学式为______ 。反应中KI的作用为______ 。
(1)基态Cu原子的价层电子排布式是
 与
与 相比较,离子半径较大的是
相比较,离子半径较大的是(2)铜的一种化合物的晶胞如图所示,其化学式为

 ,写出该反应化学方程式:
,写出该反应化学方程式:(4)上述制备反应中,下列物质均可替代H2O2作氧化剂,最适合的是是
a.硝酸 b.
 c.
c.
(5)Cu2+和I-的反应可用于Cu含量的定量分析。向CuCl2溶液中滴入KI溶液,生成一种碘化物白色沉淀,且上层溶液可使淀粉溶液变蓝。该白色沉淀的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】光纤通讯是光导纤维传送信号的一种通讯手段,合成光导纤维及氮化硅(一种无机涂层)的工艺流程如下:

回答下列问题:
(1)反应I的化学方程式为2C+ SiO2 Si+2CO↑,其中还原剂为
Si+2CO↑,其中还原剂为_______ (填化学式),该反应涉及的副反应可能有(碳不足)C+ SiO2 Si+CO2↑和(碳足量)
Si+CO2↑和(碳足量)_______________ 。
(2)经反应Ⅱ所得的四氯化硅粗品中所含的物质如下:
图中 “操作X”的名称为_______ ;PCl3的电子式为_______ 。
(3)已知反应Ⅳ的化学方程式为3SiCl4+4NH3 Si3N4+12HCl,则反应Ⅲ和Ⅳ中尾气的用途为
Si3N4+12HCl,则反应Ⅲ和Ⅳ中尾气的用途为________ 。若向一2L恒容密闭容器中投入1 mol SiC14和1 mol NH3,6 min后反应完全,则0~6 min内,HCl的平均反应速率为____________ mol·L-1·min-1。

回答下列问题:
(1)反应I的化学方程式为2C+ SiO2
 Si+2CO↑,其中还原剂为
Si+2CO↑,其中还原剂为 Si+CO2↑和(碳足量)
Si+CO2↑和(碳足量)(2)经反应Ⅱ所得的四氯化硅粗品中所含的物质如下:
| 组分名称 | SiCl4 | SiHCl3 | SiH2Cl2 | HCl | BCl3 | PCl3 |
| 质量分数 | 0.545 | 0.405 | 0.0462 | 0.0003 | 0.00193 | 0.00157 |
| 沸点/℃ | 57.6 | 31. 8 | 8. 2 | -85 | 12. 5 | 75. 5 |
(3)已知反应Ⅳ的化学方程式为3SiCl4+4NH3
 Si3N4+12HCl,则反应Ⅲ和Ⅳ中尾气的用途为
Si3N4+12HCl,则反应Ⅲ和Ⅳ中尾气的用途为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】NaClO2是一种重要的杀菌消毒剂,其一种生产工艺如图:

(1)NaClO2中Cl的化合价为_______ 。
(2)写出“反应”步骤中生成ClO2的化学方程式_______ 。
(3)“尾气吸收”是吸收“电解”过程排出的少量ClO2,发生如下反应:2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O
①用单线桥表示电子转移方向和数目_______ 。
②此吸收反应中,氧化产物是_______ ,氧化剂与还原剂的物质的量之比为_______ 。
③比较氧化性:ClO2_______ O2(填“>”、“<”或“=”)。

(1)NaClO2中Cl的化合价为
(2)写出“反应”步骤中生成ClO2的化学方程式
(3)“尾气吸收”是吸收“电解”过程排出的少量ClO2,发生如下反应:2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O
①用单线桥表示电子转移方向和数目
②此吸收反应中,氧化产物是
③比较氧化性:ClO2
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】为探究 、
、 、
、 氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验;查阅资料可知,
氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验;查阅资料可知, 易溶于
易溶于 )。
)。
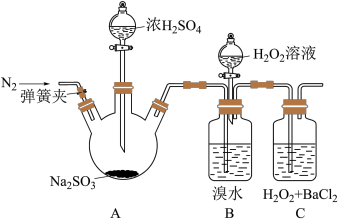
(1)A中发生反应(填“是”或“不是”)___________ 氧化还原反应。
(2)B中红棕色溴水褪色,此时发生反应的离子方程式___________ 。
(3)C中产生的白色沉淀是___________ 。
(4)甲同学通过C中产生白色沉淀,得出结论,氧化性: 。
。
①乙同学认为不能得出此结论,对实验进行了改进:打开弹簧夹,通入 ,待排净装置内空气后,关闭弹簧夹,再打开A中分液漏斗活塞;
,待排净装置内空气后,关闭弹簧夹,再打开A中分液漏斗活塞;
②丙同学进行了进一步的改进:在B和C之间增加盛放 的洗气瓶D,丙同学的目的是
的洗气瓶D,丙同学的目的是___________ 。
③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:氧化性 。
。
(5)iii中滴入少量 没有明显变化。提出假设:
没有明显变化。提出假设:
观点1: 的量少不能氧化
的量少不能氧化
观点2:B中有未反应
为验证观点2,应进行的实验操作及现象是:取少量颜色变化前的B中溶液于试管中___________ 。继续滴加 溶液,一段时间后,混合液逐渐变成红棕色,此时发生反应的离子方程式
溶液,一段时间后,混合液逐渐变成红棕色,此时发生反应的离子方程式___________ 。
(6)通过上述全部实验,得出结论: 、
、 、
、 氧化性由强到弱的顺序是
氧化性由强到弱的顺序是___________ 。
 、
、 、
、 氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验;查阅资料可知,
氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验;查阅资料可知, 易溶于
易溶于 )。
)。
实验操作 | 实验现象 |
i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
iii.打开B中分液漏斗活塞,逐滴滴加 | 开始时颜色无明显变化;继续滴加 |
(2)B中红棕色溴水褪色,此时发生反应的离子方程式
(3)C中产生的白色沉淀是
(4)甲同学通过C中产生白色沉淀,得出结论,氧化性:
 。
。①乙同学认为不能得出此结论,对实验进行了改进:打开弹簧夹,通入
 ,待排净装置内空气后,关闭弹簧夹,再打开A中分液漏斗活塞;
,待排净装置内空气后,关闭弹簧夹,再打开A中分液漏斗活塞;②丙同学进行了进一步的改进:在B和C之间增加盛放
 的洗气瓶D,丙同学的目的是
的洗气瓶D,丙同学的目的是③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:氧化性
 。
。(5)iii中滴入少量
 没有明显变化。提出假设:
没有明显变化。提出假设:观点1:
 的量少不能氧化
的量少不能氧化
观点2:B中有未反应

为验证观点2,应进行的实验操作及现象是:取少量颜色变化前的B中溶液于试管中
 溶液,一段时间后,混合液逐渐变成红棕色,此时发生反应的离子方程式
溶液,一段时间后,混合液逐渐变成红棕色,此时发生反应的离子方程式(6)通过上述全部实验,得出结论:
 、
、 、
、 氧化性由强到弱的顺序是
氧化性由强到弱的顺序是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某小组同学学习了氧化还原反应的知识后,欲探究H2O2的性质:
【预测】
(1)聚焦H2O2中的核心元素O,预测H2O2既具有氧化性,也具有还原性,理由是_______ 。
【实验和观察】
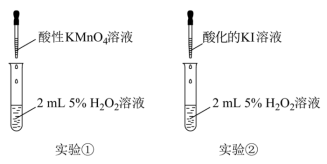
(2)实验①利用了酸性高锰酸钾的_______ 性,该实验中,证明KMnO4溶液与H2O2发生了反应的现象除了溶液紫色褪去外,还有_______ 。
(3)实验②是为了验证H2O2的_______ 性,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式,并用单线桥法表示电子转移的方向和数目_______ (已知:淀粉溶液遇I2会变蓝)。
【结论】以上实验可得出的结论是:H2O2既具有氧化性,也具有还原性。
(4)该实验也能说明H2O2、KMnO4和I2三者的氧化性由强到弱的顺序为_______ 。
【预测】
(1)聚焦H2O2中的核心元素O,预测H2O2既具有氧化性,也具有还原性,理由是
【实验和观察】

(2)实验①利用了酸性高锰酸钾的
(3)实验②是为了验证H2O2的
【结论】以上实验可得出的结论是:H2O2既具有氧化性,也具有还原性。
(4)该实验也能说明H2O2、KMnO4和I2三者的氧化性由强到弱的顺序为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】由工业级碳酸锂(含有少量碳酸镁等杂质)制备高纯碳酸锂。实验过程如下:

已知在不同温度下蒸发分解碳酸锂的产率与溶解度关系如图:

 以下,随温度升高,碳酸锂产率升高的原因可能是
以下,随温度升高,碳酸锂产率升高的原因可能是_______ 。

已知在不同温度下蒸发分解碳酸锂的产率与溶解度关系如图:

 以下,随温度升高,碳酸锂产率升高的原因可能是
以下,随温度升高,碳酸锂产率升高的原因可能是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某兴趣小组利用废铜屑(含铜、铝等)制备CuSO4·5H2O晶体,制备流程如图:

(1)“溶解Ⅰ”过程中所用试剂X为___ 。(填写试剂名称)
(2)“溶解Ⅱ”发生反应的离子方程式为___ 。
(3)“操作X”包括___ 、过滤、无水乙醇洗涤、低温干燥。
(4)某种杀菌剂中含CuSO4和Cu(OH)2,为测定其组成,兴趣小组设计如下实验:取一定量的杀菌剂,将其溶于足量的稀盐酸中,然后向其中加入足量的BaCl2溶液,过滤干燥后得白色固体2.33g。然后向滤液中滴加1.00mol·L-1的Na2H2Y(EDTA)溶液,反应至终点时消耗Na2H2Y溶液30.00 mL(离子方程式为Cu2++H2Y2-=CuY2-+2H+)。
①由准确称量后的EDTA固体配制100mL1.00mol·L-1的EDTA溶液所需的玻璃仪器除烧杯、胶头滴管外还有___ 。
②通过计算确定杀菌剂中CuSO4和Cu(OH)2的物质的量之比___ (写出计算过程)。

(1)“溶解Ⅰ”过程中所用试剂X为
(2)“溶解Ⅱ”发生反应的离子方程式为
(3)“操作X”包括
(4)某种杀菌剂中含CuSO4和Cu(OH)2,为测定其组成,兴趣小组设计如下实验:取一定量的杀菌剂,将其溶于足量的稀盐酸中,然后向其中加入足量的BaCl2溶液,过滤干燥后得白色固体2.33g。然后向滤液中滴加1.00mol·L-1的Na2H2Y(EDTA)溶液,反应至终点时消耗Na2H2Y溶液30.00 mL(离子方程式为Cu2++H2Y2-=CuY2-+2H+)。
①由准确称量后的EDTA固体配制100mL1.00mol·L-1的EDTA溶液所需的玻璃仪器除烧杯、胶头滴管外还有
②通过计算确定杀菌剂中CuSO4和Cu(OH)2的物质的量之比
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】我省自贡盛产食盐,人类与食盐关系密切,食盐在老百姓生活和现代社会的工农业生产中均有重要作用,没有食盐的生活是不可以想象的。粗盐中含有Ca2+、Mg2+、SO42-以及泥沙等杂质,
(1)为了除去粗盐中的泥沙,可采用的实验操作方法的名称是____ 、____
(2)为了除去可溶性杂质,可以按以下实验步骤进行提纯:①加过量BaCl2溶液;②加过量NaOH溶液;③加过量Na2CO3溶液;④过滤;⑤加适量盐酸。
其中,在步骤③中涉及的离子反应方程式有______ ; ________ 。
(3)含碘食盐往往加入KIO3,为了检验实验中是否含KIO3,可以用以下反应进行:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O为了从反应后的溶液中提取得到纯净的I2,可采用的实验操作方法的名称是______ 、______ 、___ 。
(1)为了除去粗盐中的泥沙,可采用的实验操作方法的名称是
(2)为了除去可溶性杂质,可以按以下实验步骤进行提纯:①加过量BaCl2溶液;②加过量NaOH溶液;③加过量Na2CO3溶液;④过滤;⑤加适量盐酸。
其中,在步骤③中涉及的离子反应方程式有
(3)含碘食盐往往加入KIO3,为了检验实验中是否含KIO3,可以用以下反应进行:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O为了从反应后的溶液中提取得到纯净的I2,可采用的实验操作方法的名称是
您最近一年使用:0次



