请回答下列问题:
(1)在标准状况下,①4gH2②11.2LO2③1 molH2O中,④9.03×1023个HCl分子,所含原子数最多的是__________ (填序号,下同),质量最大的是________ 。
(2)标准状况下,密度为0.75g·L-1的 NH3与CH4组成的混合气体中,NH3的体积分数为____________ 。
(3)某混合溶液中含有Na+、Mg2+、Cl-、SO 四种离子、若Na+、 Mg2+、Cl-的物质的量浓度依次为0.2 mol/L、0.25 mol/L、 0.4 mol/L,则c(SO
四种离子、若Na+、 Mg2+、Cl-的物质的量浓度依次为0.2 mol/L、0.25 mol/L、 0.4 mol/L,则c(SO )为
)为____________ 。
(4)使相同物质的量浓度的NaCl、MgCl2、AlCl3溶液中的Cl-完全沉淀时,若消耗相同物质的量浓度的AgNO3溶液的体积之比为3:2:1,则上述三种溶液的体积之比为_____________ 。
(1)在标准状况下,①4gH2②11.2LO2③1 molH2O中,④9.03×1023个HCl分子,所含原子数最多的是
(2)标准状况下,密度为0.75g·L-1的 NH3与CH4组成的混合气体中,NH3的体积分数为
(3)某混合溶液中含有Na+、Mg2+、Cl-、SO
 四种离子、若Na+、 Mg2+、Cl-的物质的量浓度依次为0.2 mol/L、0.25 mol/L、 0.4 mol/L,则c(SO
四种离子、若Na+、 Mg2+、Cl-的物质的量浓度依次为0.2 mol/L、0.25 mol/L、 0.4 mol/L,则c(SO )为
)为(4)使相同物质的量浓度的NaCl、MgCl2、AlCl3溶液中的Cl-完全沉淀时,若消耗相同物质的量浓度的AgNO3溶液的体积之比为3:2:1,则上述三种溶液的体积之比为
20-21高一上·江西南昌·期中 查看更多[1]
(已下线)【南昌新东方】7. 2020 高一上 南昌一中 期中 刘惠文 余贞梅
更新时间:2020-12-05 21:52:24
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】运用已学知识完成下列计算:
(1)17gNH3共有______ mol原子,0.1molH2S共有_____ 个氢原子;同质量的NH3和H2S中分子个数比为_______ 。
(2)在标准状况下,1.7g氨气所占的体积为_____ L,它与标准状况下_____ L的硫化氢(H2S)含有相同数目的氢原子。
(3)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg∙mol-1。若阿伏加 德罗常数用NA表示,则该气体的物质的量为_____ mol,该气体所含原子总数为______ 个,在标准状况下该气体的体积为________ L。若该气体不与水反应,将其溶于1L水中,所得溶液中溶质的质量分数为_________ 。
(1)17gNH3共有
(2)在标准状况下,1.7g氨气所占的体积为
(3)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg∙mol-1。若阿伏加 德罗常数用NA表示,则该气体的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在干燥烧瓶中用向上排空气法收集氯化氢,由于空气不可能排净,所以瓶内气体对氢气的相对密度为17,将此瓶气体倒置于水槽中(氯化氢极易溶于水),烧瓶内液面上升的体积占烧瓶总体积的___________ (填分数) ,假设溶质不向烧瓶外扩散,则所得盐酸中氯化氢的物质的量浓度为_________ mol/L(假设在标准状况下)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)2mol水中含有_______ mol氢原子。
(2)在0. 5molNa2SO4中含有Na+的数目是_______ 个。
(3)标准状况下,11. 2L氖气中含分子的物质的量_______ mol。
(4)11. 2gFe与足量的稀硫酸反应得到氢气在标准状况下的体积是_______ L。
(5)含0. 4molAl3+的Al2(SO4)3中所含SO 的物质的量是
的物质的量是_______ mol。
(6)已知3.01×1023个X气体分子的质量为32g,则X气体的摩尔质量_______ 。
(7)9. 8g硫酸溶解在水中配成100mL溶液,则H+的物质的量浓度_______ 。
(1)2mol水中含有
(2)在0. 5molNa2SO4中含有Na+的数目是
(3)标准状况下,11. 2L氖气中含分子的物质的量
(4)11. 2gFe与足量的稀硫酸反应得到氢气在标准状况下的体积是
(5)含0. 4molAl3+的Al2(SO4)3中所含SO
 的物质的量是
的物质的量是(6)已知3.01×1023个X气体分子的质量为32g,则X气体的摩尔质量
(7)9. 8g硫酸溶解在水中配成100mL溶液,则H+的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】有一定质量的镁铝合金,将其平均分成两份。第一份加入到100mL盐酸(密度为1.10g/mL)中,恰好完全反应,得到气体4.48L(标准状况);第二份加入到足量NaOH溶液中,得到气体3.36L(标准状况)。求:①原镁铝合金中镁的质量是多少____ ②盐酸的质量分数是多少_______
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】计算:(1)22gCO2的物质的量是__ mol;在标准状况下的体积是__ L。
(2)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是_______ ,X的相对原子质量是_______ 。
(3)2molOH-含有的质子数为_______ 个,电子数为_______ 个。
(4)现有0.27kg的质量分数为10%的CuCl2溶液,则溶液中CuCl2物质的量为_______ ;Cl-的物质的量为_______ 。
(5)100mL硫酸钠溶液中n(Na+)=0.2mol,则其中c( )=
)=_______ 。
(2)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是
(3)2molOH-含有的质子数为
(4)现有0.27kg的质量分数为10%的CuCl2溶液,则溶液中CuCl2物质的量为
(5)100mL硫酸钠溶液中n(Na+)=0.2mol,则其中c(
 )=
)=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】将11.5 g钠投入到89 g水中(足量),充分反应后所得溶液的密度为1.25 g·cm-3。
计算:(1)生成H2的体积(标准状况下)_______ 。
(2)所得溶液中溶质的物质的量浓度为多少________ ?
计算:(1)生成H2的体积(标准状况下)
(2)所得溶液中溶质的物质的量浓度为多少
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】通过计算填写下列内容:
(1)在标准状况下,6.72L CO的物质的量为_______ ,质量为_______ 。
(2)在标准状况下,23g C2H5OH的物质的量为_______ ,氢原子数目为_______ 。
(3)100mLAl2(SO4)3 和MgSO4的混合溶液中,含有Mg2+ 0.24g, SO 的物质的量浓度为1mol/L,则Al3+的物质的量浓度为
的物质的量浓度为1mol/L,则Al3+的物质的量浓度为_______ mol/L,加水稀释至1L后,MgSO4的物质的量浓度为_______ mol/L。
(1)在标准状况下,6.72L CO的物质的量为
(2)在标准状况下,23g C2H5OH的物质的量为
(3)100mLAl2(SO4)3 和MgSO4的混合溶液中,含有Mg2+ 0.24g, SO
 的物质的量浓度为1mol/L,则Al3+的物质的量浓度为
的物质的量浓度为1mol/L,则Al3+的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】CO2和O3组成的混合气体的质量为14.0g,其中碳原子与氧原子的物质的量之比是1:8。计算:
①该混合气体中CO2 的物质的量是______ ?
②标准状况下,该混合气体的体积是______ ?
③该混合气体的平均摩尔质量是______ ?
①该混合气体中CO2 的物质的量是
②标准状况下,该混合气体的体积是
③该混合气体的平均摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】硫化氢与浓硫酸发生如下反应:H2S+H2SO4(浓)→S↓+SO2↑+2H2O加热条件下,单质硫与浓硫酸又会发生如下反应:S+2H2SO4(浓) 3SO2↑+2H2O
3SO2↑+2H2O
计算:
(1)若98%浓硫酸可表示为H2SO4•aH2O,则a=__ ;若要把该浓硫酸转化为H2SO4•H2O,则98%浓硫酸与加入水的质量比为_____ 。
(2)一定条件下,将0.1mol H2S气体通入足量浓硫酸中,生成b mol SO2,则 b的取值范围是_______ 。
(3)在50mL、4.0mol/L的NaOH溶液中,通入H2S气体并充分反应,然后,小心蒸发,得到不含结晶水的白色固体.通入H2S的物质的量为x mol,生成的白色固体的质量为7.9g,通过计算确定白色固体的可能成分及每种成分的质量(结果保留一位小数)_______ 。
 3SO2↑+2H2O
3SO2↑+2H2O计算:
(1)若98%浓硫酸可表示为H2SO4•aH2O,则a=
(2)一定条件下,将0.1mol H2S气体通入足量浓硫酸中,生成b mol SO2,则 b的取值范围是
(3)在50mL、4.0mol/L的NaOH溶液中,通入H2S气体并充分反应,然后,小心蒸发,得到不含结晶水的白色固体.通入H2S的物质的量为x mol,生成的白色固体的质量为7.9g,通过计算确定白色固体的可能成分及每种成分的质量(结果保留一位小数)
您最近一年使用:0次
【推荐3】开展“三废”综合治理,是防治工业“三废”污染,搞好环境保护的重要途径之一。其中常用方法是将“三废”中有毒有害物转化为无害的物质或有用的产品。
(1)硝酸工业尾气中氮氧化物(NO与NO2)是主要的大气污染物之一,可用氨氧混合气进行选择性催化还原处理。其主要反应原理:4NO + 4NH3 + O2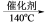 4N2 + 6H2O 6NO2 + 8NH3
4N2 + 6H2O 6NO2 + 8NH3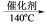 7N2 + 12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已折算至标准状况),其中NO与NO2物质的量比为4∶1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
7N2 + 12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已折算至标准状况),其中NO与NO2物质的量比为4∶1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
①氨氧混合气的平均相对分子质量为_______ (精确到0.01)。
②尾气中NO的含量为_______ mg/m3。
③要处理5m3的尾气,需要氨氧混合气的体积为_______ L。
(2)另一种处理氮氧化物的方法是用烧碱进行吸收,产物为NaNO2、NaNO3和H2O。现有含0.5mol氮氧化物的尾气,恰好被一定体积的25% NaOH溶液(密度1.28g/cm3)完全吸收。
①NaOH溶液的物质的量浓度为_______ mol/L,体积为__________ mL。
②已知反应后溶液中含有0.35mol NaNO2。若将尾气中NO与NO2的平均组成记为NOx,则x=_________ 。
(3)硫酸工业的废水中含质量分数4.9%的硫酸,加入质量分数22.2%的石灰乳,恰好使废水达到排放标准(pH=7),同时又得到副产品石膏(CaSO4·2H2O)。已知按此法处理后每小时可排放达标废水276.5吨,求每小时生产石膏的质量(忽略其他反应且不计过程中损耗)。_____________
(1)硝酸工业尾气中氮氧化物(NO与NO2)是主要的大气污染物之一,可用氨氧混合气进行选择性催化还原处理。其主要反应原理:4NO + 4NH3 + O2
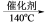 4N2 + 6H2O 6NO2 + 8NH3
4N2 + 6H2O 6NO2 + 8NH3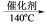 7N2 + 12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已折算至标准状况),其中NO与NO2物质的量比为4∶1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
7N2 + 12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已折算至标准状况),其中NO与NO2物质的量比为4∶1。设尾气中氮氧化物与氨氧混合气恰好完全反应。①氨氧混合气的平均相对分子质量为
②尾气中NO的含量为
③要处理5m3的尾气,需要氨氧混合气的体积为
(2)另一种处理氮氧化物的方法是用烧碱进行吸收,产物为NaNO2、NaNO3和H2O。现有含0.5mol氮氧化物的尾气,恰好被一定体积的25% NaOH溶液(密度1.28g/cm3)完全吸收。
①NaOH溶液的物质的量浓度为
②已知反应后溶液中含有0.35mol NaNO2。若将尾气中NO与NO2的平均组成记为NOx,则x=
(3)硫酸工业的废水中含质量分数4.9%的硫酸,加入质量分数22.2%的石灰乳,恰好使废水达到排放标准(pH=7),同时又得到副产品石膏(CaSO4·2H2O)。已知按此法处理后每小时可排放达标废水276.5吨,求每小时生产石膏的质量(忽略其他反应且不计过程中损耗)。
您最近一年使用:0次



