硬铝(因其主要成分,在此仅看作Al-Cu合金)常用于建筑装潢。1.18 g某种硬铝恰好与10 mL某浓度的硝酸完全反应,生成的混合气体(其中NO2与NO的体积比为2:1)再与448 mL氧气(标准状况)混合,恰好能被水完全吸收,通过计算并确定此种硬铝的化学式______________
更新时间:2021-01-05 19:13:54
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)写出实验室中制取氯气的离子方程式_______ 。
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①用化学方程式表示“84”消毒液的生成过程:_______ 。工业上用氯气与石灰乳反应制备漂白粉,其有效成分为_______ 。(填化学式)
②居家消毒时,不能将“84”消毒液与洁厕灵(有效成分为盐酸)混合使用,原因是_______ 。
③某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和 的混合溶液,经测定
的混合溶液,经测定 与
与 的离子个数比为1:3。该反应中,被氧化的Cl与被还原的Cl的质量之比为
的离子个数比为1:3。该反应中,被氧化的Cl与被还原的Cl的质量之比为_______ 。
(3)世界卫生组织将ClO2定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为 ,ClO2的消毒效率是氯气的
,ClO2的消毒效率是氯气的_______ 倍(保留两位小数)。
(1)写出实验室中制取氯气的离子方程式
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①用化学方程式表示“84”消毒液的生成过程:
②居家消毒时,不能将“84”消毒液与洁厕灵(有效成分为盐酸)混合使用,原因是
③某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和
 的混合溶液,经测定
的混合溶液,经测定 与
与 的离子个数比为1:3。该反应中,被氧化的Cl与被还原的Cl的质量之比为
的离子个数比为1:3。该反应中,被氧化的Cl与被还原的Cl的质量之比为(3)世界卫生组织将ClO2定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为
 ,ClO2的消毒效率是氯气的
,ClO2的消毒效率是氯气的
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将5.76 g铜粉投入30mL的浓HNO3中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,铜粉恰好与HNO3完全反应,共收集到标准状况下由NO2和NO组成的混合气体3. 36 L。
请回答下列问题:
(1)被还原的HNO3有___________ mol
(2)HNO3物质的量浓度为___________
(3)标准状况下,混合气体中NO的体积为___________ L。
请回答下列问题:
(1)被还原的HNO3有
(2)HNO3物质的量浓度为
(3)标准状况下,混合气体中NO的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
(1)NO的体积为_____________ L,NO2的体积为_____________ L。
(2)待产生的气体全部释放后,向溶液加入V mL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为_____________ mol/L。
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水_____________ g。
(1)NO的体积为
(2)待产生的气体全部释放后,向溶液加入V mL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】今年我国多个城市遭遇雾霾天气,这表明污染严重,空气质量下降。因此研究NO2、SO2、CO等大气污染气体的处理具有重要现实意义。
(1)NO2可用水吸收,相应的化学反应方程式为___________ 。
(2)利用反应6NO2+8NH3 7N2+12H2O也可处理NO2,当转移2.4 mol电子时,消耗的NO2在标准状况下的体积是
7N2+12H2O也可处理NO2,当转移2.4 mol电子时,消耗的NO2在标准状况下的体积是___________ L。
(3)3.2 g Cu与30 mL8 mol·L-1HNO3反应,硝酸的还原产物为NO,NO2,反应后溶液中所含H+为0.1 mol,则:
①溶液中n( )为
)为___________ mol。
②所生成的NO在标准状况下体积为___________ L。
(4)有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是3 mol·L-1和1 mol·L-1,取100 mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体的体积为___________ L(设反应中HNO3被还原成NO)。
(1)NO2可用水吸收,相应的化学反应方程式为
(2)利用反应6NO2+8NH3
 7N2+12H2O也可处理NO2,当转移2.4 mol电子时,消耗的NO2在标准状况下的体积是
7N2+12H2O也可处理NO2,当转移2.4 mol电子时,消耗的NO2在标准状况下的体积是(3)3.2 g Cu与30 mL8 mol·L-1HNO3反应,硝酸的还原产物为NO,NO2,反应后溶液中所含H+为0.1 mol,则:
①溶液中n(
 )为
)为②所生成的NO在标准状况下体积为
(4)有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是3 mol·L-1和1 mol·L-1,取100 mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,生成的气体为NO、 。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗
。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗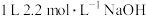 溶液和
溶液和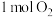 ,则生成的NO、
,则生成的NO、 的物质的量分别为
的物质的量分别为_______ 、_______ ,生成硫酸铜的物质的量为_________________ 。
 。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗
。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗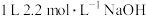 溶液和
溶液和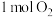 ,则生成的NO、
,则生成的NO、 的物质的量分别为
的物质的量分别为
您最近一年使用:0次

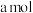 ,其中
,其中 的物质的量分数为b,将其全部投入
的物质的量分数为b,将其全部投入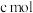 的稀硝酸中,加热使其充分反应(假设
的稀硝酸中,加热使其充分反应(假设 是唯一的还原产物)。
是唯一的还原产物)。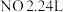 ,则反应转移电子的物质的量为
,则反应转移电子的物质的量为
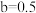 ,溶液中的
,溶液中的 与
与 的物质的量之比
的物质的量之比 ,标准状况下产生
,标准状况下产生 ,
,


