下表是元素周期表的一部分,所列的字母分别代表一种元素。
(1)元素h、c、d的非金属性由强到弱的顺序是____________ (填元素符号)。
(2)上述字母对应原子半径最大元素对应单质与d简单氢化物反应的离子方程式为____________ 。
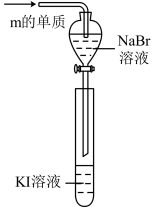
(3)利用如图装置来验证溴与碘的非金属性强弱,具体操作是先通入足量 的单质,充分反应后,观察到溶液变为橙黄色。将分液漏斗中液体滴入试管内,KI溶液变为棕黄色。判断该实验能否验证溴、碘的非金属性强弱并说明理由:
的单质,充分反应后,观察到溶液变为橙黄色。将分液漏斗中液体滴入试管内,KI溶液变为棕黄色。判断该实验能否验证溴、碘的非金属性强弱并说明理由:____________ 。
(4)元素d和e的简单离子半径更大的是____________ (填离子符号)。写出a2d的电子式:____________ 。
(5)推测原子序数为31的元素x在周期表中的位置____________ 。根据元素周期表推测x及其化合物的性质正确的是____________ (填字母)。
A.x为非金属元素B.最高价氧化物对应水化物酸性:x>m
C.x的单质可用于制半导体D.x的最高正价为+3
| a | ||||||||||
| c | d | |||||||||
| e | h | m | ||||||||
| i | ||||||||||
(2)上述字母对应原子半径最大元素对应单质与d简单氢化物反应的离子方程式为
(3)利用如图装置来验证溴与碘的非金属性强弱,具体操作是先通入足量
 的单质,充分反应后,观察到溶液变为橙黄色。将分液漏斗中液体滴入试管内,KI溶液变为棕黄色。判断该实验能否验证溴、碘的非金属性强弱并说明理由:
的单质,充分反应后,观察到溶液变为橙黄色。将分液漏斗中液体滴入试管内,KI溶液变为棕黄色。判断该实验能否验证溴、碘的非金属性强弱并说明理由:
(4)元素d和e的简单离子半径更大的是
(5)推测原子序数为31的元素x在周期表中的位置
A.x为非金属元素B.最高价氧化物对应水化物酸性:x>m
C.x的单质可用于制半导体D.x的最高正价为+3
20-21高一上·江苏南通·阶段练习 查看更多[4]
江苏省南京市第九中学2021-2022学年高一上学期12月月考化学试题江苏省南京市第九中学2020-2021学年高一上学期教学质量调研(三)化学试题(已下线)江苏省如皋市2020-2021学年高一上学期第三次月考化学试题江苏省南通市如皋中学2020-2021学年高一上学期教学质量调研(三)化学试题
更新时间:2021-01-01 21:15:54
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
针对元素①~⑩回答下列问题。
(1)元素①和②的单质化合形成的化合物 中,H元素的化合价为
中,H元素的化合价为___________ , 能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为
能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为___________ 。
(2)由元素①和⑥形成的一种物质是天然气的主要成分,其化学式为___________ ;元素⑥还可以和⑧形成一种三原子直线形分子,其结构式为___________ ;元素②的单质在元素⑦的单质中点燃生成淡黄色固体,将该固体投入硫酸亚铁溶液中,预测主要的反应现象是___________ 。
(3)元素③、⑧、⑨的简单离子中半径最大的是___________ ;(填离子符号),元素②和⑤的最高价氧化物对应的水化物之间可以发生反应,其反应的离子方程式为___________ 。
| 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ⑤ | ⑧ | ⑨ | ||||
| 4 | ③ | ④ | ⑩ | |||||
(1)元素①和②的单质化合形成的化合物
 中,H元素的化合价为
中,H元素的化合价为 能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为
能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为(2)由元素①和⑥形成的一种物质是天然气的主要成分,其化学式为
(3)元素③、⑧、⑨的简单离子中半径最大的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表列出了①~⑥6种元素在周期表中的位置,请根据要求回答问题。
(1)①~⑥6种元素中原子半径最大的是_______ 。(填元素符号)
(2)②的原子结构示意图是_______ 。
(3)由①和⑥两种元素组成的化合物的化学式是_______ ,其化学键的类型是_______ 。(填离子键、极性共价键或非极性共价键),用电子式表示该化合物的形成过程:_______ 。
(4)④和⑤两种元素的金属性强弱顺序是④_______ ⑤(填“<”或“>”)。
(5)写出⑤的单质溶于氢氧化钠溶液中的离子方程式_______ 。
族 周期 | IA | 0 | |||||||||||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | ||||||||||
| 2 | ② | ||||||||||||||||
| 3 | ③ | ④ | ⑤ | ⑥ | |||||||||||||
(2)②的原子结构示意图是
(3)由①和⑥两种元素组成的化合物的化学式是
(4)④和⑤两种元素的金属性强弱顺序是④
(5)写出⑤的单质溶于氢氧化钠溶液中的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空:
(1)表中,化学性质最不活泼的原子的原子结构示意图为_______________ 。
(2)表中,化学性质最活泼的非金属元素对应的单质是_________________ 。
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是____ ,碱性最强的是___________ 。
(4)写出元素⑥的氢化物的电子式__________
(5)写出⑤与氢氧化钠反应的化学方程式:______ 。
(6)比较③与④的化学性质,________ 更活泼,试用实验证明此现象(简述操作、现象和结论)____________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)表中,化学性质最活泼的非金属元素对应的单质是
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是
(4)写出元素⑥的氢化物的电子式
(5)写出⑤与氢氧化钠反应的化学方程式:
(6)比较③与④的化学性质,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,①~⑫分别代表12种元素,请回答:
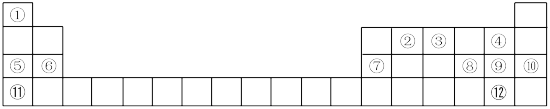
(1)写出12种元素中化学性质最不活泼的元素的原子结构示意图______________ 。
(2)⑪在元素周期表中的位置是____________________________ 。
(3)12种元素形成的单质中硬度最大的是________________ (填名称)。
(4)用电子式表示①与⑪形成化合物的过程_______________________ 。
(5)可以用来验证⑥⑦两种元素金属性强弱的实验是__________ (填字母序号)。
a 将在空气中放置已久的这两种元素的块状单质分别放入水中
b 将形状、大小相同的无氧化膜的这两种元素的单质分别和同浓度同体积的盐酸反应
c 将形状、大小相同的无氧化膜的这两种元素的单质分别和温度相同的热水作用,并滴入酚酞
d 比较这两种元素的氢化物的热稳定性
(6)⑧⑨两种元素的简单阴离子中还原性较强的是________ (填离子名称);用一个置换反应证明这一结论__________________________ (写化学方程式)。

(1)写出12种元素中化学性质最不活泼的元素的原子结构示意图
(2)⑪在元素周期表中的位置是
(3)12种元素形成的单质中硬度最大的是
(4)用电子式表示①与⑪形成化合物的过程
(5)可以用来验证⑥⑦两种元素金属性强弱的实验是
a 将在空气中放置已久的这两种元素的块状单质分别放入水中
b 将形状、大小相同的无氧化膜的这两种元素的单质分别和同浓度同体积的盐酸反应
c 将形状、大小相同的无氧化膜的这两种元素的单质分别和温度相同的热水作用,并滴入酚酞
d 比较这两种元素的氢化物的热稳定性
(6)⑧⑨两种元素的简单阴离子中还原性较强的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学课外活动小组为了验证元素化学性质递变规律,进行如下实验探究。
Ⅰ.探究1:验证同周期X、Y、Z三种元素金属性递变规律
通过实验验证三种元素金属性由强到弱是_____ ,则下列判断正确的是( )
A.原子序数:Y>Z>X B.原子的最外层电子数X>Y>Z
C.原子半径:Y>Z>X D.Y的最高价氧化物对应水化物的碱性最强
Ⅱ.探究2:验证氯元素的非金属性比硫元素的非金属性强,设计如下实验:

(1)装置A中盛放的试剂是_______ (填选项),化学反应方程式是_________ 。
A.Na2SO3溶液 B.Na2S溶液 C.Na2SO4溶液
(2)下列不能用于验证氯元素比硫元素非金属性强的依据为______ (填选项)。
A.HCl比H2S稳定
B.HClO氧化性比H2SO4强
C.HClO4酸性比H2SO4强
D.铁与Cl2反应生成FeCl3,而硫与铁反应生成FeS
(3)若要验证非金属性:Cl>I,装置A中加入淀粉碘化钾混合溶液,观察到装置A中溶液_______ 的现象,即可证明。用原子结构理论解释非金属性Cl>I的原因:同主族元素从上到下,________________ 。
Ⅰ.探究1:验证同周期X、Y、Z三种元素金属性递变规律
| 实验内容 | 实验现象 |
| 1、各取1.0g金属X和金属Z,分别加入到5mL水中 | 金属X与水反应比金属Z剧烈 |
| 2、各取1.0g的金属Z和金属Y(形状相同),分别加入到5mL1.0mol/L盐酸中。 | 金属Z与盐酸反应比金属Y剧烈 |
A.原子序数:Y>Z>X B.原子的最外层电子数X>Y>Z
C.原子半径:Y>Z>X D.Y的最高价氧化物对应水化物的碱性最强
Ⅱ.探究2:验证氯元素的非金属性比硫元素的非金属性强,设计如下实验:

(1)装置A中盛放的试剂是
A.Na2SO3溶液 B.Na2S溶液 C.Na2SO4溶液
(2)下列不能用于验证氯元素比硫元素非金属性强的依据为
A.HCl比H2S稳定
B.HClO氧化性比H2SO4强
C.HClO4酸性比H2SO4强
D.铁与Cl2反应生成FeCl3,而硫与铁反应生成FeS
(3)若要验证非金属性:Cl>I,装置A中加入淀粉碘化钾混合溶液,观察到装置A中溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
(1)利用如图装置可验证同主族元素非金属性的变化规律:装置D的作用为_____ 。

(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加_____ (填KMnO4或MnO2),写出B中反应的离子方程式_____ ,C中加淀粉碘化钾混合溶液,观察到C中溶液____ 的现象,即可证明;
(3)若要证明非金属性:C>Si,则在A中加_____ 、B中加_____ 、C中加Na2SiO3溶液,观察到C中溶液出现白色沉淀的现象,即可证明。写出C中发生反应的离子方程式____ ,此装置有不足之处,应在两个装置中间添加有_____ 溶液的洗气瓶。
(1)利用如图装置可验证同主族元素非金属性的变化规律:装置D的作用为

(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加
(3)若要证明非金属性:C>Si,则在A中加
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】表中列出了①~⑦七种元素在周期表中的位置。请按要求回答:
(1)七种元素中,原子半径最大的是_______ (填元素符号)。
(2)③与⑦的简单氢化物中,稳定性好的是(填化学式,下同)_______ ,沸点高的是_______ ,沸点高的原因是_______ 。
(3)元素②形成的一种氢化物常用作火箭燃料,则该物质的电子式为_______ 。
(4)元素④的最高价氧化物对应的水化物与元素⑤的最高价氧化物对应的水化物发生反应的离子方程式为_______ 。
(5)由①、②、③三种元素组成的离子化合物是_______ ,检验该化合物中阳离子的方法是_______ 。
(6)含有上述元素的物质间存在如图转化。

 所含的化学键类型是
所含的化学键类型是_______ ,实验室检验 是否为离子化合物的方法
是否为离子化合物的方法_______ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(2)③与⑦的简单氢化物中,稳定性好的是(填化学式,下同)
(3)元素②形成的一种氢化物常用作火箭燃料,则该物质的电子式为
(4)元素④的最高价氧化物对应的水化物与元素⑤的最高价氧化物对应的水化物发生反应的离子方程式为
(5)由①、②、③三种元素组成的离子化合物是
(6)含有上述元素的物质间存在如图转化。

 所含的化学键类型是
所含的化学键类型是 是否为离子化合物的方法
是否为离子化合物的方法
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如图是元素周期表的一部分,表中所列的数字分别代表某一种元素。
(1)⑧、⑨的最高价氧化物对应的水化物中,酸性较强的是______ (填化学式):⑥的金属单质与氢氧化钠溶液反应的化学方程式:______ 。
(2)元素②③⑤⑦⑨具有稳定结构的简单离子的半径由大到小的排序为______ (用相应的离子符号排序)。
(3)元素②的单质和⑦的单质在点燃条件下化合形成一种淡黄色的固体,请写出这种淡黄色固体与水反应的化学方程式:______ ;此反应中的氧化剂的阴阳离子比为______ ,其电子式为______ ,含有的化学键类型有______ ,属于______ (“离子”或“共价”)化合物。
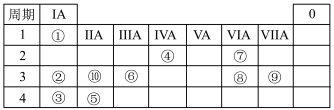
(1)⑧、⑨的最高价氧化物对应的水化物中,酸性较强的是
(2)元素②③⑤⑦⑨具有稳定结构的简单离子的半径由大到小的排序为
(3)元素②的单质和⑦的单质在点燃条件下化合形成一种淡黄色的固体,请写出这种淡黄色固体与水反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】 晶体具有优异的非线性光学性能。我国科学工作者制备的超大
晶体具有优异的非线性光学性能。我国科学工作者制备的超大 晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
(1)组成 晶体的四种原子,原子半径由大到小的顺序是
晶体的四种原子,原子半径由大到小的顺序是___________ 。四种组成元素各自所能形成的简单离子中,核外电子排布相同的是___________ (填离子符号)。
(2)已知磷酸的结构式为: ,P原子的价层电子排布式是
,P原子的价层电子排布式是___________ ,在磷酸分子中P原子的价层电子对数是___________ ,杂化轨道类型为___________ , 的空间构型是
的空间构型是___________ 。
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为___________ 。
(4)分子中的大 键可用
键可用 表示,其中m表示形成大
表示,其中m表示形成大 键的原子个数,n表示参与形成大
键的原子个数,n表示参与形成大 键的电子个数,吡啶(
键的电子个数,吡啶( )类似于苯,则吡啶中大
)类似于苯,则吡啶中大 键表示为
键表示为___________ 。
(5)元素铜、镍、铁和钾都处于元素周期表的第四周期。
①以上四种元素处于第四周期第Ⅷ族的元素是___________ (填元素符号)。
②元素铜与镍的第二电离能分别为: ,
,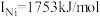 ,
,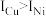 的原因是
的原因是___________ 。
③比较 和
和 稳定性较强的是
稳定性较强的是___________ 。(填离子符号)
 晶体具有优异的非线性光学性能。我国科学工作者制备的超大
晶体具有优异的非线性光学性能。我国科学工作者制备的超大 晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:(1)组成
 晶体的四种原子,原子半径由大到小的顺序是
晶体的四种原子,原子半径由大到小的顺序是(2)已知磷酸的结构式为:
 ,P原子的价层电子排布式是
,P原子的价层电子排布式是 的空间构型是
的空间构型是(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为(4)分子中的大
 键可用
键可用 表示,其中m表示形成大
表示,其中m表示形成大 键的原子个数,n表示参与形成大
键的原子个数,n表示参与形成大 键的电子个数,吡啶(
键的电子个数,吡啶( )类似于苯,则吡啶中大
)类似于苯,则吡啶中大 键表示为
键表示为(5)元素铜、镍、铁和钾都处于元素周期表的第四周期。
①以上四种元素处于第四周期第Ⅷ族的元素是
②元素铜与镍的第二电离能分别为:
 ,
,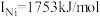 ,
,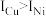 的原因是
的原因是③比较
 和
和 稳定性较强的是
稳定性较强的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】镁、钙、钾、溴、氟、硼等元素在每升海水中的含量都大于1 mg ,属于海水中的常量元素。
⑴镓与硼同主族,写出镓元素原子的价电子排布式_____________________ 。
⑵钾、钙、镓的第一电离能从大到小的顺序是_____________ 。
⑶比较氟化钠和溴化钠的熔点:氟化钠_______ 溴化钠(填“<”或“>”),分析其原因是______________ 。
⑷举出两例说明锂与镁具有相似性:①________________ 、②______________ ,这种相似性称为__________________ 。
⑸用价层电子对互斥理论推断BF3空间构型为______________ ,NF3分子中N原子的杂化轨道类型为_________ ;在NH3·BF3中接受孤对电子的原子是_________ 。
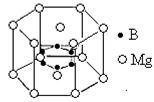
⑹2001年曾报道,硼镁化合物刷新了金属化合物超导温度的最高记录。该化合晶体结构中的晶胞如上图所示。镁原子间形成正六棱柱,且棱柱的上下底面还各有一个镁原子,六个硼原子位于棱柱内。则该化合物的化学式可表示为_______ 。
⑴镓与硼同主族,写出镓元素原子的价电子排布式
⑵钾、钙、镓的第一电离能从大到小的顺序是
⑶比较氟化钠和溴化钠的熔点:氟化钠
⑷举出两例说明锂与镁具有相似性:①
⑸用价层电子对互斥理论推断BF3空间构型为

⑹2001年曾报道,硼镁化合物刷新了金属化合物超导温度的最高记录。该化合晶体结构中的晶胞如上图所示。镁原子间形成正六棱柱,且棱柱的上下底面还各有一个镁原子,六个硼原子位于棱柱内。则该化合物的化学式可表示为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回答下列问题:
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子中,占据最高能级电子的电子云轮廓图形状为___________ 。
(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是___________ 。
(ii)离子半径:Li+___________ H-(填“>”“=”或“<”)。
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:
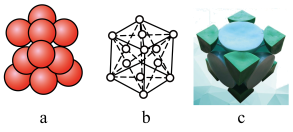
(i)晶胞中锂的配位数为___________ 。
(ii)若锂原子的半径为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为___________  (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是
(ii)离子半径:Li+
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:

(i)晶胞中锂的配位数为
(ii)若锂原子的半径为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为 (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】金属镓(Ga)应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。
(1)铝在元素周期表中的位置是_________________ 。
(2)GaAs是共价化合物,一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是_______________ (填字母)。
a.碱性:Ga (OH)3> Al (OH)3
b.非金属性:As>Ga
c.酸性:H3AsO4>H3AsO3
②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释 As 元素显负价的原因______________________________ 。
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 H3AsO4 和 Ga3+,写出该反应的化学方程式________________________________________ 。
(1)铝在元素周期表中的位置是
(2)GaAs是共价化合物,一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是
a.碱性:Ga (OH)3> Al (OH)3
b.非金属性:As>Ga
c.酸性:H3AsO4>H3AsO3
②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释 As 元素显负价的原因
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 H3AsO4 和 Ga3+,写出该反应的化学方程式
您最近一年使用:0次




