判断C的非金属性比Si的强,可依据的事实是
| A.CH4的热稳定性比SiH4的强 | B.金刚石的硬度比硅单质晶体的大 |
| C.常温下,CO2呈气态,SiO2呈固态 | D.CO2可溶于水,SiO2不溶于水 |
更新时间:2021-01-14 14:51:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列叙述能说明氯元素非金属性比硫元素强的是
①HCl的沸点比H2S高②HCl的酸性比H2S强③HCl的稳定性比H2S强④还原性:Cl-<S2-⑤HClO的酸性比H2SO4弱⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS⑦Cl2能与H2S反应生成S⑧在周期表中Cl处于S同周期的右侧
①HCl的沸点比H2S高②HCl的酸性比H2S强③HCl的稳定性比H2S强④还原性:Cl-<S2-⑤HClO的酸性比H2SO4弱⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS⑦Cl2能与H2S反应生成S⑧在周期表中Cl处于S同周期的右侧
| A.③④⑤⑦⑧ | B.③④⑥⑦⑧ | C.①③⑥⑦⑧ | D.①②③④⑤⑥⑦⑧ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图为短周期的一部分,Y原子最外层电子数是其电子层数的 2倍,下列说法正确的是
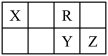

| A.Y的氢化物比 Z的氢化物稳定 |
| B.原子半径大小为Z>Y>R>X |
| C.Y、R形成的化合物 YR2能使酸性 KMnO4溶液褪色 |
| D.四种元素中最高价氧化物的水化物酸性最强的是 Y |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某陶瓷颗粒增强材料(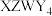 )由原子序数依次增大的X、Y、Z、W四种短周期主族元素组成,其中X与Y同周期,X原子电子层数是最外层电子数的2倍,且X与Z的最外电子数之和与W的最外层电子数相同,W的单质可用于制造太阳能电池板。下列说法错误的是
)由原子序数依次增大的X、Y、Z、W四种短周期主族元素组成,其中X与Y同周期,X原子电子层数是最外层电子数的2倍,且X与Z的最外电子数之和与W的最外层电子数相同,W的单质可用于制造太阳能电池板。下列说法错误的是
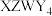 )由原子序数依次增大的X、Y、Z、W四种短周期主族元素组成,其中X与Y同周期,X原子电子层数是最外层电子数的2倍,且X与Z的最外电子数之和与W的最外层电子数相同,W的单质可用于制造太阳能电池板。下列说法错误的是
)由原子序数依次增大的X、Y、Z、W四种短周期主族元素组成,其中X与Y同周期,X原子电子层数是最外层电子数的2倍,且X与Z的最外电子数之和与W的最外层电子数相同,W的单质可用于制造太阳能电池板。下列说法错误的是A.简单离子半径: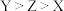 | B.最简单氢化物的热稳定性: |
| C.W、Y可形成共价晶体 | D.工业上电解Z、Y的化合物冶炼Z单质 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】短周期主族元素X、Y、Z、W的原子序数依次增大,X、W同主族,Y、Z同周期,X、Y、Z三种元素形成一种化合物M,25℃时0.1 mol/L的M溶液中c(OH-)/c(H+)=1.0×10-12,下列说法正确的是
| A.114号元素鈇(Fl)与Y在同一主族 |
| B.X分别与Z、W形成的化合物中,含化学键类型相同 |
| C.Z与X、W均可形成具有漂白性的化合物 |
| D.X、Y形成的化合物中只含有极性共价键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.H2O的沸点比H2S高,所以H2O比H2S更稳定 |
| B.碘升华和冰融化时需克服微粒间的作用力类型相同 |
| C.氯化氢溶于水电离产生氢离子和氯离子,故氯化氢是离子化合物 |
| D.NaHCO3受热分解的过程中,只有离子键被破坏 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】物质结构决定物质性质.下列性质差异与结构因素匹配错误的是
选项 | 性质差异 | 结构因素 |
A | 还原性:Na>Mg>Al | 核外电子排布 |
B | 沸点: (131℃)> (131℃)> (31.36℃) (31.36℃) | 分子间氢键 |
C | 稳定性: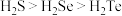 | 分子间作用力 |
D | 熔点:金刚石>碳化硅>晶体硅 | 共价键键能 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计与结论都正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 检验固体样品中是否含有 | 将固体样品加水溶解,滴入浓 溶液并加热,试管口放一张湿润的红色石蕊试纸 溶液并加热,试管口放一张湿润的红色石蕊试纸 | 湿润的红色石蕊试纸变蓝 | 样品中含有 |
| B | 探究铝与浓硫酸的钝化现象 | 室温下,将铝片直接放入浓硫酸中,一段时间后取出并用水洗净,放入 溶液 溶液 | 铝片表面未见紫红色固体生成 | 室温下浓硫酸能将铝片钝化 |
| C | 探究 、 、 元素非金属性的强弱 元素非金属性的强弱 | 向 溶液中滴加1滴酚酞,然后逐滴加入盐酸至红色褪去 溶液中滴加1滴酚酞,然后逐滴加入盐酸至红色褪去 | 混合液逐渐变成白色凝胶 | 非金属性: |
| D | 探究浓度与反应速率的关系 | 两支试管各盛 酸性高锰酸钾溶液,分别加入 酸性高锰酸钾溶液,分别加入 草酸溶液和 草酸溶液和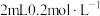 草酸溶液 草酸溶液 | 加入 草酸溶液的试管中,高锰酸钾溶液褪色更快 草酸溶液的试管中,高锰酸钾溶液褪色更快 | 反应物浓度越大,反应速率越快 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次

 为有色固体,
为有色固体, 难溶于水也不溶于稀硝酸
难溶于水也不溶于稀硝酸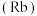 的燃烧产物比钠的燃烧产物更复杂
的燃烧产物比钠的燃烧产物更复杂 的酸性比
的酸性比 的酸性强
的酸性强

