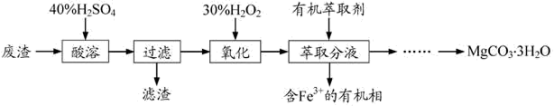
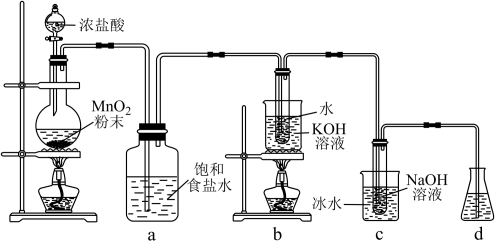
新冠肺炎疫情期间,环境消毒是极其关键的,常常喷洒“84”消毒液,其有效成分为NaClO。实验室利用下图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。
回答下列问题:
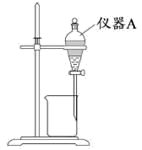
(1)盛放浓盐酸的仪器名称是_______ 。
(2)a的作用是_______ 。
(3)b中采用的加热方式是_______ ,c中发生反应的离子方程式是_______ 。
(4)d中可选用试剂_______ (填标号)。
A.Na2SO3溶液 B.NaCl溶液 C.NaOH溶液 D.稀H2SO4
(5)反应结束后,取出b中试管,经冷却、结晶、_______ 、_______ 及干燥,得到KClO3晶体。
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变,2号试管溶液变为棕色,可知该条件下NaClO的氧化能力_______ KClO3(填“大于”或“小于”)。
(7)已知某“84”消毒液瓶体部分标签如图所示,该“84”消毒液通常用水稀释100倍(体积之比)后使用。用水稀释后的溶液中c(Na+)=_______ mol/L。(保留到小数点后两位)

回答下列问题:
(1)盛放浓盐酸的仪器名称是
(2)a的作用是
(3)b中采用的加热方式是
(4)d中可选用试剂
A.Na2SO3溶液 B.NaCl溶液 C.NaOH溶液 D.稀H2SO4
(5)反应结束后,取出b中试管,经冷却、结晶、
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变,2号试管溶液变为棕色,可知该条件下NaClO的氧化能力
(7)已知某“84”消毒液瓶体部分标签如图所示,该“84”消毒液通常用水稀释100倍(体积之比)后使用。用水稀释后的溶液中c(Na+)=
84消毒液 有效成分:NaClO 规格:100mL 质量分数:25% 密度:1.19g/cm3 |
更新时间:2021-02-08 16:05:00
|
相似题推荐
【推荐1】利用 与
与 发生取代反应制取副产品盐酸的设想在工业上已成为现实,某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图所示。根据要求回答下列问题:
发生取代反应制取副产品盐酸的设想在工业上已成为现实,某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图所示。根据要求回答下列问题:
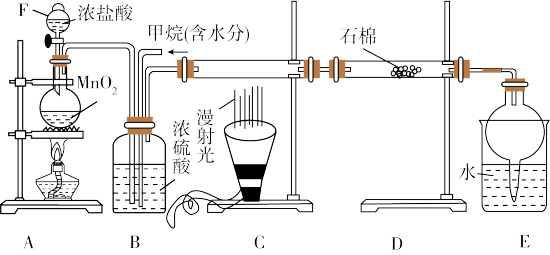
(1)实验室制取 的化学反应方程式为
的化学反应方程式为________ 。
(2)设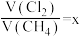 ,若理论上欲获得最多的HCl,则x的取值范围为
,若理论上欲获得最多的HCl,则x的取值范围为________ 。
(3)B装置有三种功能:①控制气体流速;②将气体混合均匀;③___________ 。
(4)D装置中的石棉上吸附着KI饱和溶液及KI粉末,其作用是________ 。
(5)E装置的作用是_______ (填字母)。
A.收集气体 B.吸收 C.防止倒吸 D.吸收HCl
C.防止倒吸 D.吸收HCl
(6)该装置还存在缺陷,原因是没有进行尾气处理,尾气的主要成分是______ (填字母)。
A.CH4 B.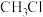 C.
C.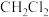 D.
D. E.
E.
 与
与 发生取代反应制取副产品盐酸的设想在工业上已成为现实,某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图所示。根据要求回答下列问题:
发生取代反应制取副产品盐酸的设想在工业上已成为现实,某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图所示。根据要求回答下列问题:
(1)实验室制取
 的化学反应方程式为
的化学反应方程式为(2)设
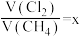 ,若理论上欲获得最多的HCl,则x的取值范围为
,若理论上欲获得最多的HCl,则x的取值范围为(3)B装置有三种功能:①控制气体流速;②将气体混合均匀;③
(4)D装置中的石棉上吸附着KI饱和溶液及KI粉末,其作用是
(5)E装置的作用是
A.收集气体 B.吸收
 C.防止倒吸 D.吸收HCl
C.防止倒吸 D.吸收HCl(6)该装置还存在缺陷,原因是没有进行尾气处理,尾气的主要成分是
A.CH4 B.
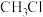 C.
C.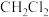 D.
D. E.
E.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】化学小组同学为研究氯气制备和氯水的成分及性质进行了如下实验。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。
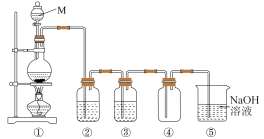
(1)M的名称是___________ ,①中反应的化学方程式是___________ 。
(2)③中存放的试剂是___________ 。(填“浓硫酸”或“饱和食盐水”)
(3)⑤中NaOH溶液的作用是___________ 。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。

(1)M的名称是
(2)③中存放的试剂是
(3)⑤中NaOH溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验。(夹持仪器已略去,气密性已检验)
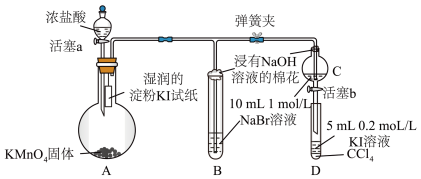
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.打开活塞b,将少量C中的溶液滴入D中,关闭活塞b,取下D振荡,静置后观察溶液颜色。
(1)A中产生黄绿色气体,该反应的离子方程式是(补全并配平):_________

(2)本实验中氯气的氧化性强于碘的实验现象是___________ 。
(3)C中溶液发生反应的离子方程式是___________ 。
(4)浸有NaOH溶液棉花可以吸收可能逸出的Cl2,相关反应的离子方程式为___________ 。
(5)为验证溴的氧化性强于碘,过程Ⅳ能观察到的现象是D中溶液变为棕黄色,且比C中溶液颜色___________ (填“深”或“浅”)。
(6)过程Ⅲ实验的目的是___________ 。
(7)结合元素周期律推断氯、溴、碘三种元素最高价氧化物对应水化物酸性最强的是___________ (填化学式)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.打开活塞b,将少量C中的溶液滴入D中,关闭活塞b,取下D振荡,静置后观察溶液颜色。
(1)A中产生黄绿色气体,该反应的离子方程式是(补全并配平):

(2)本实验中氯气的氧化性强于碘的实验现象是
(3)C中溶液发生反应的离子方程式是
(4)浸有NaOH溶液棉花可以吸收可能逸出的Cl2,相关反应的离子方程式为
(5)为验证溴的氧化性强于碘,过程Ⅳ能观察到的现象是D中溶液变为棕黄色,且比C中溶液颜色
(6)过程Ⅲ实验的目的是
(7)结合元素周期律推断氯、溴、碘三种元素最高价氧化物对应水化物酸性最强的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】“84消毒液”是常用的含氯消毒剂。
(1)“84消毒液”中的有效成分为_______ (填写化学式,下同),我们可用氯气与氢氧化钠反应制备“84消毒液”,请写出该反应的离子方程式________ ,该反应的氧化剂为_____ ,每消耗120克氢氧化钠,转移电子数为______ (阿伏伽德罗常数为NA)。
(2)某同学设计实验探究84消毒液的漂白性。
Ⅰ.在2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。
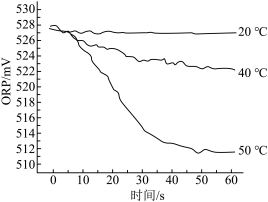
已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是为______ 。
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是______ 。
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。取含次氯酸钠14.9g/L的84消毒液lmL,加水稀释至100mL,稀释后的溶液中,次氯酸钠的物质的量浓度为____ mol/L。
(1)“84消毒液”中的有效成分为
(2)某同学设计实验探究84消毒液的漂白性。
Ⅰ.在2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。

已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是为
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。取含次氯酸钠14.9g/L的84消毒液lmL,加水稀释至100mL,稀释后的溶液中,次氯酸钠的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某学习小组用MnO2和浓盐酸共热制取氯气,再用氯气与潮湿的消石灰反应制取漂白粉(这是一个放热反应)。
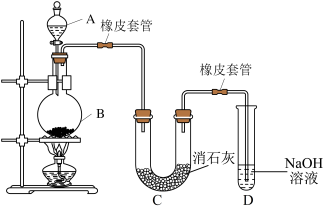
(1)圆底烧瓶内发生反应的化学方程式为_______ ;
(2)漂粉精在空气中起漂白作用的原理是_______ (用化学方程式表示)。
(3)此实验Ca(ClO)2产率太低。经分析发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是_______ 。
②试判断另一个副反应:_______ (用化学方程式表示)。

(1)圆底烧瓶内发生反应的化学方程式为
(2)漂粉精在空气中起漂白作用的原理是
(3)此实验Ca(ClO)2产率太低。经分析发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②试判断另一个副反应:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某化学实验小组设计下图装置制备氯气,图中涉及气体发生、除杂、干燥、收集及尾气处理装置。
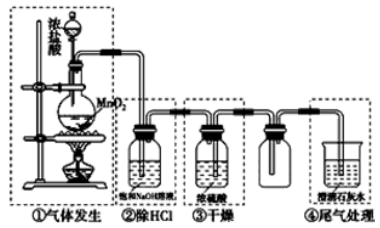
(1)上述装置中,错误的是_______(选填字母)。
(2)写出装置①中发生反应的化学方程式_______ 。该反应中,氧化剂是_______ ,HCl体现出的性质是_______ 。
(3)化学实验中常用_______ 试纸检验 是否收集满。如果有
是否收集满。如果有 产生,可观察到
产生,可观察到_______ ,反应方程式_______ 。
(4)ICl的性质与 类似,写出ICl与水反应的化学方程式是
类似,写出ICl与水反应的化学方程式是_______ 。
(5)工业上用氯气生产漂白粉,漂白粉的主要成分是,漂白粉溶于水后,遇到空气中的 ,即产生漂白、杀菌作用,漂白粉露置在空气中容易失效的原因用化学方程式表示
,即产生漂白、杀菌作用,漂白粉露置在空气中容易失效的原因用化学方程式表示_______ 。

(1)上述装置中,错误的是_______(选填字母)。
| A.①②④ | B.①②③ | C.①③④ | D.②③④ |
(3)化学实验中常用
 是否收集满。如果有
是否收集满。如果有 产生,可观察到
产生,可观察到(4)ICl的性质与
 类似,写出ICl与水反应的化学方程式是
类似,写出ICl与水反应的化学方程式是(5)工业上用氯气生产漂白粉,漂白粉的主要成分是,漂白粉溶于水后,遇到空气中的
 ,即产生漂白、杀菌作用,漂白粉露置在空气中容易失效的原因用化学方程式表示
,即产生漂白、杀菌作用,漂白粉露置在空气中容易失效的原因用化学方程式表示
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】正丁醚常用作有机反应的溶剂。实验室制备正丁醚的主要实验装置如图:

已知:I.2CH3CH2CH2CH2OH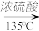 (CH3CH2CH2CH2)2O+H2O
(CH3CH2CH2CH2)2O+H2O
II.反应物和产物的相关数据如表:
III.制备流程如下:

请回答:
(1)仪器B的名称为_______ ,出水口是_______ (填“a”或‘‘b”)。
(2)浓硫酸和正丁醇添加到A中的先后顺序为_______ 。
(3)步骤②依次用水、NaOH溶液和水洗涤,第一次水洗的目的是_______ ,水层应从分液漏斗的_______ (填“上”或“下”)口分离出。
(4)步骤④中,加热蒸馏时应收集_______(填选项字母)左右的馏分。
(5)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至左侧支管口时,上层液体会流回A,下层液体可从下部放出。分水器中上层液体的主要成分为_______ (写物质名称),分水器的作用是_______ 。
(6)本实验所得正丁醚的产率为_______ 。

已知:I.2CH3CH2CH2CH2OH
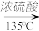 (CH3CH2CH2CH2)2O+H2O
(CH3CH2CH2CH2)2O+H2OII.反应物和产物的相关数据如表:
| 相对分子质量 | 沸点/℃ | 密度(g/cm3) | 水中溶解性 | |
| 正丁醇 | 74 | 117.2 | 0.819 | 微溶 |
| 正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |

请回答:
(1)仪器B的名称为
(2)浓硫酸和正丁醇添加到A中的先后顺序为
(3)步骤②依次用水、NaOH溶液和水洗涤,第一次水洗的目的是
(4)步骤④中,加热蒸馏时应收集_______(填选项字母)左右的馏分。
| A.100℃ | B.117℃ | C.135℃ | D.142℃ |
(6)本实验所得正丁醚的产率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】电解质在溶液中的反应实质上是离子之间的反应离子。请回答以下问题:
I.有四种物质:①氧化铁②盐酸③碳酸氢钠④氢氧化钠
(1)写出其中盐的电离方程式___________ 。
(2)上述物质中有一种与其它三种物质均能反应,此物质是___________ (填序号)。
(3)写出③④两种溶液反应的离子方程式___________ 。
Ⅱ.某溶液中含有 、
、 、
、 ,现用NaOH溶液、盐酸和
,现用NaOH溶液、盐酸和 溶液将这三种离子逐一沉淀分离。其流程图如下(已知溶液2为无色溶液)
溶液将这三种离子逐一沉淀分离。其流程图如下(已知溶液2为无色溶液)

(4)分离得到沉淀1和溶液1的实验中,使用到的玻璃仪器有烧杯、漏斗和___________ 。
(5)沉淀3的化学式:___________ 。
(6)“溶液 ”生成沉淀2的离子方程式为:
”生成沉淀2的离子方程式为:___________ 。
I.有四种物质:①氧化铁②盐酸③碳酸氢钠④氢氧化钠
(1)写出其中盐的电离方程式
(2)上述物质中有一种与其它三种物质均能反应,此物质是
(3)写出③④两种溶液反应的离子方程式
Ⅱ.某溶液中含有
 、
、 、
、 ,现用NaOH溶液、盐酸和
,现用NaOH溶液、盐酸和 溶液将这三种离子逐一沉淀分离。其流程图如下(已知溶液2为无色溶液)
溶液将这三种离子逐一沉淀分离。其流程图如下(已知溶液2为无色溶液)
(4)分离得到沉淀1和溶液1的实验中,使用到的玻璃仪器有烧杯、漏斗和
(5)沉淀3的化学式:
(6)“溶液
 ”生成沉淀2的离子方程式为:
”生成沉淀2的离子方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】硫酸肼(N2H4·H2SO4)又名硫酸联氨,在医药、染料、农业上用途广泛。回答下列问题:
已知:①Cl2与NaOH反应为放热反应,Cl2与热的NaOH溶液反应会生成NaClO3;
②利用尿素法生产水合肼的原理为CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl;
③硫酸肼的制备原理为N2H4·H2O+H2SO4=N2H4·H2SO4+H2O。
I.制备NaClO溶液。实验制备装置如图1所示:
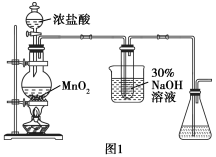
(1)图1装置试管内发生主要反应的化学方程式为_______ 。
(2)配制质量分数为30%的NaOH溶液时,所需玻璃仪器除量筒外还有_______ 。
II.尿素法生产水合肼的装置如图2所示:
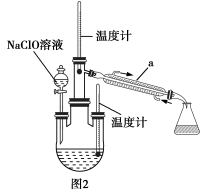
(3)把I制得的NaClO溶液注入到图2装置中的分液漏斗中,三颈烧瓶内装入一定量的尿素和NaOH溶液(物质的量之比1∶2.30),a的名称为_______ ,采用低温(低于20℃)反应,降温的方式可采用_______ ,温度高时水合肼会被氧化成无色无味的气体,该气体在标准状况下的密度为1.25g·L−1,其反应化学方程式为_______ 。反应结束后,急速升温至108℃开始回流5min,收集108~114℃馏分。
(4)测定馏分中水合肼的含量。称取馏分6.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.30mol·L−1的碘的标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。
①判断滴定终点的方法_______ 。
②实验测得消耗I2溶液的体积平均值为20.00mL,馏分中水合肼(N2H4·H2O)的质量分数为_______ 。
III.硫酸肼的制备
(5)将水合肼转移到烧杯中,滴加一定质量98%的浓硫酸,滴加时间控制在1h左右,温度60℃以下。冷藏沉降2h,得硫酸肼沉淀。抽滤,用无水乙醇洗涤,干燥,得白色硫酸肼固体。用无水乙醇而不用水洗涤的原因是_______ 。
已知:①Cl2与NaOH反应为放热反应,Cl2与热的NaOH溶液反应会生成NaClO3;
②利用尿素法生产水合肼的原理为CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl;
③硫酸肼的制备原理为N2H4·H2O+H2SO4=N2H4·H2SO4+H2O。
I.制备NaClO溶液。实验制备装置如图1所示:

(1)图1装置试管内发生主要反应的化学方程式为
(2)配制质量分数为30%的NaOH溶液时,所需玻璃仪器除量筒外还有
II.尿素法生产水合肼的装置如图2所示:

(3)把I制得的NaClO溶液注入到图2装置中的分液漏斗中,三颈烧瓶内装入一定量的尿素和NaOH溶液(物质的量之比1∶2.30),a的名称为
(4)测定馏分中水合肼的含量。称取馏分6.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.30mol·L−1的碘的标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。
①判断滴定终点的方法
②实验测得消耗I2溶液的体积平均值为20.00mL,馏分中水合肼(N2H4·H2O)的质量分数为
III.硫酸肼的制备
(5)将水合肼转移到烧杯中,滴加一定质量98%的浓硫酸,滴加时间控制在1h左右,温度60℃以下。冷藏沉降2h,得硫酸肼沉淀。抽滤,用无水乙醇洗涤,干燥,得白色硫酸肼固体。用无水乙醇而不用水洗涤的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某工厂排出的废水中含有大量的Fe2+、Cu2+和SO42-。
Ⅰ.某校研究性学习小组设计下图工艺流程以回收铜和硫酸亚铁。请回答:
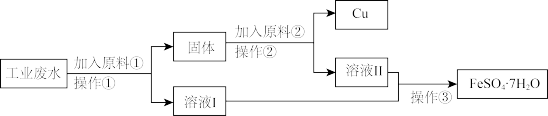
(1)加入原料①反应的离子方程式为_____
(2)操作①中用到的玻璃仪器是_____ (填序号)。
a.烧杯 b.漏斗 C.玻璃棒 d.酒精灯
(3)加入原料②的名称为_____
Ⅱ.回收的铜可用于制备胆矾(CuSO4•5H2O)。将铜和一定浓度稀硫酸混合后在加热的情况下通入氧气,发生如下反应:2Cu+2H2SO4+O2═2CuSO4+2H2O,制得硫酸铜溶液后,经过蒸发浓缩冷却结晶、过滤可得胆矾
(1)请分析2Cu+2H2SO4+O2 2CuSO4+2H2O反应中,氧化剂是
2CuSO4+2H2O反应中,氧化剂是_____ 氧化产物是_____ (填化学式)
(2)用双线桥标出反应中电子转移的方向和数目______________________
(3)若有147gH2SO4参与反应,则反应转移的电子数目为_____
Ⅰ.某校研究性学习小组设计下图工艺流程以回收铜和硫酸亚铁。请回答:

(1)加入原料①反应的离子方程式为
(2)操作①中用到的玻璃仪器是
a.烧杯 b.漏斗 C.玻璃棒 d.酒精灯
(3)加入原料②的名称为
Ⅱ.回收的铜可用于制备胆矾(CuSO4•5H2O)。将铜和一定浓度稀硫酸混合后在加热的情况下通入氧气,发生如下反应:2Cu+2H2SO4+O2═2CuSO4+2H2O,制得硫酸铜溶液后,经过蒸发浓缩冷却结晶、过滤可得胆矾
(1)请分析2Cu+2H2SO4+O2
 2CuSO4+2H2O反应中,氧化剂是
2CuSO4+2H2O反应中,氧化剂是(2)用双线桥标出反应中电子转移的方向和数目
(3)若有147gH2SO4参与反应,则反应转移的电子数目为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】纳米铁可用作特殊的催化剂,以FeSO4饱和溶液为原料制取纳米铁的工艺流程如图所示。
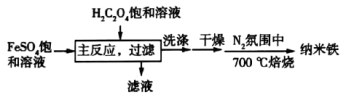
已知:主反应在80℃左右条件下进行,直至得到黄色(FeC2O4•2H2O)沉淀。
(1)实验室中FeSO4溶液在保存时需要加入少量铁粉,原因是___ 。
(2)写出进行“主反应”的化学方程式___ ,为了保证主反应的顺利进行,可以采取的加热方式是__ 。
(3)能够确定沉淀洗涤干净的操作和现象是__ 。
(4)写出焙烧过程中发生反应的化学方程式__ 。
(5)若洗涤后所得晶体未进行干燥而直接焙烧,则最终得到的纳米铁中含有的杂质可能为___ 。

已知:主反应在80℃左右条件下进行,直至得到黄色(FeC2O4•2H2O)沉淀。
(1)实验室中FeSO4溶液在保存时需要加入少量铁粉,原因是
(2)写出进行“主反应”的化学方程式
(3)能够确定沉淀洗涤干净的操作和现象是
(4)写出焙烧过程中发生反应的化学方程式
(5)若洗涤后所得晶体未进行干燥而直接焙烧,则最终得到的纳米铁中含有的杂质可能为
您最近一年使用:0次