将一定量的 通入体积为40mL的氢氧化钾溶液中,两者恰好完全反应,测得反应后溶液中有三种含氯元素的离子,其中
通入体积为40mL的氢氧化钾溶液中,两者恰好完全反应,测得反应后溶液中有三种含氯元素的离子,其中 的物质的量为0.06mol,
的物质的量为0.06mol, 的物质的量为0.03mol,请按要求回答下列问题。
的物质的量为0.03mol,请按要求回答下列问题。
(1)该反应的化学方程式为________________________________________________ 。
(2)该反应中,氧化剂与还原剂的物质的量之比为____________ 。
(3)上述反应中,通入 的物质的量为
的物质的量为____________ mol,氢氧化钾溶液的物质的量浓度为__________
mol/L。
 通入体积为40mL的氢氧化钾溶液中,两者恰好完全反应,测得反应后溶液中有三种含氯元素的离子,其中
通入体积为40mL的氢氧化钾溶液中,两者恰好完全反应,测得反应后溶液中有三种含氯元素的离子,其中 的物质的量为0.06mol,
的物质的量为0.06mol, 的物质的量为0.03mol,请按要求回答下列问题。
的物质的量为0.03mol,请按要求回答下列问题。(1)该反应的化学方程式为
(2)该反应中,氧化剂与还原剂的物质的量之比为
(3)上述反应中,通入
 的物质的量为
的物质的量为mol/L。
更新时间:2021-01-11 16:24:46
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】铜是生命必要的元素,也是人类最早使用的金属之一,西汉时期《淮南万毕术》里就有“曾青得铁,则化为铜”的记载,曾青可能是碳酸铜一类物质,把其溶于酸中得溶液,当把铁粉投入此溶液即可得铜。
(1)根据学过的化学知识,写出该过程的离子方程式:________ 。
(2)在化学反应中,铜元素可表现为0、+1、+2。Cu2+ 的未成对电子数有______ 个,向硫酸铜溶液中加入过量的氨水可以得到 [Cu(NH3)4]SO4 溶液,[Cu(NH3)4]2+的结构简式为___ 。
(3)向[Cu(NH3)4]SO4 水溶液中通入SO2 气体至溶液呈微酸性,析出白色沉淀CuNH4SO3。反应化学方程式为_____________ 。
(4)CuNH4SO3 与足量的硫酸混合并微热,得到金属Cu等物质,本法制得的Cu呈超细粉末状,有重要用途,写出该反应的离子方程式________ ,若该反应在密闭容器中进行,且酸量充足,计算反应物中Cu元素变成超细粉末Cu的转化率_______ ,理由是__________ 。
(1)根据学过的化学知识,写出该过程的离子方程式:
(2)在化学反应中,铜元素可表现为0、+1、+2。Cu2+ 的未成对电子数有
(3)向[Cu(NH3)4]SO4 水溶液中通入SO2 气体至溶液呈微酸性,析出白色沉淀CuNH4SO3。反应化学方程式为
(4)CuNH4SO3 与足量的硫酸混合并微热,得到金属Cu等物质,本法制得的Cu呈超细粉末状,有重要用途,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】煤是重要的能源,也是生产化工产品的重要原料。试用所学知识,解答下列问题:
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为________ 和________ 。
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理为FeS2 Fe2++SO42—
Fe2++SO42— Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为
Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为_______________________ ,第二步反应的离子方程式为________________ 。
(3)工业煤干馏得到的产品有焦炭、________ 。
(4)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=________ ,实际生产要将r值维持在1.7~2.2之间,原因是__________________________________________ 。
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理为FeS2
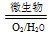 Fe2++SO42—
Fe2++SO42—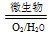 Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为
Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为(3)工业煤干馏得到的产品有焦炭、
(4)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在测定某铁矿石中的含铁量时,可准确称取0.2113g铁矿石溶解在酸里,再把Fe3+还原成Fe2+,然后用0.0223mol·L-1的KMnO4溶液滴定,发生反应的离子方程式如下:5Fe2++MnO +8H+=5Fe3++Mn2++4H2O滴定结果消耗KMnO4溶液17.20mL,试计算和回答下列问题:
+8H+=5Fe3++Mn2++4H2O滴定结果消耗KMnO4溶液17.20mL,试计算和回答下列问题:
(1)矿石中含铁的质量分数为___ 。
(2)KMnO4溶液应装在___ 式滴定管里,原因是__ 。
(3)如果矿石是用盐酸溶解制得的,Fe2+溶液里含有Cl-,则测定结果矿石中含铁量__ (填偏高、偏低、无影响),原因是___ 。
 +8H+=5Fe3++Mn2++4H2O滴定结果消耗KMnO4溶液17.20mL,试计算和回答下列问题:
+8H+=5Fe3++Mn2++4H2O滴定结果消耗KMnO4溶液17.20mL,试计算和回答下列问题:(1)矿石中含铁的质量分数为
(2)KMnO4溶液应装在
(3)如果矿石是用盐酸溶解制得的,Fe2+溶液里含有Cl-,则测定结果矿石中含铁量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮的氧化物(NO、 等)是主要的大气污染物,必须脱除才能排放。
等)是主要的大气污染物,必须脱除才能排放。
(1)臭氧脱硝法: 氧化NO结合水洗,可产生
氧化NO结合水洗,可产生 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(2)氨气催化吸收法处理尾气法:已知7mol氨气恰好能将含NO和 共6mol的混合气体完全转化为
共6mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比
的物质的量之比_______ 。
(3)研究不同温度下经酸化处理的 溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是_______ 。

(4)同时净化废气中二氧化硫和氮的氧化物的方法,将其转化为硫酸和硝酸,工艺流程如图所示。

各室中发生的反应如下:
氧化室: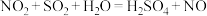
清除室: 、
、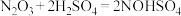 (固体)
(固体)
分解室: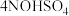 (固体)
(固体)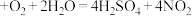
物质X和Y分别为_______ 、_______ 。(填化学式)。写出 、
、 与
与 反应生成
反应生成 的化学方程式:
的化学方程式:_______ 。
(5)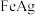 金属复合材料可将酸性水体中的
金属复合材料可将酸性水体中的 转化为
转化为 和
和 ,其反应历程如图所示(吸附在金属复合材料表面的物种用*标注)。
,其反应历程如图所示(吸附在金属复合材料表面的物种用*标注)。
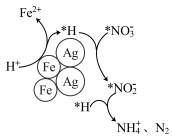
图中 的去除机理可描述为
的去除机理可描述为_______ 。
 等)是主要的大气污染物,必须脱除才能排放。
等)是主要的大气污染物,必须脱除才能排放。(1)臭氧脱硝法:
 氧化NO结合水洗,可产生
氧化NO结合水洗,可产生 ,该反应的化学方程式为
,该反应的化学方程式为(2)氨气催化吸收法处理尾气法:已知7mol氨气恰好能将含NO和
 共6mol的混合气体完全转化为
共6mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比
的物质的量之比(3)研究不同温度下经酸化处理的
 溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
(4)同时净化废气中二氧化硫和氮的氧化物的方法,将其转化为硫酸和硝酸,工艺流程如图所示。

各室中发生的反应如下:
氧化室:
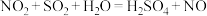
清除室:
 、
、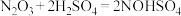 (固体)
(固体)
分解室:
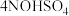 (固体)
(固体)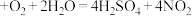
物质X和Y分别为
 、
、 与
与 反应生成
反应生成 的化学方程式:
的化学方程式:(5)
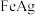 金属复合材料可将酸性水体中的
金属复合材料可将酸性水体中的 转化为
转化为 和
和 ,其反应历程如图所示(吸附在金属复合材料表面的物种用*标注)。
,其反应历程如图所示(吸附在金属复合材料表面的物种用*标注)。
图中
 的去除机理可描述为
的去除机理可描述为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知:6.4克铜与适量的浓硝酸反应,当铜完全溶解后,共收集到NO和NO2混合气体共2.24升(已折算为标准状况)。求:
(1)被还原的HNO3的物质的量______________ ;
(2)混合气体中NO_________ L,NO2________ L。
(1)被还原的HNO3的物质的量
(2)混合气体中NO
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.现有如下物质:①液态氯化氢②氯水③ ④
④ ⑤澄清石灰水⑥铝⑦NaOH溶液⑧
⑤澄清石灰水⑥铝⑦NaOH溶液⑧ 溶液
溶液
(1)这些物质中,属于电解质的是(填编号)_______ 。
(2)将铝放入氢氧化钠溶液中有气体产生,请写出发生反应的离子方程式_______ 。
(3)把少量的④加入⑤中,离子反应方程式为_______ 。
II.已知次磷酸(H3PO2)是一元中强酸。
(4)次磷酸钡是一种溶于水的强电解质,向Ba(H2PO2)2溶液中加入硫酸可以制取H3PO2,写出反应的离子方程式:_______ 。
(5)H3PO2可将溶液中的Ag+还原为银,从而用于化学镀银,反应同时生成P元素最高价氧化物对应的水化物。0.1molH3PO2能还原出金属银_______ g。
 ④
④ ⑤澄清石灰水⑥铝⑦NaOH溶液⑧
⑤澄清石灰水⑥铝⑦NaOH溶液⑧ 溶液
溶液(1)这些物质中,属于电解质的是(填编号)
(2)将铝放入氢氧化钠溶液中有气体产生,请写出发生反应的离子方程式
(3)把少量的④加入⑤中,离子反应方程式为
II.已知次磷酸(H3PO2)是一元中强酸。
(4)次磷酸钡是一种溶于水的强电解质,向Ba(H2PO2)2溶液中加入硫酸可以制取H3PO2,写出反应的离子方程式:
(5)H3PO2可将溶液中的Ag+还原为银,从而用于化学镀银,反应同时生成P元素最高价氧化物对应的水化物。0.1molH3PO2能还原出金属银
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。实验室制取干燥
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。实验室制取干燥 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为___________ 。

 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。实验室制取干燥
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。实验室制取干燥 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在高锰酸钾固体上滴加浓盐酸,马上产生黄绿色气体。反应的化学方程式为:2KMnO4 + 16HCl=2KC1 + 2MnCl2 + 5C12↑+ 8H2O
回答下列问题:
(1)此反应中的氧化剂是____ ,当在标准状况下产生0.112L氯气,转移的电子数为____ mol。
(2)氯原子的核电荷数为______ ;氧原子的原子结构示意图_______ 。
(3)在KC1固体中存在的化学键是__________ ;写出H2O电子式_________ 。
(4)工业上用氯气与消石灰作原料制造漂粉精,此反应的化学方程式是_________ 。
(5)浓盐酸的溶质是氯化氢,用一个实验证明氯化氢极易溶于水。_________ 。
回答下列问题:
(1)此反应中的氧化剂是
(2)氯原子的核电荷数为
(3)在KC1固体中存在的化学键是
(4)工业上用氯气与消石灰作原料制造漂粉精,此反应的化学方程式是
(5)浓盐酸的溶质是氯化氢,用一个实验证明氯化氢极易溶于水。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】海水是一个巨大的化学资源宝库。回答下列问题:
(1)海水提溴工艺中,发生反应: ,该反应中氧化剂是
,该反应中氧化剂是__________ ,它在反应中__________ (填“得到”或“失去”)电子;现有 标准状况下的
标准状况下的 参加该反应,则理论上可转化
参加该反应,则理论上可转化 的物质的量是
的物质的量是_________  。
。
(2)利用化学沉淀法可以去除粗盐中的杂质离子( 等)。向某粗盐水滴加过量
等)。向某粗盐水滴加过量 溶液,有关反应的离子方程式为
溶液,有关反应的离子方程式为__________ ,滴加 溶液略微过量的目的是
溶液略微过量的目的是__________ 。
(3)在常温下,将氯气通入 溶液中,可以得到一种漂白液,上述反应的化学方程式为
溶液中,可以得到一种漂白液,上述反应的化学方程式为__________ ,该漂白液的有效成分是__________ (填名称)。
(1)海水提溴工艺中,发生反应:
 ,该反应中氧化剂是
,该反应中氧化剂是 标准状况下的
标准状况下的 参加该反应,则理论上可转化
参加该反应,则理论上可转化 的物质的量是
的物质的量是 。
。(2)利用化学沉淀法可以去除粗盐中的杂质离子(
 等)。向某粗盐水滴加过量
等)。向某粗盐水滴加过量 溶液,有关反应的离子方程式为
溶液,有关反应的离子方程式为 溶液略微过量的目的是
溶液略微过量的目的是(3)在常温下,将氯气通入
 溶液中,可以得到一种漂白液,上述反应的化学方程式为
溶液中,可以得到一种漂白液,上述反应的化学方程式为
您最近一年使用:0次



