键长、键角和键能是描述共价键的三个重要参数,下列叙述正确的是
| A.键长和键角的数值可以通过晶体的X射线衍射实验获得 |
| B.因为H—O键的键能小于H—F键的键能,所以O2、F2与H2的反应能力逐渐减弱 |
| C.水分子的结构可表示为H—O—H,分子中的键角为180° |
| D.H—O键的键能为463kJ•mol-1,即18gH2O分解成H2和O2时,消耗的能量为2×463kJ |
更新时间:2021-02-19 17:24:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:
①Sn(s,白)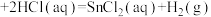

②Sn(s,灰)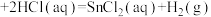

③Sn(s,灰)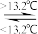 Sn(s,白)
Sn(s,白) 
下列说法不正确的是
①Sn(s,白)
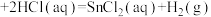

②Sn(s,灰)
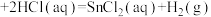

③Sn(s,灰)
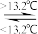 Sn(s,白)
Sn(s,白) 
下列说法不正确的是
| A.灰锡与白锡互为同素异形体 | B.锡在标准状况下以灰锡状态存在 |
| C.反应①是放热反应 | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用CO2制备甲醇是温室气体资源化重要途径。在某CO2催化加氢制甲醇的反应体系中主要存在如下反应:
反应I:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-48.2kJ·mol-1
反应II:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+42.5kJ·mol-1
反应III:CO(g)+2H2(g)=CH3OH(g)ΔH3
向恒压、密闭容器中通入1molCO2和3molH2,平衡时CO、CO2和CH3OH的物质的量分数随温度变化如图所示。下列说法不 正确的是

反应I:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-48.2kJ·mol-1
反应II:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+42.5kJ·mol-1
反应III:CO(g)+2H2(g)=CH3OH(g)ΔH3
向恒压、密闭容器中通入1molCO2和3molH2,平衡时CO、CO2和CH3OH的物质的量分数随温度变化如图所示。下列说法

| A.ΔH3=-90.7kJ·mol-1 |
| B.曲线a表示CO的物质的量分数随温度的变化 |
| C.在不改变反应时间和温度条件下,增大压强能提高CH3OH的产量 |
| D.在240~270℃内,温度改变对反应I和反应II平衡影响相反且程度接近 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据如图能量关系示意图,下列说法正确的是

| A.1molC(s)与1molO2(g)的能量之和等于393.5kJ |
| B.反应2CO(g)+O2(g)=2CO2(g)中,生成物的总能量大于反应物的总能量 |
| C.由C(s)→CO(g)的热化学方程式为:2C(s)+O2(g)=2CO(g) ΔH=-221.2kJ·mol-1,该方程式中的化学计量数不可表示分子个数 |
| D.热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO热值ΔH≈-10.1kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某学生用如图所示装置进行化学反应X+2Y=2Z能量变化情况的研究。当往试管中滴加试剂时看到U形管中液面甲处降、乙处升,关于该反应的下列叙述中不正确的是


| A.该反应为放热反应 |
| B.该反应为吸热反应 |
| C.反应物的总能量比生成物的总能量更高 |
| D.该反应过程可以看成是“贮存”于X、Y内部的部分能量转化为热能而释放出来 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】1935年,在中国化学家侯德榜的领导下,中国建成了第一座生产合成氨、硝酸等的联合企业——永利制碱厂。该企业首先合成氨,氨再经铂铑催化剂催化氧化得到NO,将NO、水和空气通入吸收塔中得到硝酸。氨催化氧化法制取NO的反应为:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ∆H=-905.8kJ/mol。下列关于工业上由氨气制取浓硝酸的过程说法正确的是
4NO(g)+6H2O(g) ∆H=-905.8kJ/mol。下列关于工业上由氨气制取浓硝酸的过程说法正确的是
 4NO(g)+6H2O(g) ∆H=-905.8kJ/mol。下列关于工业上由氨气制取浓硝酸的过程说法正确的是
4NO(g)+6H2O(g) ∆H=-905.8kJ/mol。下列关于工业上由氨气制取浓硝酸的过程说法正确的是| A.NH3的空间构型为平面三角形 |
| B.催化氧化法制取NO过程中,升高温度,可以增大该反应的平衡常数 |
| C.反应中每消耗22.4L(标准状况) NH3可放出热量226.45kJ |
| D.4mol NH3 (g)和5mol O2(g)所含能量总和比4mol NO(g)和6mol H2O(g)的总能量小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
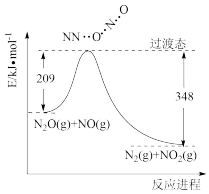
【推荐2】N2(g)和O2(g)反应生成 NO(g)的能量变化如图所示,下列说法正确的是
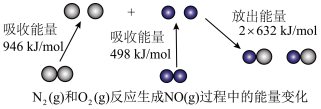

| A.通常情况下,NO(g)比N2(g)稳定 |
| B.常温下,N2(g)和O2(g)混合会直接生成NO |
| C.1molN2(g)和1molO2(g)反应生成2molNO(g)吸收的能量为180kJ |
| D.1molN2(g)和1molO2(g)具有的总能量大于2molNO(g)具有的总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下表中列出了25 ℃、101 kPa时一些物质的燃烧热数据:
已知:①1 mol液态水变为气态水要吸收44.0 kJ的热量;
②键能:C—H键 413.4 kJ·mol-1、H—H键 436.0 kJ·mol-1。
下列叙述错误的是
| 物质 | CH4(g) | CH3OCH3(g) | H2(g) | HC≡CH(g) |
| 燃烧热/(kJ·mol-1) | 890.3 | 1 453.0 | 285.8 | 1 299.6 |
②键能:C—H键 413.4 kJ·mol-1、H—H键 436.0 kJ·mol-1。
下列叙述错误的是
| A.CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH=-1 453.0 kJ·mol-1 |
| B.C≡C键的键能为786.0 kJ·mol-1 |
| C.2CH4(g)+O2(g)=CH3OCH3(g)+H2O(g) ΔH=-283.6 kJ·mol-1 |
| D.H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实不能用键能的大小来解释的是
| A.N元素的电负性较大,但N2的化学性质很稳定 |
| B.F2比O2更容易与H₂反应 |
| C.HF、HCl、HBr、HI的稳定性逐渐减弱 |
| D.稀有气体一般难发生反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】As2O3(砒霜)是两性氧化物(分子结构如图所示),溶于盐酸生成AsCl3,AsCl3用LiAlH4还原生成AlH3,下列说法正确的是


| A.As2O3分子中As原子的杂化方式为sp2 |
| B.LiAlH4为共价化合物 |
| C.AsCl3空间构型为平面正三角形 |
| D.AlH3分子键角大于109°28′ |
您最近一年使用:0次


 molO2(g)的总能量小于1molH2O(g)的能量
molO2(g)的总能量小于1molH2O(g)的能量