草酸与高锰酸钾在酸性条件下能够发生如下反应: +H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
+H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
(1)该反应中氧化剂和还原剂的物质的量之比为______ 。
(2)我们可以通过观察_____ ,来判断反应速率的大小
(3)如果研究催化剂对化学反应速率的影响,使用实验______ 和_____ (用Ⅰ~Ⅳ表示,下同),如果研究温度对化学反应速率的影响,使用实验_______ 和______ (用Ⅰ~Ⅳ表示,下同)。
(4)实验Ⅰ和Ⅳ研究浓度对反应速率的影响,Ⅳ中加入1mL蒸馏水的目的是_____ 。
(5)反应I、III、IV中都可观察到反应速率先慢后快的现象,引起这种现象的原因是_____ 。
 +H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
+H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
Ⅰ | 2 | 20 | |
Ⅱ | 2 | 20 | 5滴饱和MnSO4溶液 |
Ⅲ | 2 | 30 | |
Ⅳ | 1 | 20 | 1 mL蒸馏水 |
(2)我们可以通过观察
(3)如果研究催化剂对化学反应速率的影响,使用实验
(4)实验Ⅰ和Ⅳ研究浓度对反应速率的影响,Ⅳ中加入1mL蒸馏水的目的是
(5)反应I、III、IV中都可观察到反应速率先慢后快的现象,引起这种现象的原因是
更新时间:2021-01-29 17:31:07
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】将浓度均为0.01 mol/L的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。
已知该“碘钟实验”的总反应为H2O2+2S2O +2H+=S4O
+2H+=S4O +2H2O,反应分A、B两步进行。
+2H2O,反应分A、B两步进行。
反应A:H2O2+2I-+2H+=I2+2H2O
反应B:......
(1)反应B的离子方程式为_______ ,对于总反应,I-的作用相当于_______
(2)为了证明反应A、B的存在,进行实验Ⅰ:
a.向酸化的H2O2溶液中加入试剂X的水溶液,溶液变为蓝色;
b.再向得到的蓝色溶液中加入Na2S2O3溶液,溶液的蓝色褪去。
则试剂X应该为_______
(3)为探究溶液变蓝快慢的影响因素,进行实验Ⅱ、实验Ⅲ。(溶液浓度均为0.01 mol/L)
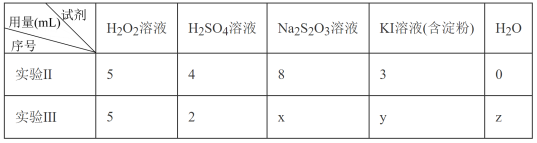
结果为溶液从混合时的无色变为蓝色的时间:实验Ⅱ<实验Ⅲ
① 实验Ⅲ中,x、y、z所对应的数值分别是_______
② 对比实验Ⅱ、实验Ⅲ,可得出的实验结论是_______
已知该“碘钟实验”的总反应为H2O2+2S2O
 +2H+=S4O
+2H+=S4O +2H2O,反应分A、B两步进行。
+2H2O,反应分A、B两步进行。反应A:H2O2+2I-+2H+=I2+2H2O
反应B:......
(1)反应B的离子方程式为
(2)为了证明反应A、B的存在,进行实验Ⅰ:
a.向酸化的H2O2溶液中加入试剂X的水溶液,溶液变为蓝色;
b.再向得到的蓝色溶液中加入Na2S2O3溶液,溶液的蓝色褪去。
则试剂X应该为_______
| A.KI | B.H2SO4、 | C.KI、淀粉 | D.Na2S2O3溶液、淀粉 |

结果为溶液从混合时的无色变为蓝色的时间:实验Ⅱ<实验Ⅲ
① 实验Ⅲ中,x、y、z所对应的数值分别是
② 对比实验Ⅱ、实验Ⅲ,可得出的实验结论是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】设计实验测定锌与硫酸反应的速率,按下列实验步骤完成实验:

①按图示安装装置,加入锌粒,然后快速加入40mL1mol/L的硫酸溶液,测量收集10mLH2所用的时间。
②按图示再安装一套装置,加入与前一套装置相同的锌粒,然后再快速加入40mL4mol/L的硫酸溶液,测量收集10mLH2所用的时间。
回答下列问题:
(1)实验所用仪器有:锥形瓶、双孔塞、分液漏斗、直角导气管、50mL注射器、铁架台、________ 。
(2)观察到的现象是:____________________________________ ;
收集10mL气体②所用时间比①所用时间________ 。
(3)所能得出的实验结论是:_________________________________ 。
(4)若在①实验中加入适量MnO2,则:________
A.如果①比②速率慢,则证明MnO2无催化作用
B.如果①比②速率快,则不能证明MnO2有无催化作用
C.如果①比②速率慢,则不能证明MnO2有无催化作用
D.如果①比②速率快,则证明MnO2有催化作用

①按图示安装装置,加入锌粒,然后快速加入40mL1mol/L的硫酸溶液,测量收集10mLH2所用的时间。
②按图示再安装一套装置,加入与前一套装置相同的锌粒,然后再快速加入40mL4mol/L的硫酸溶液,测量收集10mLH2所用的时间。
回答下列问题:
(1)实验所用仪器有:锥形瓶、双孔塞、分液漏斗、直角导气管、50mL注射器、铁架台、
(2)观察到的现象是:
收集10mL气体②所用时间比①所用时间
(3)所能得出的实验结论是:
(4)若在①实验中加入适量MnO2,则:
A.如果①比②速率慢,则证明MnO2无催化作用
B.如果①比②速率快,则不能证明MnO2有无催化作用
C.如果①比②速率慢,则不能证明MnO2有无催化作用
D.如果①比②速率快,则证明MnO2有催化作用
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】“氧来乐”是鱼塘养殖户的“救命药”,其标签如下表:

(1)“氧来乐”可以给鱼塘增氧的化学反应方程式:___________ 。有学生认为 也可以给鱼塘增氧,你认为可以吗?并简述理由:
也可以给鱼塘增氧,你认为可以吗?并简述理由:___________ 。
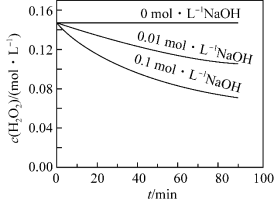
(2) 分解速率受多种因素影响。学生甲通过数字化实验测得
分解速率受多种因素影响。学生甲通过数字化实验测得 时,
时, 浓度随时间的变化如图所示,从下图中可得出的结论是:其他条件相同时,
浓度随时间的变化如图所示,从下图中可得出的结论是:其他条件相同时,___________ 。
(3)学生乙利用实验室提供的仪器和试剂进行了教材上的实验。
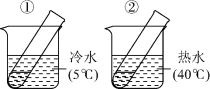
步骤:分别向①、②两支试管中加入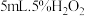 溶液,同时分别向两试管中加入2滴
溶液,同时分别向两试管中加入2滴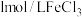 溶液(作催化剂)。待试管中均有适量气泡出现时,将试管①放入
溶液(作催化剂)。待试管中均有适量气泡出现时,将试管①放入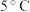 水浴中,将试管②放入
水浴中,将试管②放入 水浴中,观察实验现象。如下图。该实验是为了探究
水浴中,观察实验现象。如下图。该实验是为了探究___________ 对 分解速率的影响;
分解速率的影响;
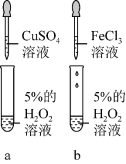
(4)学生丙为探究 两种催化剂对
两种催化剂对 分解速率的影响。
分解速率的影响。
设计了如下实验(如下图):分别向 两支试管中加入
两支试管中加入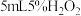 溶液,向试管a中加入2滴
溶液,向试管a中加入2滴 ,向试管b中加入2滴
,向试管b中加入2滴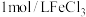 溶液,观察实验现象。该方案存在不严谨之处。请你改进:
溶液,观察实验现象。该方案存在不严谨之处。请你改进:___________ 。

| 主要成分 | 过氧化氢 |
| 含量规格 |  |
| 作用与用途 | 本品在分解过程中释放出活泼的新生态氧,用于养殖池塘的增氧,药性温和,使用方便,无残留,绿色环保。 |
| 用法 | 将本品以1000倍水稀释后直接泼洒于养殖池塘中 |
| 用量 | 每亩水深1米用本品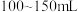 ,病情严重可加量使用,并可使用催化剂 ,病情严重可加量使用,并可使用催化剂 |
 也可以给鱼塘增氧,你认为可以吗?并简述理由:
也可以给鱼塘增氧,你认为可以吗?并简述理由:(2)
 分解速率受多种因素影响。学生甲通过数字化实验测得
分解速率受多种因素影响。学生甲通过数字化实验测得 时,
时, 浓度随时间的变化如图所示,从下图中可得出的结论是:其他条件相同时,
浓度随时间的变化如图所示,从下图中可得出的结论是:其他条件相同时,
(3)学生乙利用实验室提供的仪器和试剂进行了教材上的实验。
步骤:分别向①、②两支试管中加入
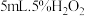 溶液,同时分别向两试管中加入2滴
溶液,同时分别向两试管中加入2滴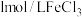 溶液(作催化剂)。待试管中均有适量气泡出现时,将试管①放入
溶液(作催化剂)。待试管中均有适量气泡出现时,将试管①放入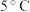 水浴中,将试管②放入
水浴中,将试管②放入 水浴中,观察实验现象。如下图。该实验是为了探究
水浴中,观察实验现象。如下图。该实验是为了探究 分解速率的影响;
分解速率的影响;
(4)学生丙为探究
 两种催化剂对
两种催化剂对 分解速率的影响。
分解速率的影响。设计了如下实验(如下图):分别向
 两支试管中加入
两支试管中加入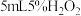 溶液,向试管a中加入2滴
溶液,向试管a中加入2滴 ,向试管b中加入2滴
,向试管b中加入2滴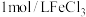 溶液,观察实验现象。该方案存在不严谨之处。请你改进:
溶液,观察实验现象。该方案存在不严谨之处。请你改进:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】研究化学反应速率是为了控制化学反应速率,使生产、生活中的大部分化学反应的速率都尽可能随着人们的意向改变。回答下列问题:
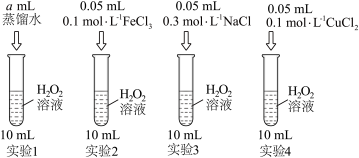
(1)某同学为探究 分解的影响因素(温度为
分解的影响因素(温度为 ,控制温度装置已省略)设计如图实验,不同时间测得的实验数据如表(
,控制温度装置已省略)设计如图实验,不同时间测得的实验数据如表( 的起始浓度为
的起始浓度为 )。
)。
①
___________ 。
②探究 对
对 分解速率的影响,应选择的实验有实验2、
分解速率的影响,应选择的实验有实验2、___________ ,实验前10min平均反应速率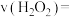
___________  ,实验2还能验证
,实验2还能验证___________ 对反应速率的影响。
③在②的基础上,实验2、实验4对比证明了___________ (填“ ”或“
”或“ ”)的催化能力较强。
”)的催化能力较强。
(2) 分解的化学方程式为
分解的化学方程式为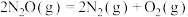 ,该反应生成物的总能量小于反应物的总能量。将
,该反应生成物的总能量小于反应物的总能量。将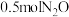 置于某恒容绝热反应器中发生该反应,反应速率与时间的关系如图。
置于某恒容绝热反应器中发生该反应,反应速率与时间的关系如图。
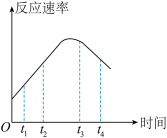
① 反应速率增加的原因是
反应速率增加的原因是___________ 。
②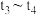 反应速率降低的原因是
反应速率降低的原因是___________ 。
(1)某同学为探究
 分解的影响因素(温度为
分解的影响因素(温度为 ,控制温度装置已省略)设计如图实验,不同时间测得的实验数据如表(
,控制温度装置已省略)设计如图实验,不同时间测得的实验数据如表( 的起始浓度为
的起始浓度为 )。
)。
时间/min 浓度/ 实验编号 | 0 | 2 | 10 | 15 | 20 |
| 1 | 1 | 几乎无变化 | 几乎无变化 | 几乎无变化 | 几乎无变化 |
| 2 | 1 | 0.80 | 0.65 | 0.52 | 0.40 |
| 3 | 1 | 几乎无变化 | 几乎无变化 | 几乎无变化 | 几乎无变化 |
| 4 | 1 | 0.90 | 0.82 | 0.75 | 0.70 |

②探究
 对
对 分解速率的影响,应选择的实验有实验2、
分解速率的影响,应选择的实验有实验2、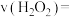
 ,实验2还能验证
,实验2还能验证③在②的基础上,实验2、实验4对比证明了
 ”或“
”或“ ”)的催化能力较强。
”)的催化能力较强。(2)
 分解的化学方程式为
分解的化学方程式为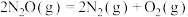 ,该反应生成物的总能量小于反应物的总能量。将
,该反应生成物的总能量小于反应物的总能量。将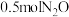 置于某恒容绝热反应器中发生该反应,反应速率与时间的关系如图。
置于某恒容绝热反应器中发生该反应,反应速率与时间的关系如图。
①
 反应速率增加的原因是
反应速率增加的原因是②
 反应速率降低的原因是
反应速率降低的原因是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
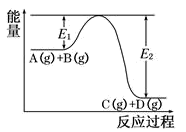
(1)该反应是________ 反应(填“吸热”“放热”)。
(2)反应体系中加入催化剂对反应热是否有影响?__________ 。
(3)在反应体系中加入催化剂,反应速率增大,E1的变化是:E1_________ (填“增大”“减小”“不变”)。
(4)由氢气和氧气反应生成1mol水蒸气放热241.8kJ·mol-1,写出其热化学方程式:____________ 。
(5)反应3Fe(s)+4H2O(g) Fe3O4+4H2(g),在一可变的容积的密闭容器中进行。
Fe3O4+4H2(g),在一可变的容积的密闭容器中进行。
①增加Fe的量, 其正反应速率的变化是_______ (填“增大”、“不变”或“减小”,以下相同)。
②保持体积不变,充入N2使体系压强增大,其正反应速率_______ 。
③保持压强不变,充入N2使容器的体积增大,逆反应速率_______ 。
 C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
(1)该反应是
(2)反应体系中加入催化剂对反应热是否有影响?
(3)在反应体系中加入催化剂,反应速率增大,E1的变化是:E1
(4)由氢气和氧气反应生成1mol水蒸气放热241.8kJ·mol-1,写出其热化学方程式:
(5)反应3Fe(s)+4H2O(g)
 Fe3O4+4H2(g),在一可变的容积的密闭容器中进行。
Fe3O4+4H2(g),在一可变的容积的密闭容器中进行。①增加Fe的量, 其正反应速率的变化是
②保持体积不变,充入N2使体系压强增大,其正反应速率
③保持压强不变,充入N2使容器的体积增大,逆反应速率
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】完成下列问题
(1)请认真观察下图,回答问题。
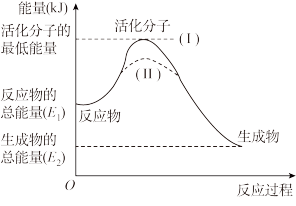
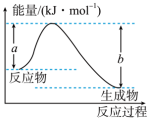
①该反应的ΔH=___________ (用含E1、E2的代数式表示)。若向该反应中加入合适的催化剂,活化能___________ (填“升高”“降低”或“不变”),ΔH___________ (填“升高”“降低”或“不变”)。
②若该图表示2H2O2(l) 2H2O(l)+O2(g) ΔH=-73.5 kJ·mol-1,该反应的活化能为54.3 kJ·mol-1,则其逆反应的活化能为
2H2O(l)+O2(g) ΔH=-73.5 kJ·mol-1,该反应的活化能为54.3 kJ·mol-1,则其逆反应的活化能为___________ kJ·mol-1。
(2)用H2O2、KI和洗洁精可完成“大象牙膏”实验(短时间内产生大量泡沫),某同学依据文献资料对该实验进行探究。
资料1:KI在该反应中的作用:H2O2+I-=H2O+IO-;H2O2+IO-=H2O+O2↑+I-。总反应的化学方程式为___________ 。
资料2:I2也可催化H2O2的分解反应。
实验中发现,H2O2与KI溶液混合后,产生大量气泡,溶液颜色变黄。再加入CCl4,振荡、静置,气泡明显减少。
①加CCl4并振荡、静置后还可观察到___________ ,说明有I2生成。
②气泡明显减少的原因可能是:i.H2O2浓度降低;ii.___________ 。以下对照实验说明i不是主要原因:向H2O2溶液中加入KI溶液,待溶液变黄后,分成两等份于A、B两试管中。A试管中加入CCl4,B试管中不加CCl4,分别振荡、静置。观察到的现象是___________ 。
(1)请认真观察下图,回答问题。

①该反应的ΔH=
②若该图表示2H2O2(l)
 2H2O(l)+O2(g) ΔH=-73.5 kJ·mol-1,该反应的活化能为54.3 kJ·mol-1,则其逆反应的活化能为
2H2O(l)+O2(g) ΔH=-73.5 kJ·mol-1,该反应的活化能为54.3 kJ·mol-1,则其逆反应的活化能为(2)用H2O2、KI和洗洁精可完成“大象牙膏”实验(短时间内产生大量泡沫),某同学依据文献资料对该实验进行探究。
资料1:KI在该反应中的作用:H2O2+I-=H2O+IO-;H2O2+IO-=H2O+O2↑+I-。总反应的化学方程式为
资料2:I2也可催化H2O2的分解反应。
实验中发现,H2O2与KI溶液混合后,产生大量气泡,溶液颜色变黄。再加入CCl4,振荡、静置,气泡明显减少。
①加CCl4并振荡、静置后还可观察到
②气泡明显减少的原因可能是:i.H2O2浓度降低;ii.
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】某课外实验小组测定了碳酸钙与稀盐酸反应过程中,生成CO2的浓度随时间的变化关系如下图所示。
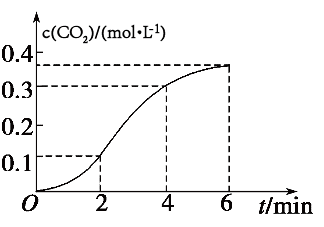
(1)碳酸钙与稀盐酸反应的离子方程式是_______ 。
(2)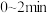 内用CO2表示的平均反应速率是
内用CO2表示的平均反应速率是_______ 。
(3)比较CO2在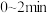 、
、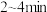 时平均反应速率的大小:υ(0~2)
时平均反应速率的大小:υ(0~2)_______ υ(2~4)(填“>”、“<”或“=”),说明该反应过程中_______ 热量,该反应中反应物的总能量_______ (填“>”、“<”或“=”)生成物的总能量。
(4)欲减缓该反应的速率,可采取的一种措施是_______ 。

(1)碳酸钙与稀盐酸反应的离子方程式是
(2)
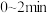 内用CO2表示的平均反应速率是
内用CO2表示的平均反应速率是(3)比较CO2在
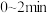 、
、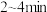 时平均反应速率的大小:υ(0~2)
时平均反应速率的大小:υ(0~2)(4)欲减缓该反应的速率,可采取的一种措施是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】Ⅰ.断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B的键能。下表列出了一些化学键的键能(E):
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应_______ (填“吸收”或“放出”)_______ kJ能量(用含有a、b的关系式表示)。 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=_______ 。
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为_______ 。
Ⅱ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
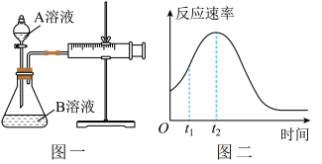
(4)该实验探究的是_______ 因素对化学反应速率的影响。如下图一,相同时间内针筒中所得的CO2体积大小关系是_______ (填实验序号)。 =
=_______ (假设混合液体积为50mL)。
(6)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定_______ 来比较化学反应速率。
(7)小组同学发现反应速率总是如上图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②_______ 。
| 化学键 | H—H | Cl—Cl | O=O | C—Cl | C—H | O—H | H—Cl |
| E/(kJ·mol-1) | 436 | 247 | x | 330 | 413 | 463 | 431 |
(1)如图表示某反应的能量变化关系,则此反应
 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为
Ⅱ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.1 mol·L-1KMnO4溶液 |
| ② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.1mol·L-1KMnO4溶液 |
 =
=(6)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定
(7)小组同学发现反应速率总是如上图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】铁单质化学性质活泼,来源丰富,价格低廉,被广泛用于修复地下水中硝酸盐氮的污染。某研究小组探究铁单质处理硝酸盐氮效果的影响因素,进行如下实验:
实验Ⅰ:在硝酸盐氮初始质量浓度为60mg/L,铁粉投加质量浓度为2.5g/L,25℃的条件下进行实验,结果如图1所示;
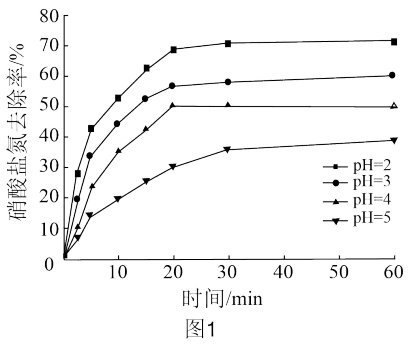
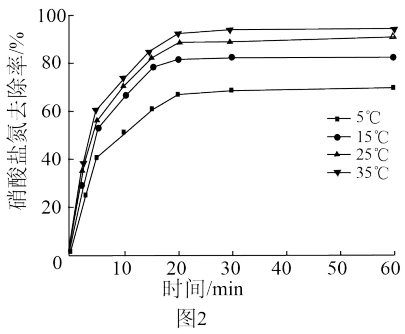
实验II:在硝酸盐氮初始质量浓度为60mg/L,铁粉投加质量浓度为2.5g/L,pH=2的条件下进行实验,结果如图2所示;
【分析与解释】
(1)在处理硝酸盐氮污染时,选用铁粉而不是铁块的原因是__ 。
(2)实验Ⅰ的目的是___ 。
(3)研究小组同学认为:在35℃,pH=2的条件下铁粉处理硝酸盐氮的效果最好,其证据是__ 。
(4)Fe与NO 反应生成Fe2+和NO的离子方程式为
反应生成Fe2+和NO的离子方程式为__ 。
实验Ⅰ:在硝酸盐氮初始质量浓度为60mg/L,铁粉投加质量浓度为2.5g/L,25℃的条件下进行实验,结果如图1所示;

实验II:在硝酸盐氮初始质量浓度为60mg/L,铁粉投加质量浓度为2.5g/L,pH=2的条件下进行实验,结果如图2所示;

【分析与解释】
(1)在处理硝酸盐氮污染时,选用铁粉而不是铁块的原因是
(2)实验Ⅰ的目的是
(3)研究小组同学认为:在35℃,pH=2的条件下铁粉处理硝酸盐氮的效果最好,其证据是
(4)Fe与NO
 反应生成Fe2+和NO的离子方程式为
反应生成Fe2+和NO的离子方程式为
您最近一年使用:0次




