回答下列问题:
(1) 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为___________ mol·L-1。
(2) 时,向
时,向 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的
晶体,保持温度不变,测得溶液的 。此时水的离子积
。此时水的离子积
___________ ,溶液中 为
为___________ mol·L-1。
(3) 时,
时,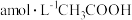 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
___________ 。
(1)
 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为(2)
 时,向
时,向 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的
晶体,保持温度不变,测得溶液的 。此时水的离子积
。此时水的离子积
 为
为(3)
 时,
时,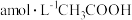 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
更新时间:2021-03-01 08:11:04
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)已知100℃时,水的离子积常数为 ,该温度下,有pH=11的NaOH溶液100mL,要使它的pH变为10(体积变化忽略不计):
,该温度下,有pH=11的NaOH溶液100mL,要使它的pH变为10(体积变化忽略不计):
①如果加入蒸馏水,应加___________ mL;
②如果加入pH=9的NaOH溶液,应加___________ mL;
③如果加入0.01 的盐酸,应加
的盐酸,应加___________ mL。
(2)在t℃时,测得0.01 NaOH溶液的pH=11,0.1
NaOH溶液的pH=11,0.1 的HA溶液中
的HA溶液中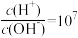 。回答下列问题:
。回答下列问题:
①该温度下,水的离子积常数Kw=___________ ;
②该温度下,0.1 的HA溶液中由水电离出的c(H+)=
的HA溶液中由水电离出的c(H+)=___________  。
。
(3)①明矾溶液呈___________ (填“酸性”“中性”或“碱性”),原因是___________ (用离子方程式表示);
②将氯化铁溶液蒸干灼烧得到的固体物质是___________ (填化学式)。
(1)已知100℃时,水的离子积常数为
 ,该温度下,有pH=11的NaOH溶液100mL,要使它的pH变为10(体积变化忽略不计):
,该温度下,有pH=11的NaOH溶液100mL,要使它的pH变为10(体积变化忽略不计):①如果加入蒸馏水,应加
②如果加入pH=9的NaOH溶液,应加
③如果加入0.01
 的盐酸,应加
的盐酸,应加(2)在t℃时,测得0.01
 NaOH溶液的pH=11,0.1
NaOH溶液的pH=11,0.1 的HA溶液中
的HA溶液中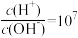 。回答下列问题:
。回答下列问题:①该温度下,水的离子积常数Kw=
②该温度下,0.1
 的HA溶液中由水电离出的c(H+)=
的HA溶液中由水电离出的c(H+)= 。
。(3)①明矾溶液呈
②将氯化铁溶液蒸干灼烧得到的固体物质是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)t℃,NH3·H2O的电离平衡常数为1.8×10-5, 的水解平衡常数为1.5×10-8,由此判断t
的水解平衡常数为1.5×10-8,由此判断t___________ 25℃(“>”“<”或“=”)
(2)BaSO4难溶于酸,可用于钡餐。某温度下将足量的BaSO4固体溶于一定量水中达到溶解平衡后,加入Na2CO3固体使c( )增大,溶液中c(
)增大,溶液中c( )的变化曲线如图所示(溶液体积不变),根据图象中数据分析、回答。Ksp(BaSO4)=1.0×10-10 (mol·L-1)2
)的变化曲线如图所示(溶液体积不变),根据图象中数据分析、回答。Ksp(BaSO4)=1.0×10-10 (mol·L-1)2

①图象中代表沉淀转化过程中c(SO )变化的曲线是
)变化的曲线是______ (填“MP”或“MN”)
②该温度下,BaCO3的Ksp=______ 。
 的水解平衡常数为1.5×10-8,由此判断t
的水解平衡常数为1.5×10-8,由此判断t(2)BaSO4难溶于酸,可用于钡餐。某温度下将足量的BaSO4固体溶于一定量水中达到溶解平衡后,加入Na2CO3固体使c(
 )增大,溶液中c(
)增大,溶液中c( )的变化曲线如图所示(溶液体积不变),根据图象中数据分析、回答。Ksp(BaSO4)=1.0×10-10 (mol·L-1)2
)的变化曲线如图所示(溶液体积不变),根据图象中数据分析、回答。Ksp(BaSO4)=1.0×10-10 (mol·L-1)2
①图象中代表沉淀转化过程中c(SO
 )变化的曲线是
)变化的曲线是②该温度下,BaCO3的Ksp=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1) 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为_________ 。
(2) 时,向
时,向 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的
晶体,保持温度不变,测得溶液的 。此时水的离子积
。此时水的离子积
________ ,溶液中 为
为________ 。
(3) 时,
时,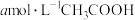 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
_______ 。
(4) 时,
时, 的
的 溶液和
溶液和 的NaOH溶液等体积混合后,溶液呈
的NaOH溶液等体积混合后,溶液呈_____ (填“酸”“中”或“碱”)性。
(5) 时,
时, ,
,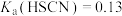 。该温度下将
。该温度下将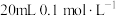
 溶液和
溶液和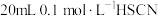 溶液分别与
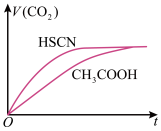
溶液分别与 溶液混合,实验测得产生的气体体积(V)随时间(t)变化的曲线如图所示,反应初始阶段,两种溶液产生
溶液混合,实验测得产生的气体体积(V)随时间(t)变化的曲线如图所示,反应初始阶段,两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是____ 。
(1)
 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为(2)
 时,向
时,向 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的
晶体,保持温度不变,测得溶液的 。此时水的离子积
。此时水的离子积
 为
为(3)
 时,
时,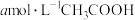 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
(4)
 时,
时, 的
的 溶液和
溶液和 的NaOH溶液等体积混合后,溶液呈
的NaOH溶液等体积混合后,溶液呈(5)
 时,
时, ,
,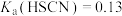 。该温度下将
。该温度下将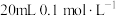
 溶液和
溶液和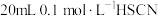 溶液分别与
溶液分别与 溶液混合,实验测得产生的气体体积(V)随时间(t)变化的曲线如图所示,反应初始阶段,两种溶液产生
溶液混合,实验测得产生的气体体积(V)随时间(t)变化的曲线如图所示,反应初始阶段,两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】下列六种情况下的pH分别为多少?(或范围)
(1)pH=2的HCl溶液稀释1000倍,所得溶液的pH( )
(2)pH=2的CH3COOH溶液稀释1000倍,所得溶液的pH( )
(3)pH=2的HCl溶液稀释100倍,所得溶液的pH( )
(4)pH=11的NaOH溶液稀释100倍,所得溶液的pH( )
(5)pH=11的NH3·H2O溶液稀释100倍,所得溶液的pH( )
(6)pH=10的NaOH溶液稀释100倍,所得溶液的pH( )
(1)pH=2的HCl溶液稀释1000倍,所得溶液的pH
(2)pH=2的CH3COOH溶液稀释1000倍,所得溶液的pH
(3)pH=2的HCl溶液稀释100倍,所得溶液的pH
(4)pH=11的NaOH溶液稀释100倍,所得溶液的pH
(5)pH=11的NH3·H2O溶液稀释100倍,所得溶液的pH
(6)pH=10的NaOH溶液稀释100倍,所得溶液的pH
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】现有浓度均为0.01mol/L的盐酸、硫酸、醋酸三种溶液,回答下列问题:
(1)分别用以上三种酸中和一定量(且等量)的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、V3,其大小关系为__________________ 。
(2)分别与Zn反应,开始时生成H2的速率为v1、v2、v3,其大小关系为________ 。
(3)将以上三种酸稀释1000倍后,pH分别变成a,b,c,其大小关系为_____________
(4)将上述盐酸稀释106倍后,c(H+): c(Cl-)=___________
(5)常温下,某浓度的盐酸和NaOH溶液的pH之和为16,当它们按一定体积比混合时,溶液的pH恰好等于7,则A与B的体积比是_____________
(1)分别用以上三种酸中和一定量(且等量)的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、V3,其大小关系为
(2)分别与Zn反应,开始时生成H2的速率为v1、v2、v3,其大小关系为
(3)将以上三种酸稀释1000倍后,pH分别变成a,b,c,其大小关系为
(4)将上述盐酸稀释106倍后,c(H+): c(Cl-)=
(5)常温下,某浓度的盐酸和NaOH溶液的pH之和为16,当它们按一定体积比混合时,溶液的pH恰好等于7,则A与B的体积比是
您最近一年使用:0次

 的盐酸平均分成两份,一份加入适量水,另一份加入与该盐酸物质的量浓度相同的适量
的盐酸平均分成两份,一份加入适量水,另一份加入与该盐酸物质的量浓度相同的适量 溶液,
溶液, 都升高了1,则加入的水与
都升高了1,则加入的水与 时,纯水中
时,纯水中 .
. 的稀硫酸与
的稀硫酸与 的
的

