MSO4和MCO3是两种难溶性盐。常温时两种物质的溶解度曲线如图所示,下列叙述错误的是
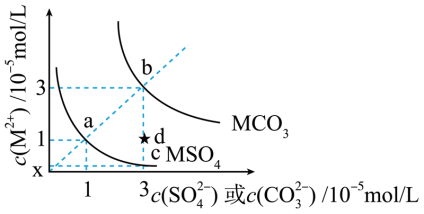
| A.Ksp(MCO3)=9.0×10−10 |
| B.c点的纵坐标0.33 |
| C.在饱和的MCO3澄清溶液里加入适量的Na2SO4固体,可使b点变为d点 |
| D.使1L含1molMSO4的悬浊液中的分散质完全转化为MCO3,需要加1molNa2CO3固体 |
2021·新疆·模拟预测 查看更多[7]
新疆维吾尔自治区2021届高三第二次联考理科综合能力测试化学试卷(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)小题22 难溶电解质的溶解平衡——备战2021年高考化学经典小题考前必刷(全国通用)江西省吉安市第一中学2021-2022学年高二上学期期中考试(理科)化学试题(已下线)题型27 沉淀溶解平衡常数及其应用图象(已下线)T13-溶液中的离子平衡(已下线)云南省昆明市官渡区第二中学2023-2024学年高三上学期开学化学试题
更新时间:2021-03-03 15:24:51
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列有关沉淀溶解平衡的说法正确的是( )
| A.在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的溶解度和Ksp均增大 |
| B.Ksp(XY2)小于Ksp(AB),则XY2的溶解度小于AB的溶解度 |
| C.在沉淀溶解平衡体系中,沉淀的速率和溶解的速率相等 |
| D.在碳酸钡的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】25℃,已知KSp(AgCl)=1.8×10-10,将2×10-5mol/L的AgNO3溶液和2×10-5mol/L的KCl溶液等体积混合,下列说法正确的是
| A.恰好形成AgCl饱和溶液 | B.能析出AgCl沉淀 |
| C.不能析出AgCl沉淀 | D.无法确定能否析出AgCl沉淀 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】某同学设计下述实验检验[Ag(NH3)2]Cl溶液中的Ag+,实验如表:
下列说法不正确的是
| 实验 | 试剂 | 现象 | |
| 试管 | 滴管 | ||
 | 2mL[Ag(NH3)2]Cl溶液 | 6滴0.1 mol∙L−1KCl溶液 | I中无明显现象 |
| 6滴0.1 mol∙L−1KI溶液 | II中产生黄色沉淀 | ||
| 6滴0.1 mol∙L−1HCl溶液 | III中产生白色沉淀 | ||
| 6滴饱和KCl溶液 | IV中产生白色沉淀 | ||
| A.I中的c(Ag+)较小,不足以与Cl-沉淀 |
B.II中存在平衡:AgI(s) Ag+(aq)+I-(aq) Ag+(aq)+I-(aq) |
| C.III说明NH3与H+的结合能力小于与Ag+的结合能力 |
| D.配离子与其它离子能否反应,其本质是平衡移动的问题 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】已知:常温下 、
、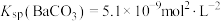 ,向硫酸钡的悬浊液中加入饱和碳酸钠溶液,充分搅拌后静置、分层,装置如图所示。下列说法正确的是
,向硫酸钡的悬浊液中加入饱和碳酸钠溶液,充分搅拌后静置、分层,装置如图所示。下列说法正确的是
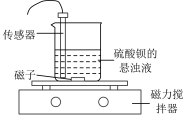
 、
、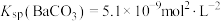 ,向硫酸钡的悬浊液中加入饱和碳酸钠溶液,充分搅拌后静置、分层,装置如图所示。下列说法正确的是
,向硫酸钡的悬浊液中加入饱和碳酸钠溶液,充分搅拌后静置、分层,装置如图所示。下列说法正确的是
| A.下层难溶的固体中含有碳酸钡 | B.下层难溶的固体中只含有硫酸钡 |
| C.下层难溶的固体中只含有碳酸钡 | D.上层溶液中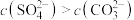 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将SO2通入溴水中,溶液褪色 | SO2具有漂白性 |
| B | 向5mL0.1mol·L-1 FeCl3溶液中滴加5滴0.1mol·L-1 KI溶液,再滴加2滴0.1mol·L-1 KSCN溶液,溶液呈红色 | FeCl3与KI反应有一定的限度 |
| C | 向偏铝酸钠溶液中通入少量CO2,产生白色沉淀 | AlO 结合H+能力比HCO 结合H+能力比HCO 强 强 |
| D | 向5mL0.1mol·L-1 AgNO3溶液滴加5滴0.1mol·L-1 K2CrO4溶液,有砖红色沉淀生成,再滴加5滴0.1mol·L-1 Na2S溶液,有黑色沉淀生成 | Ksp(Ag2CrO4)>Ksp(Ag2S) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】溶度积常数受影响()
| A.温度 | B.浓度 | C.压强 | D.酸碱性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列有关叙述中,不正确的( )
①pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
②已知25℃时,MgCO3的Ksp=6.82×10﹣6,则在该温度下,含有固体MgCO3的溶液中,无论c(Mg2+)与c(CO32﹣)是否相等,总有c(Mg2+)•c(CO32﹣)=6.82×10﹣6
③电解NaNO3溶液时,随着电解进行,溶液的pH减小
④常温下,在0.10mol•L﹣1的NH3•H2O溶液中加入少量NH4Cl晶体,则NH3•H2O电离被抑制,溶液pH减少.
①pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
②已知25℃时,MgCO3的Ksp=6.82×10﹣6,则在该温度下,含有固体MgCO3的溶液中,无论c(Mg2+)与c(CO32﹣)是否相等,总有c(Mg2+)•c(CO32﹣)=6.82×10﹣6
③电解NaNO3溶液时,随着电解进行,溶液的pH减小
④常温下,在0.10mol•L﹣1的NH3•H2O溶液中加入少量NH4Cl晶体,则NH3•H2O电离被抑制,溶液pH减少.
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列实验方案能达到目的的是
| 选项 | 实验方案 | 目的 |
| A | 在 饱和溶液中加少量 饱和溶液中加少量 粉末 粉末 | 证明存在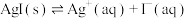 |
| B | 常温下,大小、形状相同的铝片分别与 、 、 的硫酸反应 的硫酸反应 | 探究浓度对反应速率的影响 |
| C | 常温下,用精密 计测定 计测定 、 、 溶液的 溶液的 分别为10.2、12.6 分别为10.2、12.6 | 证明HX的酸性比HY的酸性强 |
| D | 向相同浓度的 和 和 混合溶液中滴加少量 混合溶液中滴加少量 溶液 溶液 | 比较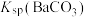 、 、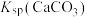 的相对大小 的相对大小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】25℃时,在含有大量 的饱和溶液中存在着平衡:
的饱和溶液中存在着平衡: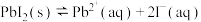 ,加入少量
,加入少量 固体,下列说法不正确的是
固体,下列说法不正确的是
 的饱和溶液中存在着平衡:
的饱和溶液中存在着平衡: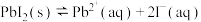 ,加入少量
,加入少量 固体,下列说法不正确的是
固体,下列说法不正确的是A.溶液中 浓度减小、 浓度减小、 浓度增大 浓度增大 | B.溶度积常数 不变 不变 |
C. 的溶解度不变 的溶解度不变 | D.沉淀溶解平衡向左移动 |
您最近一年使用:0次
【推荐3】一定温度下,可用K2S沉淀Cu2+、Mn2+、Zn2+三种离子(M2+),所需S2- 最低浓度的对数值lgc (S2-)与lgc (M2+)的关系如图所示。下列说法不正确的是
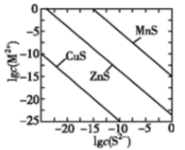

| A.三种离子对应的硫化物的溶度积常数中,Ksp(MnS)最大,约为1×10-15 ;Ksp(CuS) 最小,约为1×10 -35 |
| B.MnS+Cu2+ ⇌CuS+Mn2+,K=1020 |
| C.向ZnS的悬浊液(含ZnS固体)中滴加少量水,沉淀溶解平衡向溶解的方向移动,c(S2- )变小 |
| D.向相同浓度的Cu2+、Zn2+、Mn2+混合溶液中逐滴加入1×10-4mol•L-1的Na2S溶液, Cu2+最先沉淀 |
您最近一年使用:0次

 +6H+=3I2+3H2O
+6H+=3I2+3H2O =Fe3++NO↑+2H2O
=Fe3++NO↑+2H2O +2H2O=2Mn2++4H++5
+2H2O=2Mn2++4H++5
 (aq)
(aq) (Ax+)•c平(By-)的是
(Ax+)•c平(By-)的是 Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)

