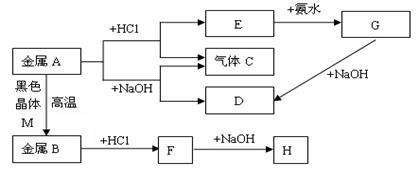
用铁、铝的混合物进行如下实验:

(1)操作X的名称是_______ 。
(2)①加入足量NaOH溶液时发生反应的离子方程式为_______ 。
(3)检验溶液E中阳离子所需试剂为_______ ,现象为_______ 。
(4)向溶液D中加入NaOH溶液并长时间暴露在空气中,此过程的现象:_______ ,此转化的化学方程式为:_______ 。
(5)写出③加入氯水的离子方程式_______ 。

(1)操作X的名称是
(2)①加入足量NaOH溶液时发生反应的离子方程式为
(3)检验溶液E中阳离子所需试剂为
(4)向溶液D中加入NaOH溶液并长时间暴露在空气中,此过程的现象:
(5)写出③加入氯水的离子方程式
更新时间:2021-03-04 08:02:31
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质。反应①②均为工业上的重要反应。
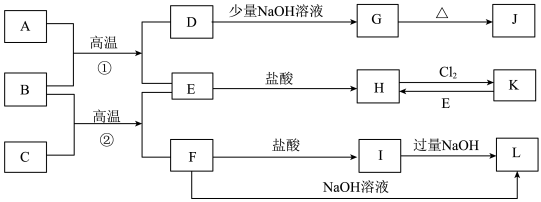
请回答下列问题:
(1)写出下列物质的化学式:D___________ ;K____________ ;L______________ 。
(2)写出B与C高温反应生成E和F的化学方程式:_______________________ 。
(3)写出D与J的稀溶液反应生成G的离子方程式:______________________ 。
(4)写出H转化为K的离子方程式:______________________ 。

请回答下列问题:
(1)写出下列物质的化学式:D
(2)写出B与C高温反应生成E和F的化学方程式:
(3)写出D与J的稀溶液反应生成G的离子方程式:
(4)写出H转化为K的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:

注: SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为___________ 。
(2)向“过滤I”所得滤液中加入NaHCO3溶液,写出该反应的离子方程式___________ 。
(3)“电解I”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是_____ 。
(4)铝粉在1 000° C时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是______ 。

注: SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为
(2)向“过滤I”所得滤液中加入NaHCO3溶液,写出该反应的离子方程式
(3)“电解I”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是
(4)铝粉在1 000° C时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
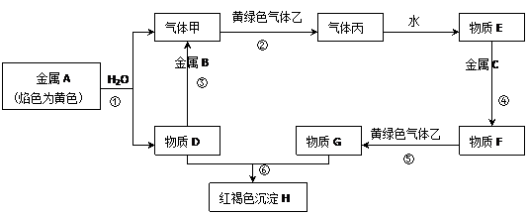
请回答下列问题:
(1)写出下列物质的化学式:A_______ C_______ 甲_______ 乙_______
(2)D溶液和F溶液在空气中混合的现象:_______ 。
(3)写出下列反应的离子方程式:反应①_______ ;反应③_______ 。
(4)检验物质D中金属阳离子的实验方法名称_______ (不要求写具体操作过程),检验物质G中金属阳离子的常用试剂_______ (填名称)
(5)实验室制备H胶体的化学反应方程式_______

请回答下列问题:
(1)写出下列物质的化学式:A
(2)D溶液和F溶液在空气中混合的现象:
(3)写出下列反应的离子方程式:反应①
(4)检验物质D中金属阳离子的实验方法名称
(5)实验室制备H胶体的化学反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】已知在温度低于570℃ 时,还原铁粉与水蒸气反应的产物是FeO;高于570℃ 时,生成Fe3O4。老师用下图所示实验装置,完成了还原铁粉与水蒸气反应的演示实验。

甲同学为探究实验后试管内固体的成分,进行了下列实验:
试回答下列问题:
(1)湿棉花的作用是______________ 。
(2)写出高于570℃ 时,Fe 与水蒸气反应的化学方程式:___________ 。
(3)乙同学认为加入KSCN 溶液没有出现血红色的原因可能是固体中没有Fe3O4,也有可能是因为___ (填物质名称)过量造成的。该物质过量时,溶液中还会发生反应,导致加入KSCN 溶液时没有出现血红色,该反应的离子方程式是______________ 。
(4)丙同学利用上述实验①加盐酸后的溶液制取白色的Fe(OH)2沉淀,向滤液中加入足量NaOH 溶液后,观察到的实验现象为___ 。

甲同学为探究实验后试管内固体的成分,进行了下列实验:
| 实验编号 | 实验操作 | 实验现象 |
① | 取少量黑色粉末放入试管中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
② | 向试管中滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
(1)湿棉花的作用是
(2)写出高于570℃ 时,Fe 与水蒸气反应的化学方程式:
(3)乙同学认为加入KSCN 溶液没有出现血红色的原因可能是固体中没有Fe3O4,也有可能是因为
(4)丙同学利用上述实验①加盐酸后的溶液制取白色的Fe(OH)2沉淀,向滤液中加入足量NaOH 溶液后,观察到的实验现象为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学看到“利用零价铁还原 脱除地下水中硝酸盐”的相关资料后,利用如图装置探究铁粉与KNO3溶液的反应。实验步骤及现象如下:
脱除地下水中硝酸盐”的相关资料后,利用如图装置探究铁粉与KNO3溶液的反应。实验步骤及现象如下:
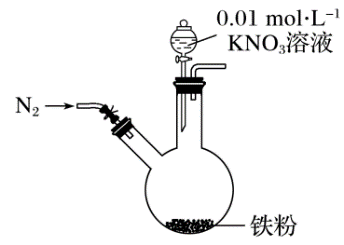
(1)通入N2并保持后续反应均在N2氛围中进行的实验目的是_______ 。
(2)白色物质是_______ (写化学式)。
(3)为了探究滤液的成分,该同学进一步设计了下述实验:
(ⅰ)根据以上实验现象,可以判断滤液中存在_______ (填离子符号)。
(ⅱ)步骤②中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因:_______ (写第一步反应)。
(ⅲ)步骤③中生成气体的离子方程式为_______ 。
 脱除地下水中硝酸盐”的相关资料后,利用如图装置探究铁粉与KNO3溶液的反应。实验步骤及现象如下:
脱除地下水中硝酸盐”的相关资料后,利用如图装置探究铁粉与KNO3溶液的反应。实验步骤及现象如下:
| 实验步骤 | 实验现象 |
| ①打开弹簧夹,缓慢通入N2 | |
| ②加入0.01mol·L-1的酸性KNO3溶液100mL | 铁粉部分溶解,溶液呈浅绿色;铁粉不再溶解后,剩余铁粉表面附着少量白色物质 |
| ③反应停止后,拔掉橡胶塞,将圆底烧瓶取下 | 烧瓶内气体的颜色没有发生变化 |
| ④将剩余固体过滤 | 表面的白色物质变为红褐色 |
(2)白色物质是
(3)为了探究滤液的成分,该同学进一步设计了下述实验:
| 实验步骤 | 实验现象 |
| ①取部分滤液于试管中,向其中加入KSCN溶液 | 溶液无变化 |
| ②将上述溶液分为两份,一份中滴入氯水,另一份中滴加稀硫酸 | 两份溶液均变为红色 |
| ③另取部分滤液于试管中,向其中加入浓NaOH溶液并加热,在试管口放置湿润的红色石蕊试纸 | 有气体生成,该气体使湿润的红色石蕊试纸变蓝 |
(ⅱ)步骤②中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因:
(ⅲ)步骤③中生成气体的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铁是人类比较早使用的金属之一,完成下列问题:
Ⅰ.电子工业中用30%的FeCl3 溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程如图所示。

(1)FeCl3 溶液蚀刻铜箔反应的离子方程式为:_______ ;
(2)滤液中存在较多的阳离子是_______ ;
(3)以下试剂也可以替代氯气完成转化,最好选用的是_______ (填序号)。
a.酸性KMnO4溶液 b.H2O2 溶液 c.溴水
Ⅱ.某氯化铁样品中含有少量FeCl2杂质,现要测定其中铁元素的质量分数,实验步骤如下:
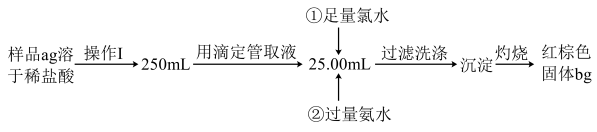
(4)过滤时所用到的玻璃仪器有_______ (填仪器名称)。
(5)写出②加入过量氨水的离子方程式:_______ 。
(6)样品中铁元素的质量分数为_______ 。
(7)若沉淀灼烧不充分,对最终测量结果的影响:_______ (填“偏大”“偏小”或“无影响”)。
Ⅰ.电子工业中用30%的FeCl3 溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程如图所示。

(1)FeCl3 溶液蚀刻铜箔反应的离子方程式为:
(2)滤液中存在较多的阳离子是
(3)以下试剂也可以替代氯气完成转化,最好选用的是
a.酸性KMnO4溶液 b.H2O2 溶液 c.溴水
Ⅱ.某氯化铁样品中含有少量FeCl2杂质,现要测定其中铁元素的质量分数,实验步骤如下:

(4)过滤时所用到的玻璃仪器有
(5)写出②加入过量氨水的离子方程式:
(6)样品中铁元素的质量分数为
(7)若沉淀灼烧不充分,对最终测量结果的影响:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】化合物A、B组成元素相同,且B为白色,C是一种与B含有相同价态该金属元素的硫酸盐,向C中加入适量的氢氧化钠溶液,可观察到生成的沉淀迅速变为灰绿色,最后变为红褐色沉淀A,加热A可得红棕色粉末D。回答下列问题:
(1)写出各物质的化学式:A_______ 、B_______ 、C_______ 、D_______ 。
(2)写出B转化为A的化学方程式:_______ 。
(3)写出A受热分解的化学方程式:_______ 。
(1)写出各物质的化学式:A
(2)写出B转化为A的化学方程式:
(3)写出A受热分解的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C是三种常见的单质,其中A为固体,B、C为气体;D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色;B和C反应的产物极易溶于水得无色溶液E。它们之间转化关系如图所示。
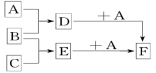
(1)写出A的化学式___________ ,B所含元素的原子结构示意图___________ ;
(2)写出D和E分别与A反应的离子方程式:
D+A:___________ ;
E+A:___________ ;
(3)写出在F中加入NaOH的产物在空气中放置所发生的反应的化学方程式___________ 。

(1)写出A的化学式
(2)写出D和E分别与A反应的离子方程式:
D+A:
E+A:
(3)写出在F中加入NaOH的产物在空气中放置所发生的反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】用含铬不锈钢废渣(含 、
、 、
、 、
、 等)制取
等)制取 (铬绿)工艺流程如图所示:
(铬绿)工艺流程如图所示:
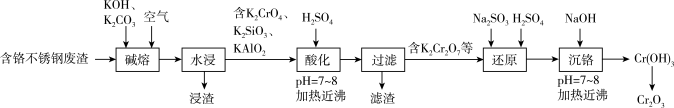
回答下列问题:
(1)“碱熔”时,为使废渣充分氧化可采取的措施是_____ (写一条)。
(2) 、KOH、
、KOH、 反应生成
反应生成 的化学方程式为
的化学方程式为_____ 。
(3)“水浸”时,碱熔渣中的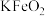 强烈水解生成的难溶物为
强烈水解生成的难溶物为_____ (填化学式);为检验“水浸”后的滤液中是否含有 ,可选用的化学试剂是
,可选用的化学试剂是_____ 。
(4)常温下,“酸化”时pH不宜过低(酸性太强)的原因是_____ 。
(5)“还原”时发生反应的离子方程式为_____ 。
(6)由 制取铬绿的方法是
制取铬绿的方法是_____ 。
 、
、 、
、 、
、 等)制取
等)制取 (铬绿)工艺流程如图所示:
(铬绿)工艺流程如图所示:
回答下列问题:
(1)“碱熔”时,为使废渣充分氧化可采取的措施是
(2)
 、KOH、
、KOH、 反应生成
反应生成 的化学方程式为
的化学方程式为(3)“水浸”时,碱熔渣中的
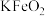 强烈水解生成的难溶物为
强烈水解生成的难溶物为 ,可选用的化学试剂是
,可选用的化学试剂是(4)常温下,“酸化”时pH不宜过低(酸性太强)的原因是
(5)“还原”时发生反应的离子方程式为
(6)由
 制取铬绿的方法是
制取铬绿的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】各物质间的转化关系如下图所示,请完成下列空白
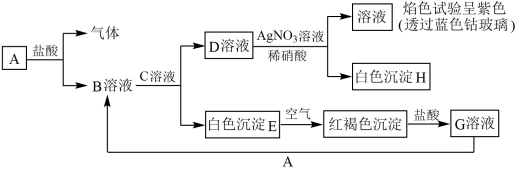
(1)写出D和B的化学式:D___________ ,B___________
(2)写出E转化为红褐色沉淀的化学方程式:___________
(3)写出向G溶液中加入A后的离子方程式:___________
(4)向G溶液中加入Cu也能生成B,写出加入Cu的离子方程式___________

(1)写出D和B的化学式:D
(2)写出E转化为红褐色沉淀的化学方程式:
(3)写出向G溶液中加入A后的离子方程式:
(4)向G溶液中加入Cu也能生成B,写出加入Cu的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于胃酸 。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验:

(1)试剂1可选择_______ 。
(2)加入试剂2为了验证 是否被氧化,试剂2选择
是否被氧化,试剂2选择_______ 。
(3)一般在服用“速力菲”时,同时服用维生素C,将不易吸收的 转化为
转化为 ,说明维生素C具有
,说明维生素C具有_______ 性。
(4)加入新制氯水,溶液中发生反应的离子方程式是_______ 。
(5)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色絮状沉淀
,溶液中白色絮状沉淀 更易被氧化,请写出
更易被氧化,请写出 在空气中被
在空气中被 氧化的化学方程式是
氧化的化学方程式是_______ ,沉淀转化过程的现象是_______ 。
 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验:
(1)试剂1可选择
(2)加入试剂2为了验证
 是否被氧化,试剂2选择
是否被氧化,试剂2选择(3)一般在服用“速力菲”时,同时服用维生素C,将不易吸收的
 转化为
转化为 ,说明维生素C具有
,说明维生素C具有(4)加入新制氯水,溶液中发生反应的离子方程式是
(5)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色絮状沉淀
,溶液中白色絮状沉淀 更易被氧化,请写出
更易被氧化,请写出 在空气中被
在空气中被 氧化的化学方程式是
氧化的化学方程式是
您最近一年使用:0次