按要求写出化学方程式。
(1)Na和H2O反应:_______
(2)Na2O2和CO2反应:_______
(3)Na2O2和H2O反应:_______
(4)Fe在Cl2中燃烧:_______
(5)Fe和H2O(g)的反应:_______
(6)Fe和FeCl3(aq)的反应:_______
(7)Cl2和NaOH(aq)的反应:_______
(1)Na和H2O反应:
(2)Na2O2和CO2反应:
(3)Na2O2和H2O反应:
(4)Fe在Cl2中燃烧:
(5)Fe和H2O(g)的反应:
(6)Fe和FeCl3(aq)的反应:
(7)Cl2和NaOH(aq)的反应:
更新时间:2021-03-11 13:10:57
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1molO3转化为1molO2和1molH2O)等物质常被用作消毒剂,等物质的量的上述物质消毒效率(消毒效率是指单位物质的量消毒剂的得电子数目)最高的是__ (填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为__ ,H2O2被称为“绿色氧化剂”的理由是___ 。
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定,可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平),在该反应中,当有1molClO2生成时转移的电子个数约为___ 。
(4)“84”消毒液(主要成分是NaClO))和洁厕剂(主要成分是浓盐酸)不能混用,原因是__ (用化学方程式表示):利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式:__ 。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1molO3转化为1molO2和1molH2O)等物质常被用作消毒剂,等物质的量的上述物质消毒效率(消毒效率是指单位物质的量消毒剂的得电子数目)最高的是
A.Cl2 B.H2O2 C.ClO2 D.O3
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定,可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平),在该反应中,当有1molClO2生成时转移的电子个数约为
(4)“84”消毒液(主要成分是NaClO))和洁厕剂(主要成分是浓盐酸)不能混用,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】含氯消毒剂、过氧化物能有效灭活病毒,是常用消毒剂。请回答下列问题:
(1)消毒剂次氯酸钠可由氯气和NaOH溶液反应制得,反应的化学方程式为________ 。
(2)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由Cl2O与ClO2按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是________ 。
②制备时Cl2O与ClO2完全反应的物质的量理论比为________ 。
(3)兴趣小组设计如下图实验装置制取少量消毒液。
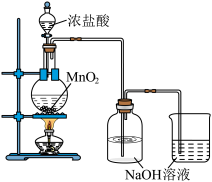
①MnO2与浓HCl反应的离子方程式为________ 。
②充分反应后,测得消毒液中NaCl与NaClO的物质的量之比大于1。可能的原因有________ (用文字简述)。
(4)Na2O2在呼吸面具中作供氧剂使用,若有7.8 g Na2O2参加反应,则转移的电子的物质的量为________ 。
(1)消毒剂次氯酸钠可由氯气和NaOH溶液反应制得,反应的化学方程式为
(2)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由Cl2O与ClO2按一定比例混合后在NaOH溶液中反应制得。
①NaClO2中氯元素的化合价是
②制备时Cl2O与ClO2完全反应的物质的量理论比为
(3)兴趣小组设计如下图实验装置制取少量消毒液。

①MnO2与浓HCl反应的离子方程式为
②充分反应后,测得消毒液中NaCl与NaClO的物质的量之比大于1。可能的原因有
(4)Na2O2在呼吸面具中作供氧剂使用,若有7.8 g Na2O2参加反应,则转移的电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】正误判断
1.1molCa变成Ca2+时失去的电子数为2NA。(_______)
2.1molCl2与足量Fe反应,转移的电子数为3NA。(_______)
3.1molCl2参加反应转移电子数一定为2NA。(_______)
4.在反应KIO3+6HI=KI+3I2+3H2O中,每生成3molI2转移的电子数为6NA。(_______)
5.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA。(_______)
1.1molCa变成Ca2+时失去的电子数为2NA。(_______)
2.1molCl2与足量Fe反应,转移的电子数为3NA。(_______)
3.1molCl2参加反应转移电子数一定为2NA。(_______)
4.在反应KIO3+6HI=KI+3I2+3H2O中,每生成3molI2转移的电子数为6NA。(_______)
5.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
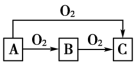
(1)若A是一种金属,C是淡黄色固体,则B的化学式为____________ ,A→C反应的化学方程式为________________________________ 。
(2)若A是一种非金属,其常见单质为黑色固体,C是最主要的温室气体,则C的分子式为______ ,B→C反应的化学方程式为_____________________________ 。

(1)若A是一种金属,C是淡黄色固体,则B的化学式为
(2)若A是一种非金属,其常见单质为黑色固体,C是最主要的温室气体,则C的分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】探究钠及其化合物的性质,请按要求填空:
(1)Na、 、
、 、
、 久置空气中最终都是变为
久置空气中最终都是变为___________ (填化学式);
(2)写出金属钠投入水中发生反应的化学方程式是___________ ;
(3)在一定量的稀盐酸中,加入少量高铜酸钠( )固体,产生黄绿色气体。写出稀盐酸与高铜酸钠固体反应的化学方程式是
)固体,产生黄绿色气体。写出稀盐酸与高铜酸钠固体反应的化学方程式是___________ 。
(1)Na、
 、
、 、
、 久置空气中最终都是变为
久置空气中最终都是变为(2)写出金属钠投入水中发生反应的化学方程式是
(3)在一定量的稀盐酸中,加入少量高铜酸钠(
 )固体,产生黄绿色气体。写出稀盐酸与高铜酸钠固体反应的化学方程式是
)固体,产生黄绿色气体。写出稀盐酸与高铜酸钠固体反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】钠的氧化物有氧化钠和过氧化钠两种.
(1)写出过氧化钠与水及二氧化碳反应的化学方程式,并分析电子转移的方向和数目,指出氧化剂、还原剂.____________________________________________________________________
(2)在呼吸面具和潜水艇里,用作氧气来源的物质是________ .
A.H2O2 B.Na2O2
C.KClO3 D.KMnO4
(3)把Na2O2投入到少量紫色石蕊溶液中,有什么现象?如何解释?_____________________________________ .
(1)写出过氧化钠与水及二氧化碳反应的化学方程式,并分析电子转移的方向和数目,指出氧化剂、还原剂.
(2)在呼吸面具和潜水艇里,用作氧气来源的物质是
A.H2O2 B.Na2O2
C.KClO3 D.KMnO4
(3)把Na2O2投入到少量紫色石蕊溶液中,有什么现象?如何解释?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】A、B、C 为中学常见单质,其中一种为金属;通常情况下,A 为固体,B 为液体,C 为气体。D、 E、F、G、H、X 均为化合物,其中 X 是一种无氧强酸、E 为黑色固体,H 在常温下为液体。它们之间的 转化关系如图所示(其中某些反应条件和部分反应物已略去)。
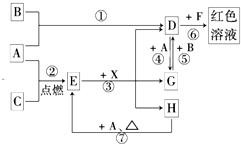
(1)写出化学式:A____________ 、D__________ 、E__________ 、X________ 。
(2) 在反应①~⑦中,不属于氧化还原反应的是__________ (填编号)。
(3) 反应⑥的离子方程式为__________ 。
(4)反应⑦的化学方程式为__________ ,该反应中每消耗 0.3molA,可转移电子__________ mol。

(1)写出化学式:A
(2) 在反应①~⑦中,不属于氧化还原反应的是
(3) 反应⑥的离子方程式为
(4)反应⑦的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】正误判断
1.铁位于元素周期表中第4周期VIIIB族。(_______)
2.铁的化学性质比较活泼,所以铁在自然界中全部以化合态存在。(_______)
3.Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2。(_______)
4.Fe分别与氯气、盐酸反应得到相同的氯化物。(_______)
5.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4。(_______)
6.工业上可用铁制容器储存、运输浓硝酸、浓硫酸。(_______)
7.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3。(_______)
8.工业上在高温下用CO还原含Fe2O3的铁矿石炼铁。(_______)
9.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应。(_______)
1.铁位于元素周期表中第4周期VIIIB族。(_______)
2.铁的化学性质比较活泼,所以铁在自然界中全部以化合态存在。(_______)
3.Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2。(_______)
4.Fe分别与氯气、盐酸反应得到相同的氯化物。(_______)
5.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4。(_______)
6.工业上可用铁制容器储存、运输浓硝酸、浓硫酸。(_______)
7.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3。(_______)
8.工业上在高温下用CO还原含Fe2O3的铁矿石炼铁。(_______)
9.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求回答问题:
Ⅰ.(1) 含0.3 mol Al3+的Al2(SO4)3溶液中所含的SO 的物质的量是
的物质的量是___________ mol。
(2)由CH4和O2的组成的混和气体,在标况下的密度是H2的15倍。则该混合气体中CH4和O2的体积比为_______ 。
(3)Al粉和NaOH溶液反应的离子方程式:__________________ 。
(4)铁粉和水蒸气反应化学方程式:_________________ 。
Ⅱ.铝粉与某些金属氧化物 组成的混合物叫铝热剂,铝热剂在高温下发生的反应叫铝热反应.如:2Al+Fe2O3 2Fe+Al2O3,反应发生时放出大量的热.仔细阅读上述信息回答下列问题:
2Fe+Al2O3,反应发生时放出大量的热.仔细阅读上述信息回答下列问题:
(1)“铝热反应”属于四大基本反应类型中的________ 反应.
(2)信息中的“某些”反应指________ (填“比铝活泼的”、“比铝稳定的”或“任意”)金属.
(3)试写出铝粉与MnO2发生的铝热反应方程式________________________ .
Ⅰ.(1) 含0.3 mol Al3+的Al2(SO4)3溶液中所含的SO
 的物质的量是
的物质的量是(2)由CH4和O2的组成的混和气体,在标况下的密度是H2的15倍。则该混合气体中CH4和O2的体积比为
(3)Al粉和NaOH溶液反应的离子方程式:
(4)铁粉和水蒸气反应化学方程式:
Ⅱ.铝粉与
 2Fe+Al2O3,反应发生时放出大量的热.仔细阅读上述信息回答下列问题:
2Fe+Al2O3,反应发生时放出大量的热.仔细阅读上述信息回答下列问题:(1)“铝热反应”属于四大基本反应类型中的
(2)信息中的“某些”反应指
(3)试写出铝粉与MnO2发生的铝热反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】常温下,在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应。
(1)铁粉与水蒸气反应的化学方程式是______
(2)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法______
(3)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是________ (结合化学方程式说明):
(4)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是_______
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有人设计如图所示的装置:

请简述实验操作及原理_______
(1)铁粉与水蒸气反应的化学方程式是
(2)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法
(3)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是
(4)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有人设计如图所示的装置:

请简述实验操作及原理
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列关于铁元素及其化合物的知识:
(1)除去铁粉中混有的铝粉可以选用的试剂为_________(填序号)。
(2)在常温下,铁与水并不起反应,但在高温下,铁与水蒸气可发生反应。
该反应的化学方程式_____________________________________ ;
该反应中的还原剂是____________ ,氧化剂是___________ 。
(3)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是(用离子方程式表示)______________________________ 。
(1)除去铁粉中混有的铝粉可以选用的试剂为_________(填序号)。
| A.稀盐酸 | B.氢氧化钠溶液 | C.浓硫酸 |
该反应的化学方程式
该反应中的还原剂是
(3)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是(用离子方程式表示)
您最近一年使用:0次



