原子序数小于等于36的Q、W、X、Y、Z五种元素,其中Q是形成化合物种类最多的元素,W和Y的基态原子2p能级所含成单电子数均为2,Z的基态原子核外含有13种运动状态不同的电子。回答下列问题(涉及元素时用对应的元素符号表示):
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是______ 。
(2)1molQWX与1molWQ2Y所含σ键的比值为______ 。
(3)根据等电子体理论可以预测WXY-的空间构型为______ 。
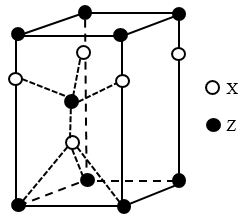
(4)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为______ 。
(5)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为。______ 。
②该化合物所属晶体类型为______ 晶体,预测其熔点应______ 金刚石(填“高于”或“低于”)。
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是
(2)1molQWX与1molWQ2Y所含σ键的比值为
(3)根据等电子体理论可以预测WXY-的空间构型为
(4)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为

(5)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为。
②该化合物所属晶体类型为
更新时间:2021-03-14 08:47:57
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
【推荐1】物质的组成与结构决定了物质的性质与变化。回答下列问题:
(1)在现代化学中,常利用_______ 上的特征谱线来鉴定元素,称为光谱分析。
(2)聚酰亚胺简式是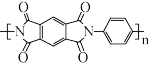
①C、N、O、H四种元素电负性由小到大的顺序是_______ (填元素符号)。
②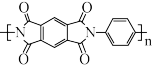 中C原子的杂化轨道类型为
中C原子的杂化轨道类型为_______ 。
(3)[Zn(IMI)4](ClO4)2是Zn2+的另一种配合物,IMI的结构为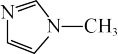 ,则1 molIMI中含有σ键的物质的量为
,则1 molIMI中含有σ键的物质的量为_______ 。
(4)NaN3中阴离子空间构型为_______ ;键角H2S_______ H2O(填“大于”“小于”或“等于”)。
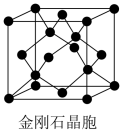
(5)金刚石与石墨都是碳的同素异形体。若碳原子半径为rnm,根据硬球接触模型,金刚石晶胞中碳原子的空间占有率为_______ (用含π的代数式表示);金刚石的密度为_______ g/cm3(写出用r和NA表示的计算式即可)
(1)在现代化学中,常利用
(2)聚酰亚胺简式是

①C、N、O、H四种元素电负性由小到大的顺序是
②
 中C原子的杂化轨道类型为
中C原子的杂化轨道类型为(3)[Zn(IMI)4](ClO4)2是Zn2+的另一种配合物,IMI的结构为
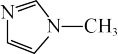 ,则1 molIMI中含有σ键的物质的量为
,则1 molIMI中含有σ键的物质的量为(4)NaN3中阴离子空间构型为
(5)金刚石与石墨都是碳的同素异形体。若碳原子半径为rnm,根据硬球接触模型,金刚石晶胞中碳原子的空间占有率为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】研究发现,铜基催化剂可以促进二氧化碳( )转换成一氧化碳(CO)、甲醛(
)转换成一氧化碳(CO)、甲醛( )或乙烯(
)或乙烯( )及乙醇(
)及乙醇( )等多碳化合物,对于“碳达峰”和“碳中和”目标的顺利实现具有积极推动作用。
)等多碳化合物,对于“碳达峰”和“碳中和”目标的顺利实现具有积极推动作用。
(1)Cu基态原子核外电子排布式为___________ ,该元素位于元素周期表第___________ 族,属于___________ 区。
(2)下列说法正确是___________(填序号)
(3)已知具有相同价电子数和相同原子数的分子或离子具有相同的结构,这一原理称为“等电子原理”。根据等电子原理,写出两个与 具有相同空间构型的分子或者离子
具有相同空间构型的分子或者离子___________ 。
(4)在海洋生物作用下形成 ,亦是减缓大气中
,亦是减缓大气中 增加的主要途径。
增加的主要途径。 中的化学键除了σ键外,还存在
中的化学键除了σ键外,还存在___________ 和大π键
(5)已和 在高温高压下所形成的晶体的晶胞如图所示,
在高温高压下所形成的晶体的晶胞如图所示, 的晶胞参数(棱长)apm,其密度为
的晶胞参数(棱长)apm,其密度为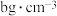 ,则阿伏伽德罗常数为
,则阿伏伽德罗常数为___________ /mol(列出计算式即可)。
 )转换成一氧化碳(CO)、甲醛(
)转换成一氧化碳(CO)、甲醛( )或乙烯(
)或乙烯( )及乙醇(
)及乙醇( )等多碳化合物,对于“碳达峰”和“碳中和”目标的顺利实现具有积极推动作用。
)等多碳化合物,对于“碳达峰”和“碳中和”目标的顺利实现具有积极推动作用。(1)Cu基态原子核外电子排布式为
(2)下列说法正确是___________(填序号)
A. , , , , 的沸点: 的沸点: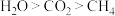 |
B. 分子中含有极性键,是极性分子 分子中含有极性键,是极性分子 |
C. 、 、 分子中碳原子的杂化方式不同 分子中碳原子的杂化方式不同 |
D.根据价层电子互斥理论, , , , , , , 分子中, 分子中, 的中心原子价层电子对数不同于其他分子 的中心原子价层电子对数不同于其他分子 |
(3)已知具有相同价电子数和相同原子数的分子或离子具有相同的结构,这一原理称为“等电子原理”。根据等电子原理,写出两个与
 具有相同空间构型的分子或者离子
具有相同空间构型的分子或者离子(4)在海洋生物作用下形成
 ,亦是减缓大气中
,亦是减缓大气中 增加的主要途径。
增加的主要途径。 中的化学键除了σ键外,还存在
中的化学键除了σ键外,还存在(5)已和
 在高温高压下所形成的晶体的晶胞如图所示,
在高温高压下所形成的晶体的晶胞如图所示, 的晶胞参数(棱长)apm,其密度为
的晶胞参数(棱长)apm,其密度为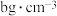 ,则阿伏伽德罗常数为
,则阿伏伽德罗常数为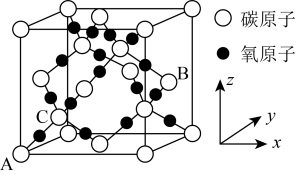
您最近一年使用:0次
【推荐3】核安全与放射性污染防治已引起广泛关注。在爆炸的核电站周围含有放射性物质 碘-131和钙-137。碘-131 —旦被人体吸入,可能会引发甲状腺肿大等疾病。
(1)与钠同主族的前四周期(包括第四周期)的三种元素X、Y、Z的第一电离能如下表:
基态Z原子倒数第二层电子的排布式为______ 。X、Y、Z三种元素形成的单质熔点由高到低的顺序为_______ (用元素符号表示),其原因为___________ .
(2)F与I同主族,BeF2分子中心原子的杂化类型为_________ ,BeF2分子是________ 分子(选填“极性”或“非极性”)。
(3)已知高碘酸有两种形式,化学式分别为H5IO6( )和HIO4 ,二者酸性强弱顺序为:H5IO6
)和HIO4 ,二者酸性强弱顺序为:H5IO6 ________ HIO4(选填">"或"<"“=”)。从电子云的重叠方式的角度分析,H5IO6分子中的化学键有________ (写出两种).
(4)131I2晶体的晶胞结构如图甲所示,该晶胞中平均含有________ 个131I原子,晶体中碘分子的排列有_________ 种不同的方向。

(5)KI的晶胞结构如图乙所示,每个K+周围紧邻的K+个数为_______ 个。KI晶体的密度为ρg.cm-3 ,K和I的原子半径分别为rkcm和rI cm,阿伏伽德罗常数的值为NA,则 KI晶胞中的空间利用率为_______ . [空间利用率=(球体积/晶胞体积)×100%,用相关字母的代数式表示即可]
(1)与钠同主族的前四周期(包括第四周期)的三种元素X、Y、Z的第一电离能如下表:
| 元素代号 | X | Y | Z |
| 第一电离能/(kJ.mol) | 520 | 496 | 419 |
(2)F与I同主族,BeF2分子中心原子的杂化类型为
(3)已知高碘酸有两种形式,化学式分别为H5IO6(
 )和HIO4 ,二者酸性强弱顺序为:H5IO6
)和HIO4 ,二者酸性强弱顺序为:H5IO6 (4)131I2晶体的晶胞结构如图甲所示,该晶胞中平均含有

(5)KI的晶胞结构如图乙所示,每个K+周围紧邻的K+个数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】B、C、N、Si是几种常见的重要非金属元素,其形成的各种化合物在自然界中广泛存在。
⑴ 基态硼原子的电子排布式为___________________________ 。C、N、Si元素原子的第一电离能由大到小的顺序为____________________________ 。
⑵ BF3与一定量的水可形成如图晶体R。
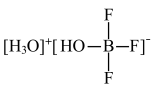
① 晶体R中各种微粒间的作用力涉及______ (填字母)。
a.离子键 b.共价键 c.配位键
d.金属键 e.范德华力
② R中阴离子的空间构型为_______________ 。
⑶ 乙二胺(H2NCH2CH2NH2)与CuCl2溶液可形成配离子(结构如图) 乙二胺分子中氮原子的杂化类型为______ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,其原因是________________________________ 。

⑷ 氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。它的晶体结构如图所示。六方相氮化硼是否含有π键?______ (填 “含”或“不含”),其质地软的原因是______________________________________ ,该物质能否导电?______ (填“能”或“不能”),其原因是_________________ 。

⑸ SiC是原子晶体,其晶胞结构类似金刚石,假设正方体的边长为a cm,估算SiC晶体的密度为_______ g∙cm−3(用含NA、a的代数式表示)。
⑴ 基态硼原子的电子排布式为
⑵ BF3与一定量的水可形成如图晶体R。
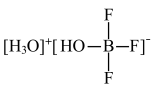
① 晶体R中各种微粒间的作用力涉及
a.离子键 b.共价键 c.配位键
d.金属键 e.范德华力
② R中阴离子的空间构型为
⑶ 乙二胺(H2NCH2CH2NH2)与CuCl2溶液可形成配离子(结构如图) 乙二胺分子中氮原子的杂化类型为

⑷ 氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。它的晶体结构如图所示。六方相氮化硼是否含有π键?

⑸ SiC是原子晶体,其晶胞结构类似金刚石,假设正方体的边长为a cm,估算SiC晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】氧化镍为绿色粉末状固体,可用作搪瓷的密着剂和着色剂,陶瓷和玻璃的颜料。也可用作电子元件材料、催化剂和蓄电池材料。工业上可通过下列两种方法制取
NiCO3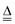 NiO+CO2↑ Ni(NO3)2·6H2O
NiO+CO2↑ Ni(NO3)2·6H2O 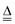 NiO+2HNO3+4H2O。
NiO+2HNO3+4H2O。
回答下列问题
(1)镍元素在元素周期表中的位置为__________ ,其价电子轨道表达式为____________________ 。
(2)上述两个反应涉及的非金属元素中第一电离能最大的元素为_________ 。其原子核外未成对电子数是__________ 。
(3)上述两个反应生成的非金属氧化物沸点较高的是_______ ,其主要原因是_________________ 。
(4)NO3-离子的空间构型是___________ ,其中心原子的杂化方式为___________ 。
(5)氧化镍晶体结构与氯化钠相似,其晶胞结构如下图,结构中氧离子采用面心立方最密堆积,镍离子的堆积方式是______________ 。
(6)纳米材料的表面原子占总原子数的比例极大,这是它有许多特殊性质的原因,假设某氧化镍纳米粒子的形状为立方体,其边长是氧化镍晶胞(如右图)的5倍,这种纳米颗粒的表面原子与总原子数的比为__________ 。
NiCO3
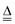 NiO+CO2↑ Ni(NO3)2·6H2O
NiO+CO2↑ Ni(NO3)2·6H2O 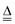 NiO+2HNO3+4H2O。
NiO+2HNO3+4H2O。回答下列问题
(1)镍元素在元素周期表中的位置为
(2)上述两个反应涉及的非金属元素中第一电离能最大的元素为
(3)上述两个反应生成的非金属氧化物沸点较高的是
(4)NO3-离子的空间构型是
(5)氧化镍晶体结构与氯化钠相似,其晶胞结构如下图,结构中氧离子采用面心立方最密堆积,镍离子的堆积方式是

(6)纳米材料的表面原子占总原子数的比例极大,这是它有许多特殊性质的原因,假设某氧化镍纳米粒子的形状为立方体,其边长是氧化镍晶胞(如右图)的5倍,这种纳米颗粒的表面原子与总原子数的比为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E的+1价阳离子的核外有3层电子且各层均处于全满状态。
(1)E元素基态原子的核外电子排布式为________________ 。
(2)B、C、D三种元素的第一电离能由小到大的顺序为_______ (填元素符号),其原因是___________________________ 。
(3)B2A4是石油炼制的重要产物之一 。B2A4分子中B原子轨道的杂化类型为________ ;1 mol B2A2分子中含________ mol σ键。
(4)已知D、E能形成晶胞结构如图所示的两种化合物,则化学式:甲为_____ ,乙为______ ;高温时,甲易转化为乙的原因为__________________________ 。
(1)E元素基态原子的核外电子排布式为
(2)B、C、D三种元素的第一电离能由小到大的顺序为
(3)B2A4是石油炼制的重要产物之一 。B2A4分子中B原子轨道的杂化类型为
(4)已知D、E能形成晶胞结构如图所示的两种化合物,则化学式:甲为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。
(1)基态Ni原子价电子中成对电子数与未成对电子数之比为_________ 。
(2)MgO与CaO这两个物质,其中熔点较高的是______ ,原因是___________________________________________ 。
(3)第二周期中,第一电离能介于B元素和N元素之间的元素有_________ 种。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合, 其结构如图所示。
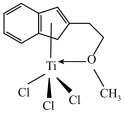
①组成M的元素中,电负性最大的是__________ (填名称)。
②M中碳原子的杂化方式为__________ 。
③M中不含__________ (填代号)。
a、π键 b、σ键 c、离子键 d、配位键
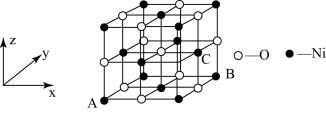
(5)NiO的晶体结构如图所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为________________ 。
(1)基态Ni原子价电子中成对电子数与未成对电子数之比为
(2)MgO与CaO这两个物质,其中熔点较高的是
(3)第二周期中,第一电离能介于B元素和N元素之间的元素有
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合, 其结构如图所示。

①组成M的元素中,电负性最大的是
②M中碳原子的杂化方式为
③M中不含
a、π键 b、σ键 c、离子键 d、配位键
(5)NiO的晶体结构如图所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】GaN是制造5G芯片的材料,氮化镓和氮化铝LED可发出紫外光。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]____ 。
(2)根据元素周期律,元素的电负性Ga____ (填“大于”或“小于”,下同)As。
(3)科学家合成了一种阳离子为“N5n+”,其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”化学式为“N8”的离子晶体,其电子式为____ ,其中的阴离子的空间构型为____ 。
(4)组成相似的CaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是________ 。
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为___ ;紧邻的As原子之间的距离为b,紧邻的As、Ca原子之间的距离为d,则b:d=____ ,该晶胞的密度为__ g ▪cm-3。(阿伏加 德罗常数用NA表示)

(1)基态Ga原子的核外电子排布式为[Ar]
(2)根据元素周期律,元素的电负性Ga
(3)科学家合成了一种阳离子为“N5n+”,其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”化学式为“N8”的离子晶体,其电子式为
(4)组成相似的CaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
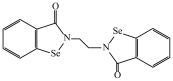
①已知Se与S在同一主族,基态Se原子的核外电子排布式为[Ar]_______ 。
②比较键角的大小:气态 分子
分子_______  离子(填“>”、“<”或“=”),原因是
离子(填“>”、“<”或“=”),原因是_______ 。
(2)富马酸亚铁(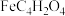 )是一种补铁剂。富马酸分子的结构模型如图所示:
)是一种补铁剂。富马酸分子的结构模型如图所示:
下列相关说法正确的是_______。
(3)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:

①该超导材料的最简化学式为_______ 。
②Fe原子的配位数为_______ 。
③该晶胞参数a=b=0.4nm,c=1.4nm。阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为_______  (列出计算式)。
(列出计算式)。
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

①已知Se与S在同一主族,基态Se原子的核外电子排布式为[Ar]
②比较键角的大小:气态
 分子
分子 离子(填“>”、“<”或“=”),原因是
离子(填“>”、“<”或“=”),原因是(2)富马酸亚铁(
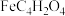 )是一种补铁剂。富马酸分子的结构模型如图所示:
)是一种补铁剂。富马酸分子的结构模型如图所示:
下列相关说法正确的是_______。
| A.富马酸分子中σ键和π键的数目比是10:3 |
B.富马酸分子中C的杂化方式有 、 、 |
| C.富马酸分子可以形成分子内氢键,使得富马酸一级和二级电离常数变大 |
| D.富马酸亚铁中各元素的电负性由大到小的顺序为O>C>H>Fe |
(3)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:

①该超导材料的最简化学式为
②Fe原子的配位数为
③该晶胞参数a=b=0.4nm,c=1.4nm。阿伏加德罗常数的值为
 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】KZnF3被认为是良好的光学基质材料,可由K2CO3、ZnF2、NH4HF2制备。回答下列问题:
(1)基态Zn原子的价电子轨道表达式为_____ ;基态N原子中未成对电子数为_____ 。
(2)O的第一电离能小于N的第一电离能的原因为_____ ;NH4HF2的组成元素的电负性由大到小的顺序为_____ (用元素符号表示)。
(3)K2CO3中阴离子的立体构型为_____ ;其中C原子的杂化方式为_____ ;HF的沸点远大于HCl的原因是_____ 。
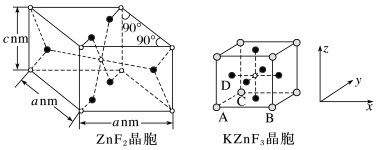
(4)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示:
①ZnF2和KZnF3晶体(晶胞顶点为K+)中,Zn的配位数之比为_____ 。
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为_____ g•cm-3(用含a、c、NA的代数式表示)。
③KZnF3晶胞中原子坐标参数A为(0,0,0),B为(1,0,0),C为(0,1,0),则D的原子坐标参数为_____ 。
(1)基态Zn原子的价电子轨道表达式为
(2)O的第一电离能小于N的第一电离能的原因为
(3)K2CO3中阴离子的立体构型为
(4)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示:

①ZnF2和KZnF3晶体(晶胞顶点为K+)中,Zn的配位数之比为
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为
③KZnF3晶胞中原子坐标参数A为(0,0,0),B为(1,0,0),C为(0,1,0),则D的原子坐标参数为
您最近一年使用:0次
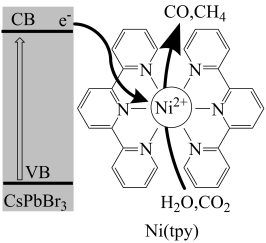
【推荐2】浙江师范大学的研究团队研究获得了一类具有高活性和选择性的钙钛矿光催化剂(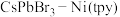 ),这一成果发表在2020年1月Chem. Mater.上。带有负电荷的CsPbBr3将带正电的
),这一成果发表在2020年1月Chem. Mater.上。带有负电荷的CsPbBr3将带正电的 固定在其表面,用于可见光驱动CO2还原。
固定在其表面,用于可见光驱动CO2还原。
(1)写出Ni基态原子的价电子排布图(轨道表达式)___________________ 。
(2)C、N、O、Cs、Pb元素第一电离能由大到小的顺序是____________________ 。
(3) 是二价阳离子,该离子中氮原子的杂化类型为
是二价阳离子,该离子中氮原子的杂化类型为_________ ,该离子结构中含有_________ (填字母)。
a.离子键 b.配位键 C.π键 d.氢键
(4)某些氧化物的熔点数据如下表所示:
解释表中氧化物之间熔点差异的原因:______________________________ 。
(5)氮化镓是一种半导体材料。晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。
①与同一个Ga原子相连的N原子构成的空间构型为__________ ;
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如图,则2、3、4原子的分数坐标不可能的是( )

a.(0.75,0.25,0.25) b.(0.25,0.75,0.75)
c.(0.25,0.75,0.25) d.(0.75,0.75,0.75)
③ GaN晶体中N和N的原子核间距为a pm,GaN摩尔质量为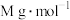 ,阿伏加 德罗常数的值为NA,则GaN晶体的密度为
,阿伏加 德罗常数的值为NA,则GaN晶体的密度为___________  (
(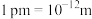 )。
)。
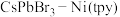 ),这一成果发表在2020年1月Chem. Mater.上。带有负电荷的CsPbBr3将带正电的
),这一成果发表在2020年1月Chem. Mater.上。带有负电荷的CsPbBr3将带正电的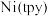 固定在其表面,用于可见光驱动CO2还原。
固定在其表面,用于可见光驱动CO2还原。
(1)写出Ni基态原子的价电子排布图(轨道表达式)
(2)C、N、O、Cs、Pb元素第一电离能由大到小的顺序是
(3)
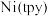 是二价阳离子,该离子中氮原子的杂化类型为
是二价阳离子,该离子中氮原子的杂化类型为a.离子键 b.配位键 C.π键 d.氢键
(4)某些氧化物的熔点数据如下表所示:
| 氧化物 | CO2 | Cs2O | PbO |
| 熔点/℃ | -56.6 | 490 | 888 |
解释表中氧化物之间熔点差异的原因:
(5)氮化镓是一种半导体材料。晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。
①与同一个Ga原子相连的N原子构成的空间构型为
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如图,则2、3、4原子的分数坐标不可能的是

a.(0.75,0.25,0.25) b.(0.25,0.75,0.75)
c.(0.25,0.75,0.25) d.(0.75,0.75,0.75)
③ GaN晶体中N和N的原子核间距为a pm,GaN摩尔质量为
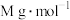 ,阿伏加 德罗常数的值为NA,则GaN晶体的密度为
,阿伏加 德罗常数的值为NA,则GaN晶体的密度为 (
(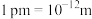 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】我国科学家研究发现AgCrS2(AMX2家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态铬原子M层的电子排布式为_______ ;基态硫原子核外电子中含有_______ 个未成对电子。
(2)同周期元素Si、P、S的电负性由大到小的顺序为_______ (用元素符号表示),O、S为同主族元素,H2O的键角比H2S大的原因是_______ 。
(3)硫元素能形成多种微粒如H2S、SO2、SO3、SO 、SO
、SO 等。SO2的立体构型为
等。SO2的立体构型为_______ ,SO3的中心原子的价层电子对数为_______ 。
(4)CrO5中Cr元素化合价为+6价,常温下呈蓝色,则其结构式可能为_______ (填标号)。
(5)某含铬化合物立方晶胞如图所示。该晶体的化学式为_______ ;与Cr最近的氧原子的个数为_______ ;Ca和Cr的最近距离为anm,设NA为阿伏加德罗常数的值,则该晶体密度为_______ (填含a、NA的表达式)g•cm-3。
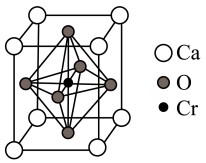
(1)基态铬原子M层的电子排布式为
(2)同周期元素Si、P、S的电负性由大到小的顺序为
(3)硫元素能形成多种微粒如H2S、SO2、SO3、SO
 、SO
、SO 等。SO2的立体构型为
等。SO2的立体构型为(4)CrO5中Cr元素化合价为+6价,常温下呈蓝色,则其结构式可能为
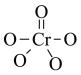 |  |  |
| A | B | C |

您最近一年使用:0次



