有A、B、C、D四种元素,其中A和B原子都有1个未成对电子,A+比B-少一个电子层。B原子得一个电子填入3p轨道后,3p轨道已充满。C原子的p轨道中有3个未成对电子,其气态氢化物的水溶液的pH在同族氢化物中最大。D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D40%,且其核内质子数等于中子数。据此判断:
(1)A是__ ,B是___ ,C是___ ,D是___ 。(填元素名称)
(2)B-的电子排布式___ ,A+的结构示意图___ ,D原子的轨道表示式__ 。
(3)在A、B、D三种元素的简单离子中,半径最小的是___ ,其离子还原性最强的是__ 。(填离子符号)
(4)AB电子式___ 。
(1)A是
(2)B-的电子排布式
(3)在A、B、D三种元素的简单离子中,半径最小的是
(4)AB电子式
更新时间:2021-03-15 17:29:12
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】元素周期表前18位元素A、B、C、D核电荷数依次增大。A元素原子核内无中子,B元素原子M层电子数比最内层的电子数多1个,C元素的原子最外层电子数是K层电子数的3倍,D-离子电子层结构与氩原子的电子层结构相同。由此推断:
(1)A、B、C、D元素符号依次是_______ 、_______ 、_______ 、_______ 。
(2)①A原子的结构示意图为_______ ;
②C离子的结构示意图为_______ 。
(3)B离子的电子式为_______ ;
(4)D-的电子式为_______ 。
(5)B单质和C单质反应生成的化合物的化学式是_______ 。
(6)与B离子电子层结构相同的微粒有_______ 。(任意写出4种即可)
(1)A、B、C、D元素符号依次是
(2)①A原子的结构示意图为
②C离子的结构示意图为
(3)B离子的电子式为
(4)D-的电子式为
(5)B单质和C单质反应生成的化合物的化学式是
(6)与B离子电子层结构相同的微粒有
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】我国的天宫空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。
(1)镓的原子结构示意图为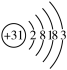 ,其在元素周期表中的位置是
,其在元素周期表中的位置是___________ 。
(2)GaAs熔融状态不能导电,据此判断它可能是___________ (填“共价”或“离子”)化合物。
(3) 基态As原子电子排布式为___________ ;电子占据最高能级的电子云轮廓图为___________ 形。
(4)As与P同族且相邻。磷的最外层电子的轨道表示式为___________ 。
(5)As与Se同周期且相邻,第一电离能As___________ Se;电负性As___________ Se(填“>”或“<”)。
(6) 用
用 还原生成
还原生成 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为___________ , 沸点比
沸点比 的
的___________ (填“高”或“低”),原因是:___________ 。
(1)镓的原子结构示意图为
 ,其在元素周期表中的位置是
,其在元素周期表中的位置是(2)GaAs熔融状态不能导电,据此判断它可能是
(3) 基态As原子电子排布式为
(4)As与P同族且相邻。磷的最外层电子的轨道表示式为
(5)As与Se同周期且相邻,第一电离能As
(6)
 用
用 还原生成
还原生成 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为 沸点比
沸点比 的
的
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】A、 B、C、D、E是5种短周期主族元素,它们的原子序数依次增大。A原子次外层电子数与最外层电子数之比为1:2;B的阴离子和C的阳离子具有相同的电子层结构,B与C的单质在不同条件下反应,生成两种阴阳离子个数比都为1:2的化合物F和G,G的相对分子质量大于F,D的L层电子数等于K、M两个电子层上的电子数之和,完成下列空格:
(1)请在下图中用“实线”画出金属元素与非金属元素的分界线,并在相应的位置上填上A、B两种元素的元素符号_______ 。
(2) D元素位于周期表是 _______ 。
(3)写出C元素的最高价氧化物对应水化物和E元素的最高价氧化物对应水化物反应的化学方程式:_______ 。
(4)将FeSO4溶液加到少量G粉末中,溶液中产生红褐色沉淀,溶液表面没有气泡,写出反应的离子方程式:_______ 。
(5)B、E两元素氢化物沸点高低顺序是_______ (用分子式表示),并用物质结构知识解释原因_______ 。
(6)非金属性强弱比较:D_______ E(填写“>”“=”或“<”),写出一个化学方程式加以验证:_______ 。
(7)化合物H由D和B两种元素组成,且所有原子的最外层均满足8电子稳定结构,写出H的结构式:_______ 。
(8)已知铁原子最外层有2个电子,画出铁的原子结构示意图:_______ 。
(1)请在下图中用“实线”画出金属元素与非金属元素的分界线,并在相应的位置上填上A、B两种元素的元素符号
| H | He | |||||||||||||||||
| Fr | Og |
(3)写出C元素的最高价氧化物对应水化物和E元素的最高价氧化物对应水化物反应的化学方程式:
(4)将FeSO4溶液加到少量G粉末中,溶液中产生红褐色沉淀,溶液表面没有气泡,写出反应的离子方程式:
(5)B、E两元素氢化物沸点高低顺序是
(6)非金属性强弱比较:D
(7)化合物H由D和B两种元素组成,且所有原子的最外层均满足8电子稳定结构,写出H的结构式:
(8)已知铁原子最外层有2个电子,画出铁的原子结构示意图:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】有A、B、C、D、E五种元素。其相关信息如下:
回答下列问题:
(1)写出元素符号B:_______ ,C:_______ ,E:_______ 。
(2)F元素可形成F2+和F3+,其中较稳定的是F3+,原因是_______ 。
(3)A和C形成的18电子分子的结构式_______ 。
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有_______ (填序号)。
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键
[E(CA3)4]2+具有对称的空间构型,若[E(CA3)4]2+中的两个CA3被两个其他基团取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为_______ (填字母)。
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,这是有关“湿法炼铜”的最早文献记录。若向盛装有硫酸铜水溶液的试管里加入氨水,首先生成蓝色沉淀,继续滴加氨水,得到深蓝色的透明溶液。请写出蓝色沉淀溶解的离子反应方程式:_______ 。
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道中有三个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层上有两个运动状态不同的电子 |
| E | E能与氧形成砖红色E2O和黑色的EO两种氧化物 |
| F | 基态原子3d能级上有6个电子 |
(1)写出元素符号B:
(2)F元素可形成F2+和F3+,其中较稳定的是F3+,原因是
(3)A和C形成的18电子分子的结构式
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键
[E(CA3)4]2+具有对称的空间构型,若[E(CA3)4]2+中的两个CA3被两个其他基团取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,这是有关“湿法炼铜”的最早文献记录。若向盛装有硫酸铜水溶液的试管里加入氨水,首先生成蓝色沉淀,继续滴加氨水,得到深蓝色的透明溶液。请写出蓝色沉淀溶解的离子反应方程式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】碳、硅、铁、铜、铝、钛是重要的材料元素。请回答下列有关问题:
(1)上述元素中属于主族元素的是___________ (填写元素符号,下同),在元素周期表d区的元素是___________ 。
(2)原子核外电子含有四个电子层的元素是___________ ,基态原子的原子轨道中未成对电子数最多的是___________ 。
(3)基态钛原子价电子的轨道表示式为___________ 。
(4)基态铜原子的价电子排布式为3d104s1,由此可判断铜在元素周期表中位于第___________ 周期___________ 族。
(1)上述元素中属于主族元素的是
(2)原子核外电子含有四个电子层的元素是
(3)基态钛原子价电子的轨道表示式为
(4)基态铜原子的价电子排布式为3d104s1,由此可判断铜在元素周期表中位于第
您最近一年使用:0次
【推荐3】研究发现,在CO2低压合成甲醇反应CO23H2CH3OHH2O中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为________ 。元素Mn与O中,第一电离能较大的是________ ,基态原子核外未成对电子数较多的是________ 。
(2)CO2和CH3OH分子中C原子的杂化形式分别为________ 和________ 。
(3)比较CO2和H2O沸点________ ,原因是________ 。
(4)MnNO3中的化学键除了σ键外,还存在________ 。
(1)Co基态原子核外电子排布式为
(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)比较CO2和H2O沸点
(4)MnNO3中的化学键除了σ键外,还存在
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】磷酸亚铁锂( )可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用
)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用 、
、 、LiCl和苯胺等作为原料制备。回答下列问题:
、LiCl和苯胺等作为原料制备。回答下列问题:
(1)苯胺与甲苯(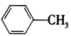 )的相对分子质量相近,但苯胺的熔点(-5.9℃)沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是___________ 。
(2) 中,电负性最高的元素是
中,电负性最高的元素是___________ ;P的___________ 杂化轨道与O的2p轨道形成___________ 键。
(3) 和
和 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
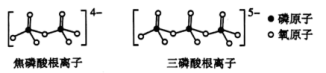
这类磷酸根离子的化学式可用通式表示为___________ (用n代表P原子数)。
 )可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用
)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用 、
、 、LiCl和苯胺等作为原料制备。回答下列问题:
、LiCl和苯胺等作为原料制备。回答下列问题:(1)苯胺与甲苯(
 )的相对分子质量相近,但苯胺的熔点(-5.9℃)沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(2)
 中,电负性最高的元素是
中,电负性最高的元素是(3)
 和
和 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
这类磷酸根离子的化学式可用通式表示为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D、E、F、G、W是原子序数依次增大的8种元素,A元素原子的2p原子轨道上有2个未成对的电子,B元素在同周期中原子半径最大,与A可形成原子个数比为1:1和2:1的两种化合物,C单质是一种常见的半导体材料,F有9个原子轨道,且只有一个未成对电子,没有空轨道,G的单质是一种常见金属,其+2价离子G2+有4个未成对电子,W能形成红色(或砖红色)的W2A和黑色的WA两种化合物。
(1)C元素在元素周期表中的位置___________ ,W位于元素周期表___________ 区,W的简化电子排布式___________ 。
(2)EF2中心原子杂化轨道类型___________ ,EA 的VSEPR模型
的VSEPR模型___________ ,EA 的空间构型
的空间构型___________ 。
(3)D、E、F三元素第一电离能从大到小的顺序是___________ (用元素符号及“ ”表示)。
”表示)。
(4)A、B、C、D四元素电负性由大到小顺序___________ (用元素符号及“ ”表示)。
”表示)。
(5)G3+比G2+稳定,原因是___________ 。
(1)C元素在元素周期表中的位置
(2)EF2中心原子杂化轨道类型
 的VSEPR模型
的VSEPR模型 的空间构型
的空间构型(3)D、E、F三元素第一电离能从大到小的顺序是
 ”表示)。
”表示)。(4)A、B、C、D四元素电负性由大到小顺序
 ”表示)。
”表示)。(5)G3+比G2+稳定,原因是
您最近一年使用:0次



