我国的天宫空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。
(1)镓的原子结构示意图为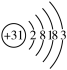 ,其在元素周期表中的位置是
,其在元素周期表中的位置是___________ 。
(2)GaAs熔融状态不能导电,据此判断它可能是___________ (填“共价”或“离子”)化合物。
(3) 基态As原子电子排布式为___________ ;电子占据最高能级的电子云轮廓图为___________ 形。
(4)As与P同族且相邻。磷的最外层电子的轨道表示式为___________ 。
(5)As与Se同周期且相邻,第一电离能As___________ Se;电负性As___________ Se(填“>”或“<”)。
(6) 用
用 还原生成
还原生成 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为___________ , 沸点比
沸点比 的
的___________ (填“高”或“低”),原因是:___________ 。
(1)镓的原子结构示意图为
 ,其在元素周期表中的位置是
,其在元素周期表中的位置是(2)GaAs熔融状态不能导电,据此判断它可能是
(3) 基态As原子电子排布式为
(4)As与P同族且相邻。磷的最外层电子的轨道表示式为
(5)As与Se同周期且相邻,第一电离能As
(6)
 用
用 还原生成
还原生成 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为 沸点比
沸点比 的
的
更新时间:2023-06-07 11:50:16
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】当今社会,各国治理污染的压力都很大,如何变废为宝,合理利用资源,是摆在科学家面前的课题。科学家设计在催化剂表面利用 还原氮的氧化物的一种反应机理如图所示。
还原氮的氧化物的一种反应机理如图所示。
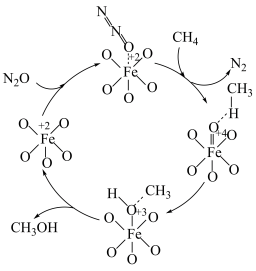
回答下列问题:
(1)基态Fe原子与基态 离子中未成对的电子数之比为
离子中未成对的电子数之比为__________ 。
(2)第二周期第一电离能比N大的主族元素为__________ (填化学式)。上述历程中涉及反应的非金属电负性由大到小的顺序为__________ (填化学式)。
(3)硝酸根离子的空间构型为__________ ,其中N的杂化轨道类型为__________ 。
(4) 中化学键类型有
中化学键类型有______ (填选项字母),甲醇易溶于水的原因是__________ 。
A.非极性共价键 B.氢键 C. 键 D.极性共价键
键 D.极性共价键
(5)铁的晶胞类型有多种,其中图甲中与一个铁原子等距离且最近的铁原子有_______ 个,图乙所示晶胞的密度为__________  (用含有a、
(用含有a、 的代数式表示)。
的代数式表示)。

 还原氮的氧化物的一种反应机理如图所示。
还原氮的氧化物的一种反应机理如图所示。
回答下列问题:
(1)基态Fe原子与基态
 离子中未成对的电子数之比为
离子中未成对的电子数之比为(2)第二周期第一电离能比N大的主族元素为
(3)硝酸根离子的空间构型为
(4)
 中化学键类型有
中化学键类型有A.非极性共价键 B.氢键 C.
 键 D.极性共价键
键 D.极性共价键(5)铁的晶胞类型有多种,其中图甲中与一个铁原子等距离且最近的铁原子有
 (用含有a、
(用含有a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】美国芝加哥大学化学研究所近日揭示了WO3/CeO2-TiO2双催化剂在低温下催化氮的污染性气体转化为无毒气体,其过程如图所示
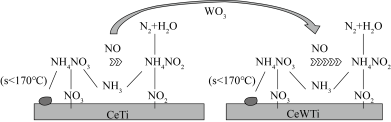
(1)Ti价电子排布式为______________ ,其能量最高的能层是___________ 。
(2)N、O、H三种原子的电负性由大到小的顺序为___________________ 。
(3)NO2-的空间构型为___________ ,与NO3-互为等电子体的分子为_______________
(4)WO3可作为苯乙烯氧化的催化剂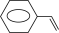 +H2O2
+H2O2
 +H2O
+H2O
① 中碳原子的杂化方式为
中碳原子的杂化方式为_________ 。
②1molH2O2中δ键个数为____________ 。
③ 属于
属于______________ 晶体。
(5)W和Ti可形成金属互化物,某W和Ti的金属互化物如图所示,则该晶体的化学式为__________ 。
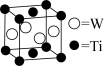
(6)金属钛的晶体堆积方式为____________

(1)Ti价电子排布式为
(2)N、O、H三种原子的电负性由大到小的顺序为
(3)NO2-的空间构型为
(4)WO3可作为苯乙烯氧化的催化剂
 +H2O2
+H2O2
 +H2O
+H2O①
 中碳原子的杂化方式为
中碳原子的杂化方式为②1molH2O2中δ键个数为
③
 属于
属于(5)W和Ti可形成金属互化物,某W和Ti的金属互化物如图所示,则该晶体的化学式为

(6)金属钛的晶体堆积方式为
您最近一年使用:0次
【推荐3】磷、硫、氯、砷等是农药中的重要组成元素。回答下列问题:
(1)基态砷原子的核外子排布式为_______ 。
(2)生产农药的原料PSCl3中P、S、Cl的第一电离能由大到小的顺序为_______ ,电负性由大到小的顺序为_______ 。
(3)AsCl3分子的立体构型为_______ ,其中As的杂化轨道类型为_______ 。
(4)H2O与H2S为同族元素的氢化物,H2O可以形成H9O 或H3O+,而H2S几乎不能形成类似的H9S
或H3O+,而H2S几乎不能形成类似的H9S 或H3S+,其原因是
或H3S+,其原因是_______ 。
(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2 000 ℃,其晶胞结构如图所示。
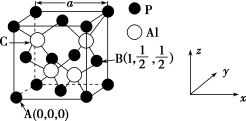
①磷化铝的晶体类型为_______ 。
②A、B点的原子坐标如图所示,则C点的原子坐标为_______ 。
③磷化铝的晶胞参数a=546.35 pm,其密度为_______ g·cm-3(列出计算式即可,用NA表示阿伏加德罗常数的值)。
(1)基态砷原子的核外子排布式为
(2)生产农药的原料PSCl3中P、S、Cl的第一电离能由大到小的顺序为
(3)AsCl3分子的立体构型为
(4)H2O与H2S为同族元素的氢化物,H2O可以形成H9O
 或H3O+,而H2S几乎不能形成类似的H9S
或H3O+,而H2S几乎不能形成类似的H9S 或H3S+,其原因是
或H3S+,其原因是(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2 000 ℃,其晶胞结构如图所示。

①磷化铝的晶体类型为
②A、B点的原子坐标如图所示,则C点的原子坐标为
③磷化铝的晶胞参数a=546.35 pm,其密度为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】现有部分短周期元素的性质或原子结构如表:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是_____ 。
(2)元素Y与氢元素形成一种离子YH ,写出某溶液中含该微粒的电子式
,写出某溶液中含该微粒的电子式_____ ,如何检验该离子_____ 。
(3)元素Z在周期表中的位置_____ ,元素Z与元素T相比,非金属性较强的是_____ (用元素符号表示),下列表述中能证明这一事实的是_____ (填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下,Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质性质的差异性是学习化学的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是_____ ,理由是_____ 。
| 元素编号 | 元素性质或原子结构 |
| T | M层上有6个电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| W | 其单质既能跟酸反应,又能跟强碱反应,都产生H2 |
(2)元素Y与氢元素形成一种离子YH
 ,写出某溶液中含该微粒的电子式
,写出某溶液中含该微粒的电子式(3)元素Z在周期表中的位置
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下,Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质性质的差异性是学习化学的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为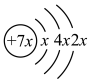 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)A为____ (写出元素符号,下同);
(2)B为____ ,简化电子排布式是____ ;
(3)C为____ ,外围电子排布式是____ ;
(4)D为____ ,轨道表示式是____ ;
(5)E原子结构示意图是____ 。
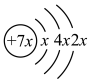 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:(1)A为
(2)B为
(3)C为
(4)D为
(5)E原子结构示意图是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】短周期主族元素A、B、C、D、E原子序数依次增大。A、E同主族,E原子最外层上的电子数是D原子最外层电子数的4倍,D离子与C2-具有相同核外电子排布。
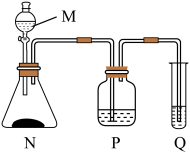
试回答下列问题:
(1)元素E在元素周期表中的位置是______ 。
(2)A和E最高价氧化物对应的水化物,酸性较弱的为_____ 。若用图中装置验证这两种酸的酸性强弱,则在仪器P中加入的试剂为_____ ,Q中观察到的实验现象是_____ 。
(3)由以上五种元素组成的物质,其组成和结构信息如下表:
①a含有的化学键有_____ 。
②b与c反应的化学方程式为_____ 。

试回答下列问题:
(1)元素E在元素周期表中的位置是
(2)A和E最高价氧化物对应的水化物,酸性较弱的为
(3)由以上五种元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A、C、D的盐 |
| b | C、D组成的化合物,且原子数之比为1∶1 |
| c | 化学组成为AC2 |
②b与c反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】氢原子是最轻的原子,人们曾预言它可能是所有元素之母。碳是地球上组成生命的最基本的 元素之一。按要求回答:
(1)宇宙中含量最多的元素是氢和______ 。基态碳原子的核外电子占有______ 个原子轨道。
(2)光化学烟雾中除了含有 NOx 外,还含有 HCOOH、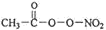 (PAN)等二次污染物。
(PAN)等二次污染物。
①PAN 中 C 的杂化方式有______ 。1mol PAN 中含有的σ键数目为______ 。组成PAN 的元素的电负性大小顺序为______ 。
②相同压强下,HCOOH 的沸点比 CH3OCH3______ (填“高”或“低”),
(3)水溶液中有 H3O+、H5O2+、H9O4+ 等微粒的形式。请画出 H5O2的结构式:______ 。
(4)硅和碳在同一主族。下图为 SiO2晶胞中 Si 原子沿 z 轴方向在 xy 平面的投影图(即俯视图),其 中 O原子略去,Si 原子旁标注的数字表示每个 Si 原子位于 z 轴的高度,则 SiA 与 SiB 之间的距离是______ nm。
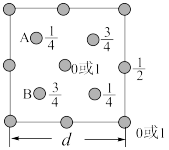 (d 的单位为 nm)
(d 的单位为 nm)
(1)宇宙中含量最多的元素是氢和
(2)光化学烟雾中除了含有 NOx 外,还含有 HCOOH、
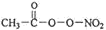 (PAN)等二次污染物。
(PAN)等二次污染物。①PAN 中 C 的杂化方式有
②相同压强下,HCOOH 的沸点比 CH3OCH3
(3)水溶液中有 H3O+、H5O2+、H9O4+ 等微粒的形式。请画出 H5O2的结构式:
(4)硅和碳在同一主族。下图为 SiO2晶胞中 Si 原子沿 z 轴方向在 xy 平面的投影图(即俯视图),其 中 O原子略去,Si 原子旁标注的数字表示每个 Si 原子位于 z 轴的高度,则 SiA 与 SiB 之间的距离是
 (d 的单位为 nm)
(d 的单位为 nm)
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】由P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,试回答下列问题:
(1)基态Cl原子的核外电子排布式为___________ 。P、S、Cl的第一电离能由大到小的顺序为___________
(2) 分子中中心原子的杂化轨道类型是
分子中中心原子的杂化轨道类型是___________ ,该分子的空间结构为___________ 。
(3)已知NiO的晶体结构如图1所示,若NiO晶胞中A的坐标为(0,0,0),B的坐标为(1,1,0),则C的坐标为___________ 。

(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为 作密置单层排列,
作密置单层排列, 填充其中(如图2所示),已知
填充其中(如图2所示),已知 的半径为am,则每平方米分散的该晶体的质量为
的半径为am,则每平方米分散的该晶体的质量为___________ g(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)基态Cl原子的核外电子排布式为
(2)
 分子中中心原子的杂化轨道类型是
分子中中心原子的杂化轨道类型是(3)已知NiO的晶体结构如图1所示,若NiO晶胞中A的坐标为(0,0,0),B的坐标为(1,1,0),则C的坐标为

(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为
 作密置单层排列,
作密置单层排列, 填充其中(如图2所示),已知
填充其中(如图2所示),已知 的半径为am,则每平方米分散的该晶体的质量为
的半径为am,则每平方米分散的该晶体的质量为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】基于CH3NH3PbI3的有机-无机杂化钙钛矿被认为是下一代太阳能电池的可选材料之一、
(1)基态Pb原子中,电子占据的最高能级为___________ 。写出基态C原子的价电子排布图___________ 。
(2)合成CH3NH3PbI3需要使用的主要试剂有CH3NH2、HI、PbI2、DMF(结构如图所示)。
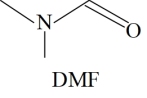
①PbI2分子的构型是___________ 。
②DMF中,N原子的杂化方式是___________ 。C、N、O三种元素第一电离能性从大到小的顺序是___________ 。DMF中存在的化学键键型不包括下列说法中的___________ (填序号)。
A. 极性键 B. 非极性键 C. 离子键 D. π键
(3)理想的钙钛矿晶胞如图所示
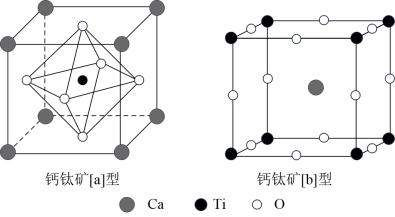
①从图中任意一种晶胞可确定钙钛矿的分子式是___________ ;
②设NA为阿伏加德罗常数的值,若已知钙钛矿[b]型的密度约为ρ g/cm3,则钙钛矿[b]型晶胞中两个O原子的最短距离是___________ nm。
(1)基态Pb原子中,电子占据的最高能级为
(2)合成CH3NH3PbI3需要使用的主要试剂有CH3NH2、HI、PbI2、DMF(结构如图所示)。

①PbI2分子的构型是
②DMF中,N原子的杂化方式是
A. 极性键 B. 非极性键 C. 离子键 D. π键
(3)理想的钙钛矿晶胞如图所示

①从图中任意一种晶胞可确定钙钛矿的分子式是
②设NA为阿伏加德罗常数的值,若已知钙钛矿[b]型的密度约为ρ g/cm3,则钙钛矿[b]型晶胞中两个O原子的最短距离是
您最近一年使用:0次



