短周期主族元素A、B、C、D、E原子序数依次增大。A、E同主族,E原子最外层上的电子数是D原子最外层电子数的4倍,D离子与C2-具有相同核外电子排布。
试回答下列问题:
(1)元素E在元素周期表中的位置是______ 。
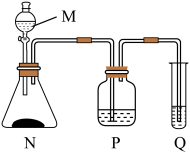
(2)A和E最高价氧化物对应的水化物,酸性较弱的为_____ 。若用图中装置验证这两种酸的酸性强弱,则在仪器P中加入的试剂为_____ ,Q中观察到的实验现象是_____ 。
(3)由以上五种元素组成的物质,其组成和结构信息如下表:
①a含有的化学键有_____ 。
②b与c反应的化学方程式为_____ 。

试回答下列问题:
(1)元素E在元素周期表中的位置是
(2)A和E最高价氧化物对应的水化物,酸性较弱的为
(3)由以上五种元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A、C、D的盐 |
| b | C、D组成的化合物,且原子数之比为1∶1 |
| c | 化学组成为AC2 |
②b与c反应的化学方程式为
更新时间:2020-06-28 08:56:24
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】元素周期律是重要的化学学习工具。随着原子序数变化,7种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
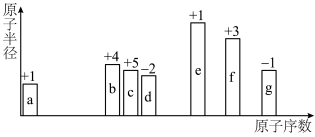
(1)b在元素周期表中的位置是_______ 周期_______ 族。7种元素中金属性最强的是_______ (用元素符号表示,下同),与d处于同一主族的短周期元素是_______ 。
(2)b和c的最高价氧化物的水化物中,酸性较强的是_______ (用化学式表示,下同),c和d的简单氢化物的稳定性较弱的是_______ 。
(3)d和f形成的化合物为_______ (用化学式表示),该化合物在熔融状态下能导电,属于_______ 化合物(填“离子”或“共价”),该化合物与盐酸反应的离子方程式为_______ 。
(4)d、e的单质在加热条件下反应生成的化合物中存在的化学键有_______ 。
(5)用电子式表示由a、c两种元素形成的化合物的形成过程______________ 。

(1)b在元素周期表中的位置是
(2)b和c的最高价氧化物的水化物中,酸性较强的是
(3)d和f形成的化合物为
(4)d、e的单质在加热条件下反应生成的化合物中存在的化学键有
(5)用电子式表示由a、c两种元素形成的化合物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】现有部分短周期主族元素的有关信息,如下表:
(1)T的一种单质相对分子质量为256,能溶于CS2,该单质的分子式为____________ (用元素符号表示);指出T单质的一种用途_____________________________ 。
⑵写出Z氢氧化物的电离方程式:__________________________ ;下列酸中不能溶解Z单质的是_________
a.浓硝酸 b.热浓硫酸 c.浓盐酸 d.稀硝酸
⑶可用于扑灭Y单质燃烧引起的火灾的物质是___________ 。
a.二氧化碳 b.水 c.沙土 d.干粉(主要成分为NaHCO3)
⑷.元素X元素T相比,非金属性较强的是__________ (用元素符号表示)。下列表述中能证明这一事实的是____________ 。
a.在溶液中T的单质能置换出X的单质
b.X的气态氢化物比T的气态氢化物更稳定
c.T的无氧酸钠盐溶液pH>7,而X的+7价含氧酸钠盐溶液pH=7
| 元素编号 | 元素性质或原子结构 |
| T | 核外有5种不同能量的电子,其中有2个未成对电子 |
| X | 最高化合价为+7价 |
| Y | 短周期主族元素原子中半径最大 |
| Z | 地壳中含量最多的金属 |
(1)T的一种单质相对分子质量为256,能溶于CS2,该单质的分子式为
⑵写出Z氢氧化物的电离方程式:
a.浓硝酸 b.热浓硫酸 c.浓盐酸 d.稀硝酸
⑶可用于扑灭Y单质燃烧引起的火灾的物质是
a.二氧化碳 b.水 c.沙土 d.干粉(主要成分为NaHCO3)
⑷.元素X元素T相比,非金属性较强的是
a.在溶液中T的单质能置换出X的单质
b.X的气态氢化物比T的气态氢化物更稳定
c.T的无氧酸钠盐溶液pH>7,而X的+7价含氧酸钠盐溶液pH=7
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】选相应实验目的填入下述括号内:
A、验证同主族元素的金属性从上至下递增
B、验证同主族元素的非金属性从上至下递减
C、验证同周期元素的金属性从左至右递减
D、验证同周期元素的非金属性从左至右递增
实验1、比较钠、镁、铝分别与水反应的快慢______
实验2、溴化钠溶液中滴入氯水,碘化钠溶液中滴入溴水______
实验3、比较钾、钠分别与水反应的快慢______
实验4、在 、
、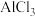 溶液中逐滴加入NaOH溶液至过量,从而比较
溶液中逐滴加入NaOH溶液至过量,从而比较 、
、 的碱性
的碱性 ______ .
A、验证同主族元素的金属性从上至下递增
B、验证同主族元素的非金属性从上至下递减
C、验证同周期元素的金属性从左至右递减
D、验证同周期元素的非金属性从左至右递增
实验1、比较钠、镁、铝分别与水反应的快慢
实验2、溴化钠溶液中滴入氯水,碘化钠溶液中滴入溴水
实验3、比较钾、钠分别与水反应的快慢
实验4、在
 、
、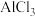 溶液中逐滴加入NaOH溶液至过量,从而比较
溶液中逐滴加入NaOH溶液至过量,从而比较 、
、 的碱性
的碱性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答下列问题:

已知:亚硫酸 为二元弱酸,不稳定,易分解生成
为二元弱酸,不稳定,易分解生成 气体和
气体和 。
。
(1)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:___________ ;用电子式表示⑤和⑧以数目比2:1形成化合物的过程___________ 。
(2)④⑤⑧形成的简单离子半径由大到小的顺序为___________ (填离子符号);⑦⑧⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为___________ (填化学式)。
(3)元素④和元素⑧的最简单氢化物的沸点由大到小的顺序为___________ (填化学式)。
(4)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应,写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式:___________ 。
(5)有两种化合物A和B都由①④⑤⑧四种元素组成。若A与B在水溶液中能发生反应产生气泡,则该反应的离子方程式为___________ 。

已知:亚硫酸
 为二元弱酸,不稳定,易分解生成
为二元弱酸,不稳定,易分解生成 气体和
气体和 。
。(1)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:
(2)④⑤⑧形成的简单离子半径由大到小的顺序为
(3)元素④和元素⑧的最简单氢化物的沸点由大到小的顺序为
(4)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应,写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式:
(5)有两种化合物A和B都由①④⑤⑧四种元素组成。若A与B在水溶液中能发生反应产生气泡,则该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】科学家合成一种新化合物(如图所示)。其中W、X、Y、Z为短周期元素,且位于同一周期,W是所在周期中第一电离能最小的元素,Y元素基态原子的未成对电子数等于其电子层数,Z元素的原子核外最外层电子数是X元素原子核外电子数的一半。回答下列问题:
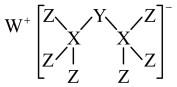
(1)W、X、Y、Z原子半径由大到小的顺序为
(2)Z的核外电子排布式为
(3)基态X原子价电子轨道表示式为
(4)W元素基态原子核外电子有
(5)X的电负性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素周期表揭示了化学元素间的内在联系,对化学学习和研究有很重要的作用。下表列出了①~⑧八种元素在周期表中的位置:
请按要求回答下列问题:
(1)画出⑧的原子结构示意图________ 。
(2)由③、④、⑦四种元素形成的简单离子半径由大到小的顺序是________ (用离子符号表示)。
(3)由元素①和②形成的最简单化合物甲的电子式为________ ,由元素③和⑥形成化合物乙,则乙与NaOH溶液发生反应的化学方程式为________ 。
(4)硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在元素周期表中的位置如图所示:
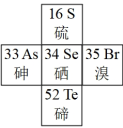
i.在元素周期表中位置表示为________ 。
ii.关于硒的下列说法中正确的是________ 。
A. 既有氧化性又有还原性 B.原子半径由大到小顺序:
既有氧化性又有还原性 B.原子半径由大到小顺序: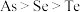
C.热稳定性: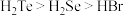 D.酸性:
D.酸性: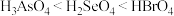
族 周期 | IA | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
(1)画出⑧的原子结构示意图
(2)由③、④、⑦四种元素形成的简单离子半径由大到小的顺序是
(3)由元素①和②形成的最简单化合物甲的电子式为
(4)硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在元素周期表中的位置如图所示:

i.在元素周期表中位置表示为
ii.关于硒的下列说法中正确的是
A.
 既有氧化性又有还原性 B.原子半径由大到小顺序:
既有氧化性又有还原性 B.原子半径由大到小顺序: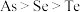
C.热稳定性:
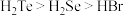 D.酸性:
D.酸性: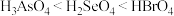
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1︰1的离子化合物A,X与Z能形成原子个数比为1︰1的共价化合物B,它们之间能实现如下图所示转化(部分产物已略去):

(1)Y在周期表的位置是_______ ;Z2的结构式是_______ 。
(2)反应①的离子方程式是_______ 。
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如下图所示(夹持固定装置的仪器已略去)。
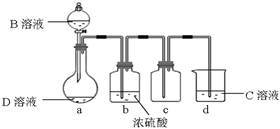
Ⅰ、写出反应②的离子方程式_______ 。
II、上述实验装置不够完善,改进方法是_______ 。
Ⅲ、足量Z2通入FeBr2溶液中发生反应的离子方程式是_______ 。

(1)Y在周期表的位置是
(2)反应①的离子方程式是
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如下图所示(夹持固定装置的仪器已略去)。

Ⅰ、写出反应②的离子方程式
II、上述实验装置不够完善,改进方法是
Ⅲ、足量Z2通入FeBr2溶液中发生反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】通常状况下,X、Y和Z是三种气态单质。X的组成元素是第3周期原子半径最小的元素(稀有气体元素除外);Y和Z均由元素R组成,Y能氧化I-,反应的离子方程式为 。
。
(1)写出物质的分子式:X___________ ,Y___________ ,Z___________ 。
(2)Y与Z的关系是___________ (填序号)。
a.互为同位素 b.属于同一物质
c.互为同素异形体 d.互为同分异构体
(3)导致大气中Y减少的主要物质是___________ 。
(4)将Y和二氧化硫分别通入品红溶液中,都能使品红溶液褪色。利用褪色的溶液区别二者的实验方法是___________ 。
(5)举例说明X的氧化性比硫单质的氧化性强:___________ (用化学方程式表示)。
 。
。(1)写出物质的分子式:X
(2)Y与Z的关系是
a.互为同位素 b.属于同一物质
c.互为同素异形体 d.互为同分异构体
(3)导致大气中Y减少的主要物质是
(4)将Y和二氧化硫分别通入品红溶液中,都能使品红溶液褪色。利用褪色的溶液区别二者的实验方法是
(5)举例说明X的氧化性比硫单质的氧化性强:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】X、Y、Z、Q四种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳中含量(质量分数)最多的元素,Q的核电荷数是X与Z的核电荷数之和。请回答下列问题。
(1)X、Y的元素符号依次为___________ 、___________ 。
(2)XZ2与YZ2分别属于___________ (填“极性分子”或“非极性分子”,下同)和___________ 。
(3)Q的元素符号是___________ ,它位于第___________ 周期,在形成化合物时它的最高化合价为___________ 。
(1)X、Y的元素符号依次为
(2)XZ2与YZ2分别属于
(3)Q的元素符号是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一、元素周期表与元素周期律在化学学习研究中有很重要的作用。下表是元素周期表的一部分,列出了①~⑩10种元素在周期表中的位置。
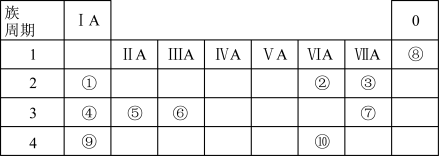
回答下列问题:
(1)①~⑩元素性质最不活泼的元素是___________ (填元素符号)。
(2)①④⑤⑥中最高价氧化物的水化物碱性最强的是___________ (填化学式),该水化物所含的化学键类型有___________ 。
(3)元素③⑥⑦的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)元素②的简单氢化物的电子式为___________ ,该氢化物常温下和元素④的单质反应的离子方程式是___________ 。
(5)元素⑩[硒(Se)]被誉为“生命元素”,科学补硒可以减少疾病的发生。铜仁市“富硒”耕地丰富,产出的“富硒”农产品受市场青睐,为“黔货出山”和“乡村振兴”作出了重要贡献。下列推断正确的是___________(填字母)。

回答下列问题:
(1)①~⑩元素性质最不活泼的元素是
(2)①④⑤⑥中最高价氧化物的水化物碱性最强的是
(3)元素③⑥⑦的简单离子半径由大到小的顺序是
(4)元素②的简单氢化物的电子式为
(5)元素⑩[硒(Se)]被誉为“生命元素”,科学补硒可以减少疾病的发生。铜仁市“富硒”耕地丰富,产出的“富硒”农产品受市场青睐,为“黔货出山”和“乡村振兴”作出了重要贡献。下列推断正确的是___________(填字母)。
A. 既有氧化性又有还原性 既有氧化性又有还原性 |
B. 的稳定性比 的稳定性比 强 强 |
C. 的酸性强于 的酸性强于 |
D. 在一定条件下可与NaOH溶液反应 在一定条件下可与NaOH溶液反应 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D、E、F是原子序数依次增大的前20号元素。元素A的周期数、主族序数、原子序数均相等;元素B的最高价氧化物对应水化物的化学式为HBO3;元素C与E同主族,且E元素原子的最外层电子数比次外层少2个,E、F两元素可形成化合物;D、E、F三种元素的最高价氧化物对应水化物之间可以两两反应。
(1)F在周期表中的位置为:___________ ,F2E中F离子的结构示意图为___________ 。
(2)气态化合物BA3的电子式为___________ ,空间构型为___________ ,将BA3通入滴有酚酞的水中,溶液变红,用电离方程式解释此现象___________ 。
(3)B、C、D三种元素的离子半径由大到小的顺序为:___________ (用离子符号表示)。
(4)E的一种同位素原子为33E,1mol33E的中子数为___________ 。
(1)F在周期表中的位置为:
(2)气态化合物BA3的电子式为
(3)B、C、D三种元素的离子半径由大到小的顺序为:
(4)E的一种同位素原子为33E,1mol33E的中子数为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】短周期元素的单质X、Y、Z在通常状况下均为气态,并有如图所示的转化关系(反应条件略去)。
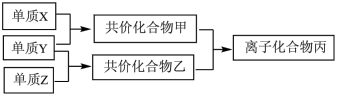
已知:a.常见双原子单质分子中,X分子所含共价键最多。
b.甲分子中含有10个电子,乙分子中含有18个电子。
(1)写出X的化学式_________________________________________ 。
(2)化合物丙中含有化学键的类型为__________________________________________ 。
(3)写出甲与乙反应生成丙的化学方程式___________________________________________________ 。

已知:a.常见双原子单质分子中,X分子所含共价键最多。
b.甲分子中含有10个电子,乙分子中含有18个电子。
(1)写出X的化学式
(2)化合物丙中含有化学键的类型为
(3)写出甲与乙反应生成丙的化学方程式
您最近一年使用:0次



