元素周期律是重要的化学学习工具。随着原子序数变化,7种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
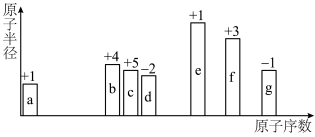
(1)b在元素周期表中的位置是_______ 周期_______ 族。7种元素中金属性最强的是_______ (用元素符号表示,下同),与d处于同一主族的短周期元素是_______ 。
(2)b和c的最高价氧化物的水化物中,酸性较强的是_______ (用化学式表示,下同),c和d的简单氢化物的稳定性较弱的是_______ 。
(3)d和f形成的化合物为_______ (用化学式表示),该化合物在熔融状态下能导电,属于_______ 化合物(填“离子”或“共价”),该化合物与盐酸反应的离子方程式为_______ 。
(4)d、e的单质在加热条件下反应生成的化合物中存在的化学键有_______ 。
(5)用电子式表示由a、c两种元素形成的化合物的形成过程______________ 。

(1)b在元素周期表中的位置是
(2)b和c的最高价氧化物的水化物中,酸性较强的是
(3)d和f形成的化合物为
(4)d、e的单质在加热条件下反应生成的化合物中存在的化学键有
(5)用电子式表示由a、c两种元素形成的化合物的形成过程
更新时间:2024-02-21 15:12:58
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】某研究性学习小组用不纯的氧化铝(杂质为Fe2O3)为原料,设计了冶炼铝的以下工艺流程(部分反应产物没有标出):
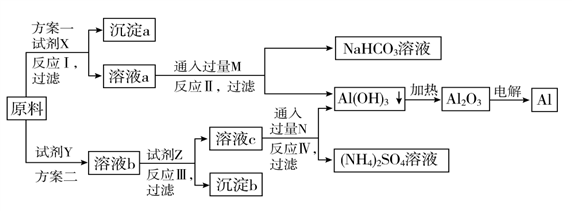
(1)试剂X的化学式为________ ,反应Ⅰ的离子方程式是________________________ 。实验室配制480 mL 1 mol·L-1X的溶液必须用到玻璃仪器除烧杯、玻璃棒、试剂瓶、胶头滴管外,还有________________ 。
(2)通入过量的M、N化学式分别为________ 、________ ,反应Ⅱ、Ⅳ的离子方程式分别____________________________ 、______________________ 。
(3)按照方案设计,试剂Z的作用是调节溶液的pH为3.1,以生成沉淀b[Fe(OH)3]。试剂Z可选用________ (填字母)。
A.Al2O3 B.H2SO4
C.NaOH D.Al(OH)3
(4)从实际工业的角度,你认为方案________ 更合理,理由是__________________ 。

(1)试剂X的化学式为
(2)通入过量的M、N化学式分别为
(3)按照方案设计,试剂Z的作用是调节溶液的pH为3.1,以生成沉淀b[Fe(OH)3]。试剂Z可选用
A.Al2O3 B.H2SO4
C.NaOH D.Al(OH)3
(4)从实际工业的角度,你认为方案
您最近半年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】为探究化合物X(含有三种元素,摩尔质量318g•mol-1)的组成和性质,某研究小组设计并完成了如图实验:
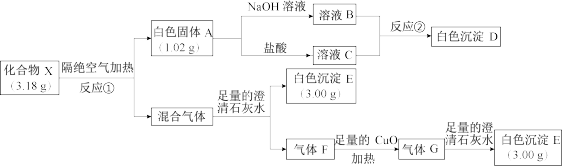
请回答下列问题:
(1)写出化合物X中存在的元素___ 。(请用元素符号表达)
(2)写出反应①的化学方程式__ 。
(3)写出反应②的离子方程式___ 。

请回答下列问题:
(1)写出化合物X中存在的元素
(2)写出反应①的化学方程式
(3)写出反应②的离子方程式
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、E为短周期元素,原子序数依次增大,质子数之和为39,B、C同周期,A、D同主族,A、C能形成两种液态化合物A2C和A2C2,E是地壳中含量最多的金属元素。
(1)E元素在周期表中的位置为_______ ;B、C的氢化物稳定性强的是_______  用化学式表示,下同
用化学式表示,下同 ;B、C、D组成的化合物中含有的化学键为
;B、C、D组成的化合物中含有的化学键为_______
(2)D2C2的电子式是_______ ,将D的单质投入A2C中,反应后得到一种无色溶液,E的单质在该无色溶液中反应的离子方程式为_______ ;
(3)元素D的单质在一定条件下,能与A单质化合生成氢化物DA,熔点为800℃。DA能与水反应放出氢气,化学反应方程式为_______ 。
(4)废印刷电路版上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡既达到了上述目的,又保护了环境,试写出反应的化学方程式_______ 。
(1)E元素在周期表中的位置为
 用化学式表示,下同
用化学式表示,下同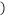 ;B、C、D组成的化合物中含有的化学键为
;B、C、D组成的化合物中含有的化学键为(2)D2C2的电子式是
(3)元素D的单质在一定条件下,能与A单质化合生成氢化物DA,熔点为800℃。DA能与水反应放出氢气,化学反应方程式为
(4)废印刷电路版上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡既达到了上述目的,又保护了环境,试写出反应的化学方程式
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】如表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
(1)化学性质最稳定的元素是____ (填元素名称),金属性最强的元素是____ (填元素符号)。
(2)图中标出的元素的最高价氧化物对应的水化物中,酸性最强的是____ (用化学式回答),写出该水化物与⑧的最高价氧化物的水化物反应的离子方程式:____ 。
(3)①与④可形成18电子的化合物,该化合物的化学式为____ 。
(4)⑤与⑦形成的化合物中化学键类型为____ ,用电子式表示该化合物的形成过程:____ 。
(5)④与⑥形成的粒子个数比为1:1的化合物的电子式为____ ;⑤、⑨的简单氢化物的沸点由高到低的顺序为____ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)图中标出的元素的最高价氧化物对应的水化物中,酸性最强的是
(3)①与④可形成18电子的化合物,该化合物的化学式为
(4)⑤与⑦形成的化合物中化学键类型为
(5)④与⑥形成的粒子个数比为1:1的化合物的电子式为
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】A、B、C、D、E、F是六种短周期元素,它们的原子序数依次增大;A元素的原子半径最小:B元素的一种单质是空气中含量最多的一种成分:D与A同主族;F元素原子的最外层电子数是其次外层电子数的 ;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:
;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:
(1)B元素的原子结构示意图___________ ;E元素在周期表中的位置是___________ 。
(2)上述6种元素中,金属性最强的元素是___________ (写元素名称,下同):非金属性最强的元素是___________ 。
(3)A、B、C和F可组成一种化合物,其原子个数之比为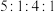 。写出该化合物的化学式
。写出该化合物的化学式___________ 。
(4)写出含E元素的氧化物与氢氧化钠溶液反应的离子方程式___________ 。
(5)由C、D两种元素形成的原子个数之比为 的化合物中,所含化学键的类型有
的化合物中,所含化学键的类型有___________ 。
 ;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:
;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:(1)B元素的原子结构示意图
(2)上述6种元素中,金属性最强的元素是
(3)A、B、C和F可组成一种化合物,其原子个数之比为
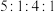 。写出该化合物的化学式
。写出该化合物的化学式(4)写出含E元素的氧化物与氢氧化钠溶液反应的离子方程式
(5)由C、D两种元素形成的原子个数之比为
 的化合物中,所含化学键的类型有
的化合物中,所含化学键的类型有
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】R、W、X、Y、M 是原子序数依次增大的五种主族元素。R 最常见同位素的原子核中不含中子。W 与 X 可形成两种稳定的化合物:WX 和 WX2.工业革命以来,人类使用的化石燃料在燃烧过程中将大量 WX2 排入大气,在一定程度导致地球表面平均温度升高。Y 与 X 是同一主族的元素,且在元素周期表中与 X 相邻。
(1)W 的原子结构示意图是___________ 。
(2) R2X、R2Y 中,稳定性较高的是___________ (填化学式),请从原子结构的角度解释其原因:___________ 。
(3) Se与Y是同一主族的元素,且在元素周期表中与 Y 相邻。
①根据元素周期律,下列推断正确的是___________ (填字母序号)。
a.Se 的最高正化合价为+7 价
b.H2Se 的还原性比 H2Y 强
c.H2SeO3 的酸性比 H2YO4 强
d.SeO2 在一定条件下可与 NaOH 溶液反应
②室温下向 SeO2固体表面吹入NH3, 可得到两种单质和 H2O , 该反应的化学方程式为___________ 。
(1)W 的原子结构示意图是
(2) R2X、R2Y 中,稳定性较高的是
(3) Se与Y是同一主族的元素,且在元素周期表中与 Y 相邻。
①根据元素周期律,下列推断正确的是
a.Se 的最高正化合价为+7 价
b.H2Se 的还原性比 H2Y 强
c.H2SeO3 的酸性比 H2YO4 强
d.SeO2 在一定条件下可与 NaOH 溶液反应
②室温下向 SeO2固体表面吹入NH3, 可得到两种单质和 H2O , 该反应的化学方程式为
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,表中的每个编号代表一种元素。请根据要求回答问题:
(1)元素①③④组成的化合物的电子式是___________ ,其属于___________ (填“离子化合物”或“共价化合物”)。
(2)元素⑤的离子结构示意图是___________ ;元素⑩的单质常温下为___________ 的液体(填颜色)。
(3)元素③⑥⑨的非金属性比较:___________ (填化学式,下同);元素②③⑦的原子半径比较:___________ 。元素⑥⑨的氢化物稳定性比较:___________ 。
(4)元素①③⑦可组成酸性强于硫酸的强酸,其化学式为___________ 。
(5)元素⑧的单质与水反应的化学方程式为___________ 。
| 族 周期 | IA | ⅡA | ⅢB~ⅡB | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ||||||||
| 2 | ② | ③ | |||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | |||||
| 4 | ⑧ | ⑨Se | ⑩Br |
(2)元素⑤的离子结构示意图是
(3)元素③⑥⑨的非金属性比较:
(4)元素①③⑦可组成酸性强于硫酸的强酸,其化学式为
(5)元素⑧的单质与水反应的化学方程式为
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:___________ (填具体元素符号或化学式,下同),元素⑩在周期表中的位置是___________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是___________ ,碱性最强的化合物的化学式是___________ 。
(3)元素③与④形成淡黄色化合物的电子式:___________ ,该化合物中___________ (填“含”或“不含”)共价键。
(4)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是___________ (用离子符号表示),写出和这三种离子具有相同核外电子数的三原子分子的结构式___________
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)元素③与④形成淡黄色化合物的电子式:
(4)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、E为短周期元素且它们的原子序数依次增大,A的核外电子总数与其周期数相同;其中D原子的L电子层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的L电子层中未成对电子数与D相同,但还有空轨道;D与E同族。请回答下列问题:
(1)A与B形成的共价化合物中既含有σ键,又含π键的化合物是___________ (任写一种)。
(2)C的简单氢化物的电子式为___________ 。
(3)B的氢化物中空间结构为正四面体形的是___________ (填名称),键角为___________ ,中心原子的杂化方式为___________ 杂化。
(4)A与B形成B2A2分子,其分子中σ键和π键的数目之比为___________ 。
(5)基态原子第一电离能:C___________ (填“>”“<”或“=”)E.
(6)离子CD3-的中心原子的价层电子对数为___________ 。
(1)A与B形成的共价化合物中既含有σ键,又含π键的化合物是
(2)C的简单氢化物的电子式为
(3)B的氢化物中空间结构为正四面体形的是
(4)A与B形成B2A2分子,其分子中σ键和π键的数目之比为
(5)基态原子第一电离能:C
(6)离子CD3-的中心原子的价层电子对数为
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】A、B、C、D、E、F为前四周期元素且原子序数依次增大,其中基态A原子的电子分布在3个能级,且每个能级所含的电子数相同;C的原子核外最外层有 6 个运动状态不同的电子;D是短周期元素中电负性最小的元素;E的最高价氧化物的水化物酸性最强;基态F原子核外最外层只有一个电子,其余能层均充满电子。G元素与D元素同主族,且相差3个周期。
(1)下列物质的性质与氢键有关的是_______ 。
a.可燃冰的形成 b. A的氢化物的沸点 c. B的氢化物的热稳定性
(2)E的最高价含氧酸中 E 原子的杂化方式为_______ 。 基态 E 原子中,核外电子占据最高能级的电子云轮廓形状为_______ 。
(3)F原子的外围电子排布式为_______ 。
(4)已知元素 A、B形成的(AB)2分子中所有原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为_______ 。
(5)通常情况下,D单质的熔沸点比G单质高,原因是_______ 。
(6)已知 DE 晶体的晶胞如图所示:
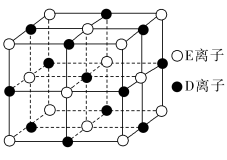
若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示A的一种晶体的晶胞(已知 A−A 键的键长为a cm, NA表示阿伏加德罗常数),则该晶胞中含有_______ 个 A 原子,该晶体的密度是_______ g·cm-3(列式表示)。
(1)下列物质的性质与氢键有关的是
a.可燃冰的形成 b. A的氢化物的沸点 c. B的氢化物的热稳定性
(2)E的最高价含氧酸中 E 原子的杂化方式为
(3)F原子的外围电子排布式为
(4)已知元素 A、B形成的(AB)2分子中所有原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为
(5)通常情况下,D单质的熔沸点比G单质高,原因是
(6)已知 DE 晶体的晶胞如图所示:

若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示A的一种晶体的晶胞(已知 A−A 键的键长为a cm, NA表示阿伏加德罗常数),则该晶胞中含有
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】2019年的化学诺贝尔奖颁给了为锂电池研究作出贡献的三位科学家,其研究的是两种常见锂电池:一种是采用镍钴锰酸锂Li(NiCoMn)O2或镍钴铝酸锂为正极的“三元材料锂电池”;另一种是采用磷酸铁锂(LiFePO4)为正极的电池。请回答下列问题:
(1)Mn位于元素周期表的_______ 区(填“s”或“p”或“d”或“ds”或“f”),基态钴原子的未成对电子数为_______ ,1mol [CoCl (NH3)5] Cl2 中含σ键数目为_______ NA。
(2)磷元素的最高价氧化物的水化物H3PO4在工业上有诸多特殊的用途,其中PO 的空间构型是
的空间构型是_______ ,中心原子的杂化方式是_______ 。
(3)PH3是_______ 分子(填“极性”或“非极性”),其在水中的溶解性比NH3小,原因是_______ 。
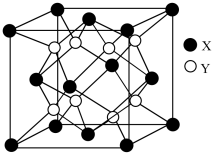
(4)硫化锂Li2S(摩尔质量M g∙mol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ρ g·cm-3,则距离最近的两个S2-的距离是_______ cm。(用含ρ、M、NA的计算式表示)
(1)Mn位于元素周期表的
(2)磷元素的最高价氧化物的水化物H3PO4在工业上有诸多特殊的用途,其中PO
 的空间构型是
的空间构型是(3)PH3是
(4)硫化锂Li2S(摩尔质量M g∙mol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ρ g·cm-3,则距离最近的两个S2-的距离是

您最近半年使用:0次

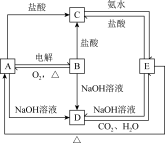
 D的化学方程式:
D的化学方程式:

