下表是元素周期表的一部分,表中的每个编号代表一种元素。请根据要求回答问题:
(1)元素①③④组成的化合物的电子式是___________ ,其属于___________ (填“离子化合物”或“共价化合物”)。
(2)元素⑤的离子结构示意图是___________ ;元素⑩的单质常温下为___________ 的液体(填颜色)。
(3)元素③⑥⑨的非金属性比较:___________ (填化学式,下同);元素②③⑦的原子半径比较:___________ 。元素⑥⑨的氢化物稳定性比较:___________ 。
(4)元素①③⑦可组成酸性强于硫酸的强酸,其化学式为___________ 。
(5)元素⑧的单质与水反应的化学方程式为___________ 。
| 族 周期 | IA | ⅡA | ⅢB~ⅡB | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ||||||||
| 2 | ② | ③ | |||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | |||||
| 4 | ⑧ | ⑨Se | ⑩Br |
(2)元素⑤的离子结构示意图是
(3)元素③⑥⑨的非金属性比较:
(4)元素①③⑦可组成酸性强于硫酸的强酸,其化学式为
(5)元素⑧的单质与水反应的化学方程式为
更新时间:2022-01-23 07:49:42
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表为元素周期表的一部分,请参照元素 在表中的位置,用相应化学用语回答下列问题:
在表中的位置,用相应化学用语回答下列问题:
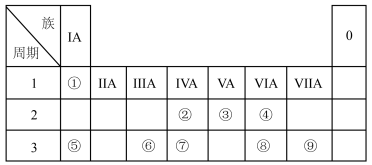
(1)画出表中形成化合物种类最多元素的原子结构示意图______ ;写出它与原子半径最小的原子形成 电子且为正四面体结构的化合物的电子式
电子且为正四面体结构的化合物的电子式______ ,用电子式表示 和
和 形成化合物的过程
形成化合物的过程______ 。
(2) 形成的简单离子半径由大到小的顺序为
形成的简单离子半径由大到小的顺序为______  填离子符号
填离子符号 ;
; 的最高价氧化物对应水化物的酸性由强到弱的顺序为
的最高价氧化物对应水化物的酸性由强到弱的顺序为______  填化学式
填化学式 。
。
(3)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是______  填化学式
填化学式 ,写出它与
,写出它与 的最高价氧化物对应水化物发生反应的离子方程式:
的最高价氧化物对应水化物发生反应的离子方程式:______ 。
(4)有两种化合物 和
和 都由
都由 四种元素组成.若
四种元素组成.若 与
与 在水溶液中能发生离子反应,则该反应的离子方程式为
在水溶液中能发生离子反应,则该反应的离子方程式为 ______ 。
 在表中的位置,用相应化学用语回答下列问题:
在表中的位置,用相应化学用语回答下列问题:
(1)画出表中形成化合物种类最多元素的原子结构示意图
 电子且为正四面体结构的化合物的电子式
电子且为正四面体结构的化合物的电子式 和
和 形成化合物的过程
形成化合物的过程(2)
 形成的简单离子半径由大到小的顺序为
形成的简单离子半径由大到小的顺序为 填离子符号
填离子符号 ;
; 的最高价氧化物对应水化物的酸性由强到弱的顺序为
的最高价氧化物对应水化物的酸性由强到弱的顺序为 填化学式
填化学式 。
。(3)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是
 填化学式
填化学式 ,写出它与
,写出它与 的最高价氧化物对应水化物发生反应的离子方程式:
的最高价氧化物对应水化物发生反应的离子方程式:(4)有两种化合物
 和
和 都由
都由 四种元素组成.若
四种元素组成.若 与
与 在水溶液中能发生离子反应,则该反应的离子方程式为
在水溶液中能发生离子反应,则该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】现有部分短周期元素的性质或原子结构如表:
(1)元素X在元素周期表中的位置为________ ,X与Q按原子个数比为1:2形成的化合物的电子式为________ 。
(2)元素Y的原子结构示意图为________ ,其与氢元素形成一种分子YH3,写出实验室制备该物质的化学方程式________ 。
(3)元素Z与元素T相比,非金属性较强的是________ (用元素符号表示),下列表述中能证明这一事实的是________ 。
a.Z离子的还原性小于T离子的还原性
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.Z的含氧酸的酸性强于T
(4)在碱性溶液中,X的简单氢化物与Q2组成燃料电池,其负极的电极反应式为________ 。
| 元素编号 | 元素性质或原子结构 |
| Q | 地壳中含量最高的元素 |
| T | M层上电子数是K层上电子数的3倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)元素Y的原子结构示意图为
(3)元素Z与元素T相比,非金属性较强的是
a.Z离子的还原性小于T离子的还原性
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.Z的含氧酸的酸性强于T
(4)在碱性溶液中,X的简单氢化物与Q2组成燃料电池,其负极的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】I.请用下列10种物质的序号填空:①O2②H2③NH4NO3④K2O2⑤Ba(OH)2⑥NH3(⑦CO2⑧NaF
只含有极性键是______ (填序号),既含有离子键又含有非极性键的是________ (填序号)。
II.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
(1)②③④三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是(填化学式)_________ 。
(2)④与⑧形成的简单化合物的电子式_________ 。
(3)⑥的气态氢化物催化氧化的化学方程式为_________ 。
(4)元素②和⑤的最高价氧化物对应水化物相互反应的离子方程式为___________ 。
(5)元素⑨的单质易溶于CCl4中,所得溶液颜色为_______ 色。
III.元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是__________ (填选项)。

A.⑥、⑧、⑨对应单核离子的半径依次增大
B.⑤的三种核素的化学性质不相同
C.④的最高价氧化物对应的水化物能与其氢化物反应,生成离子化合物
D.⑧、⑨两种元素的气态氢化物及其最高价氧化物的水化物均为强酸
只含有极性键是
II.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
| ① | |||||||||||||||||
| ⑥ | ⑦ | ||||||||||||||||
| ② | ④ | ⑤ | ⑧ | ||||||||||||||
| ③ | ⑩ | ||||||||||||||||
| ⑨ |
(1)②③④三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是(填化学式)
(2)④与⑧形成的简单化合物的电子式
(3)⑥的气态氢化物催化氧化的化学方程式为
(4)元素②和⑤的最高价氧化物对应水化物相互反应的离子方程式为
(5)元素⑨的单质易溶于CCl4中,所得溶液颜色为
III.元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是

A.⑥、⑧、⑨对应单核离子的半径依次增大
B.⑤的三种核素的化学性质不相同
C.④的最高价氧化物对应的水化物能与其氢化物反应,生成离子化合物
D.⑧、⑨两种元素的气态氢化物及其最高价氧化物的水化物均为强酸
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】四种短周期元素在周期表中的位置如图,其中只有M为金属元素。
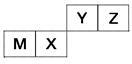
请回答下列问题:
(1)这些元素的氢化物中,水溶液碱性最强的是______ (写化学式),该氢化物的电子式为______ 。
(2)元素X和元素Y的最高价氧化物对应水化物的酸性较弱的是______ ,列举一个化学方程式证明______ 。
(3)元素Z与元素M组成的化合物中所含化学键类型为______ ,元素Z与元素X组成的化合物中所含化学键类型为______ 。

请回答下列问题:
(1)这些元素的氢化物中,水溶液碱性最强的是
(2)元素X和元素Y的最高价氧化物对应水化物的酸性较弱的是
(3)元素Z与元素M组成的化合物中所含化学键类型为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】下表是元素周期表的一部分,编号代表一种元素。请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为_______ ;考古时利用_______ (填核素符号)测定一些文物年代。
(2)元素③、④、⑦、⑧中,原子半径从大到小的顺序是_______ (用元素符号表示)。
(3)元素⑥单质和④最高价氧化物对应的水化物在溶液中反应的离子方程式为_______ 。
(4)⑤⑥两元素相比较,金属性较强的是_______ (填名称)可以验证该结论的实验是_______ (填字母)。
A. 将在空气中放置已久的这两种元素的块状单质分别放入热水中
B. 将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
C. 将形状、大小相同的这两种元素的单质分别和热水作用,并滴入酚酞溶液
D. 比较这两种元素的气态氢化物的稳定性
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)元素③、④、⑦、⑧中,原子半径从大到小的顺序是
(3)元素⑥单质和④最高价氧化物对应的水化物在溶液中反应的离子方程式为
(4)⑤⑥两元素相比较,金属性较强的是
A. 将在空气中放置已久的这两种元素的块状单质分别放入热水中
B. 将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
C. 将形状、大小相同的这两种元素的单质分别和热水作用,并滴入酚酞溶液
D. 比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】2023年是元素周期表诞生154周年,元素周期表(律)在学习、研究和生产实践中有很重要的作用。下表为元素周期表的一部分,回答下列问题。
(1)元素①~⑧中,金属性最强的元素的最高价氧化物对应的水化物中含有的化学键类型为________ ,该物质与⑥的最高价氧化物对应的水化物反应的离子方程式为______ 。
(2)元素①和④可形成不同种分子,用电子式表示其中一种的形成过程_________ 。
(3)元素的非金属性:⑧_________ ⑩(填“>”或“<”),下列事实不能 说明上述结论的是_________ 。
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
(4)⑤能与⑧形成AB型化合物,用原子结构解释原因:_________ 。
(5)元素⑨的元素符号为Ga,画出该元素的原子结构示意图_________ 。镓(Ga)及其化合物应用广泛,常用于半导体、合金材料等工业,氮化嫁(GaN)材料的研究与应用是目前半导体研究的前沿和热点。已知:镓在化合物中常显+3价,氢氧化镓难溶于水,化学性质类似氢氧化铝。
设计氧化镓转化为氢氧化镓的一种方案_________ (依次写出离子方程式)。
| 周期族 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ | ||||||
(2)元素①和④可形成不同种分子,用电子式表示其中一种的形成过程
(3)元素的非金属性:⑧
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
(4)⑤能与⑧形成AB型化合物,用原子结构解释原因:
(5)元素⑨的元素符号为Ga,画出该元素的原子结构示意图
设计氧化镓转化为氢氧化镓的一种方案
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】元素周期表是元素周期律的具体表现,是学习和研究化学的重要工具.下图是元素周期表的一部分:
请完成下列填空:
(1)元素①的简单气态氢化物的空间构型是_____________ 。
(2)元素②、③、④的简单离子半径由大到小的顺序为_____________ (用离子符号表示)。
(3) 元素在周期表中的位置是
元素在周期表中的位置是____ ,最后一行元素的基态原子中只有1个未成对电子的是_____ (填元素名称)。
(4)元素④、⑤非金属性更强的是________ (填元素符号),请从原子结构的角度解释:_________ 。并写出一个证明它们非金属性强弱的化学反应方程式________________________ 。
(5)表中第一电离能最大的元素是_____________ ,理由是__________________________ 。
| ① | ② | ||||
| ③ | ④ | ⑤ | ⑥ | ||
 |  |  |  |  |
(1)元素①的简单气态氢化物的空间构型是
(2)元素②、③、④的简单离子半径由大到小的顺序为
(3)
 元素在周期表中的位置是
元素在周期表中的位置是(4)元素④、⑤非金属性更强的是
(5)表中第一电离能最大的元素是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)H、B、N中,原子半径最大的是_______ 。根据对角线规则,B的一些化学性质与元素_______ 的相似。
(2)NH3BH3分子中,N—B化学键称为_______ 键,其电子对由_______ 提供。氨硼烷在催化剂作用下水解释放氢气:3NH3BH3+6H2O=3NH +B3O
+B3O +9H2。B3O
+9H2。B3O 的结构为
的结构为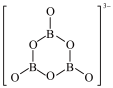 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由_______ 变为_______ 。
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是_______ 。
(4)研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。
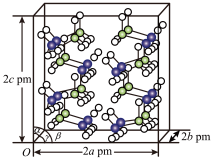
氨硼烷晶体的密度ρ=_______ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)H、B、N中,原子半径最大的是
(2)NH3BH3分子中,N—B化学键称为
 +B3O
+B3O +9H2。B3O
+9H2。B3O 的结构为
的结构为 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是
(4)研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。

氨硼烷晶体的密度ρ=
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】A、B、C、D四种短周期元素,原子序数依次增大,B、C同周期,A、D同主族且A为非金属性最强的元素,C的原子结构示意图为 ,A、B可形成BA2型化合物。据此填空:
,A、B可形成BA2型化合物。据此填空:
(1)C的元素名称为____ ,其气态氢化物的化学式为_____ 。
(2)A、B、C、D四种元素的原子半径由大到小的顺序为___ (用元素符号表示)。
(3)B和D的最高价氧化物对应的水化物反应的离子方程式是_____ 。
(4)某同学根据元素周期律推知:A元素和D元素最高价氧化物对应的水化物酸性前者强。该同学的推断是否正确?____ ,请说明理由:_____ 。
 ,A、B可形成BA2型化合物。据此填空:
,A、B可形成BA2型化合物。据此填空:(1)C的元素名称为
(2)A、B、C、D四种元素的原子半径由大到小的顺序为
(3)B和D的最高价氧化物对应的水化物反应的离子方程式是
(4)某同学根据元素周期律推知:A元素和D元素最高价氧化物对应的水化物酸性前者强。该同学的推断是否正确?
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】2022年是门捷列夫发现元素周期律153周年,下图为元素周期表的一部分。门捷列夫预言了多种当时未知的元素,T为其中之一。L在地壳中含量排第二位,广泛应用于信息技术等领域。
(1)写出J的原子结构示意图___________ 。
(2)下列说法不正确的是___________。
(3)已知X2Q4结构中含非极性共价键,试画出其结构式(用元素符号表示):___________ 。
(4)非金属性Q_____ M(用<、=、>来表示),判断依据是(试用一个化学方程式来表示)______ 。
| X | Y | Z | ||
| L | J | Q | ||
| T | M |
(2)下列说法不正确的是___________。
| A.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ2 |
| B.Q、J的氧化物的水化物酸性J<Q |
| C.用pH试纸测得Q单质的水溶液pH=3 |
| D.原子半径大小:L>J>Z |
(4)非金属性Q
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】图是元素周期表的短周期部分示意图,每个字母分别表示一种元素。
请回答下列问题:
(1)a的一种核素核内有一个质子、一个中子,该核素的符号为__________ 。
(2)b、c、d、f四种元素的原子半径由大到小的顺序为________ (用元素符号表示)。
(3)c、d、e、h四种元素最高价氧化物对应水化物的酸性由强到弱的顺序为_________ (用化学式表示)。
(4)从b、f形成的化合物与d、f形成的化合物的混合物中分离提纯d、f形成的化合物,可加入上述________ (用元素符号表示)两种元素形成的化合物的水溶液后再过滤洗涤。
| a | ||||||||
| c | e | f | g | |||||
| b | d | h |
(1)a的一种核素核内有一个质子、一个中子,该核素的符号为
(2)b、c、d、f四种元素的原子半径由大到小的顺序为
(3)c、d、e、h四种元素最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)从b、f形成的化合物与d、f形成的化合物的混合物中分离提纯d、f形成的化合物,可加入上述
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表是元素周期表的一部分:
(1)从原子结构角度分析,D、E、G、I四种元素处于同一行,是由于它们的_______ 相同。E和F元素在周期表处于同一列是由于它们的______ 相同。
(2)E元素的最低化合价为___________ ,原子半径:r(E)_________ r(D)填“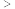 ”、“
”、“ ”或“
”或“ ”
” ,离子半径:r(G)
,离子半径:r(G)_________ r(C)(填“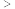 ”、“
”、“ ”或“
”或“ ”)。
”)。
(3)在表中所列元素中最高价氧化物对应水化物中酸性最强的是________ (写化学式)。
(4)科学家通过对某些元素的化合物进行研究,寻找高效农药。这些元素往往位于元素周期表的_____________ (选填序号)。
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)E元素的最低化合价为
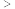 ”、“
”、“ ”或“
”或“ ”
” ,离子半径:r(G)
,离子半径:r(G)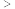 ”、“
”、“ ”或“
”或“ ”)。
”)。(3)在表中所列元素中最高价氧化物对应水化物中酸性最强的是
(4)科学家通过对某些元素的化合物进行研究,寻找高效农药。这些元素往往位于元素周期表的
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
您最近一年使用:0次



