2022年是门捷列夫发现元素周期律153周年,下图为元素周期表的一部分。门捷列夫预言了多种当时未知的元素,T为其中之一。L在地壳中含量排第二位,广泛应用于信息技术等领域。
(1)写出J的原子结构示意图___________ 。
(2)下列说法不正确的是___________。
(3)已知X2Q4结构中含非极性共价键,试画出其结构式(用元素符号表示):___________ 。
(4)非金属性Q_____ M(用<、=、>来表示),判断依据是(试用一个化学方程式来表示)______ 。
| X | Y | Z | ||
| L | J | Q | ||
| T | M |
(2)下列说法不正确的是___________。
| A.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ2 |
| B.Q、J的氧化物的水化物酸性J<Q |
| C.用pH试纸测得Q单质的水溶液pH=3 |
| D.原子半径大小:L>J>Z |
(4)非金属性Q
更新时间:2022-01-21 21:46:50
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
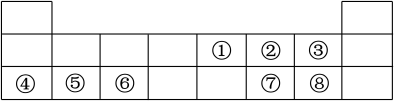
【推荐1】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题:
(1)元素⑩在周期表中的位置是___________ ,⑦的原子结构示意图为___________ 。
(2)④、⑤、⑥的简单离子半径由大到小的顺序为___________ (用离子符号和“>”表示)。
(3)④⑧⑨的气态氢化物中,最稳定的是___________ (用名称表示),最高价氧化物对应水化物中,酸性最强的是___________ (用化学式表示)。
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式___________ 。
(5)下列五种物质中,①H2O ②CO2 ③Na2O2 ④NaOH ⑤NaBr,
只存在共价键的是___________ ,只存在离子键的是___________ ,既存在离子键又存在共价键的是___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||||||||||||
| ⑩ |
(2)④、⑤、⑥的简单离子半径由大到小的顺序为
(3)④⑧⑨的气态氢化物中,最稳定的是
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式
(5)下列五种物质中,①H2O ②CO2 ③Na2O2 ④NaOH ⑤NaBr,
只存在共价键的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下面是元素周期表的结构,用化学用语完成下列问题。
(1)表中有编号的元素中化学性质最不活泼的,其原子结构示意图为__ ;④与⑤按照原子个数比1∶1形成的化合物中含有的化学键有___ 。
(2)①与②形成的最简单化合物的空间构型为__ ,将此化合物与⑧的单质混合于一干燥的集气瓶,密封后放在光亮处一段时间后,观察到的现象是__ 。
(3)由③形成的单质的电子式为__ ;⑤与⑦的最低价形成的化合物的电子式为__ 。
(4)⑧的最高价氧化物对应的水化物的化学式是___ ;①分别与④、⑦形成的简单化合物的稳定性由强到弱的顺序是__ 。
(5)④、⑥、⑧三种元素的原子形成的简单离子中半径由大到小的顺序是__ 。
(6)运用你掌握的化学理论,设计一个实验,证明⑦的非金属性比②强__ (用化学方程式表示出反应原理)。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||||||||||||
(2)①与②形成的最简单化合物的空间构型为
(3)由③形成的单质的电子式为
(4)⑧的最高价氧化物对应的水化物的化学式是
(5)④、⑥、⑧三种元素的原子形成的简单离子中半径由大到小的顺序是
(6)运用你掌握的化学理论,设计一个实验,证明⑦的非金属性比②强
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表为元素周期表的短周期区域一部分,回答下列问题:
(1)⑤的简单离子结构示意图为 ,此元素在周期表中的位置为
,此元素在周期表中的位置为________ ,同主族元素中,非金属性强于此元素的有___________ (填元素符号)。
(2)④与⑤组成的化合物常用于食品调味,用电子式表示此化合物的形成过程__________ 。
(3)②、③、④元素的简单离子半径由大到小的顺序为_________ (填离子符号)。
(4)由③、④组成的化合物中可能含有化学键的类型为_______________ 。
(5)②与③的简单氢化物稳定性更强的是_______ (填化学式)。
(6)设计实验证明②的非金属性强于①:____________________ 。
| ① | ② | ③ | ||||
| ④ | ⑤ |
 ,此元素在周期表中的位置为
,此元素在周期表中的位置为(2)④与⑤组成的化合物常用于食品调味,用电子式表示此化合物的形成过程
(3)②、③、④元素的简单离子半径由大到小的顺序为
(4)由③、④组成的化合物中可能含有化学键的类型为
(5)②与③的简单氢化物稳定性更强的是
(6)设计实验证明②的非金属性强于①:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】元素周期表的发现,揭示了原子结构与元素性质的关系。X、Y、Z、W是元素周期表中短周期元素,它们的的相对位置如表所示,请回答下列问题:
(1)写出W在元素周期表的位置:_______ ,Y的简单离子的结构示意图为_______ 。
(2)X与氢元素组成含10个电子、18个电子的分子的化学式分别为_______ 、_______
(3)写出实验室制Z元素单质的化学方程式为:_______
(4)关于Z同主族元素,下列说法不正确的是_______
(5)将一块未打磨过的W固体放入装有少量NaOH溶液的试管中,会发现开始没有气泡,一段时间后产生气泡,请写出发生反应的离子方程式:_______
(6)Y与Z形成的液体化合物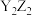 该物质可与水反应生成
该物质可与水反应生成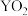 气体,1mol
气体,1mol 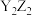 参加反应时转移1.5mol电子,其中只有一种元素化合价发生改变,写出
参加反应时转移1.5mol电子,其中只有一种元素化合价发生改变,写出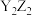 与水反应的化学方程式:
与水反应的化学方程式:_______ 。
X | |||||
W | Y | Z | |||
(2)X与氢元素组成含10个电子、18个电子的分子的化学式分别为
(3)写出实验室制Z元素单质的化学方程式为:
(4)关于Z同主族元素,下列说法不正确的是_______
| A.从上到下密度逐渐增大 | B.从上到下熔点和沸点都逐渐升高 |
| C.从上到下元素的非金属性越来越强 | D.它们单质的颜色从上到下逐渐加深 |
(6)Y与Z形成的液体化合物
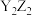 该物质可与水反应生成
该物质可与水反应生成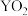 气体,1mol
气体,1mol 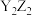 参加反应时转移1.5mol电子,其中只有一种元素化合价发生改变,写出
参加反应时转移1.5mol电子,其中只有一种元素化合价发生改变,写出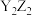 与水反应的化学方程式:
与水反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】人体必需的部分元素在元素周期表中的分布情况如下:
请回答下列问题:
(1)①的元素符号是___________ 。
(2)食盐是人类生命活动需要的营养物质,所含两种元素的原子半径大小;Na___________ Cl(填“>”或“<”);
(3)上表所列元素中,非金属性最强的是___________ (写名称);金属性最强的元素的最高价氧化物对应的水化物化学式为___________ 。
| 族 周期 | ⅠA | 0 | ||||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | C | N | O | F | ||||||
| 3 | Na | Mg | P | ① | Cl | Ar | ||||
| 4 | K | Ca | …… | |||||||
(1)①的元素符号是
(2)食盐是人类生命活动需要的营养物质,所含两种元素的原子半径大小;Na
(3)上表所列元素中,非金属性最强的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】已知几种元素的性质或原子结构的相关叙述如表所示,回答下列问题。
(1)元素X的一种同位素用作相对原子质量的标准,这种同位素的原子符号是___________ 。X的另一种同位素可用来测定文物所属年代,这种同位素的原子符号是___________ 。
(2)Y形成的另一种单质,主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是___________ 。
(3)画出T的原子结构示意图:___________ 。
(4)T与Y可以形成T2Y2的化合物,写出其与XY2反应的化学方程式___________ 。
元素编号 | 元素性质或原子结构的相关叙述 |
T | 失去一个电子后、形成与Ne相同的核外电子排布 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 其某种单质是空气的主要成分,也是最常见的助燃剂 |
Z | 原子核外有3个电子层,最外层比次外层少1个电子 |
(2)Y形成的另一种单质,主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是
(3)画出T的原子结构示意图:
(4)T与Y可以形成T2Y2的化合物,写出其与XY2反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2:1和1:1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1) E的元素名称是___________________ ,乙的电子式为___________________ 。
(2)写出甲的化学式___________________ ,该化合物中存在的化学键有___________________
(3) C、D、E三种元素的离子半径由大到小的顺序是___________________ (用离子符号填写)。
(1) E的元素名称是
(2)写出甲的化学式
(3) C、D、E三种元素的离子半径由大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】元素周期表有许多有趣的编排方式,有同学将短周期元素按照原子序数递增的顺序进行排列,得到如图所示的“蜗牛元素周期表”,图中每个圆圈代表一种元素,其中①代表氢元素。请回答下列问题:

(1)⑨在元素周期表中的位置为_______ 。
(2)④⑤⑦的离子半径由大到小的顺序为_______ 。
(3)③⑨⑩的最高价氧化物对应水化物的酸性由强到弱的顺序是_______ (填化学式)。
(4)用电子式表示由⑦和①组成的化合物的形成过程:_______ 。
(5)实验室制取④的简单氢化物的化学方程式为_______ 。
(6)可以验证⑦、⑧两元素金属性强弱的实验是_______(填字母)。

(1)⑨在元素周期表中的位置为
(2)④⑤⑦的离子半径由大到小的顺序为
(3)③⑨⑩的最高价氧化物对应水化物的酸性由强到弱的顺序是
(4)用电子式表示由⑦和①组成的化合物的形成过程:
(5)实验室制取④的简单氢化物的化学方程式为
(6)可以验证⑦、⑧两元素金属性强弱的实验是_______(填字母)。
| A.比较⑦、⑧两种元素的单质的硬度及熔点 |
| B.将除去氧化物薄膜的⑦、⑧的单质分别和热水作用,并滴入酚酞溶液 |
| C.将除去氧化物薄膜的⑦、⑧的单质分别和2mL1 mol∙L−1的盐酸反应 |
| D.比较⑦、⑧两种元素的最高价氧化物对应水化物的溶解性 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答下列问题。
(1)元素④的符号是_______ ;
(2)⑤和⑥两种元素原子半径的大小关系:⑤_______ ⑥(填“>”或“<”);
(3)①和②两种元素金属性强弱关系:①_______ ②(填“>”或“<”);
(4)属于碱金属元素有_______ 。(填元素符号)
(5)①的最高价氧化物的水化物与元素③的单质反应的化学方程式为:_______ 。
| 族 周期 | ⅠA | 0 | |||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ⑤ | Ne | |||||||
| 3 | ① | ② | ③ | ④ | ⑥ |
(2)⑤和⑥两种元素原子半径的大小关系:⑤
(3)①和②两种元素金属性强弱关系:①
(4)属于碱金属元素有
(5)①的最高价氧化物的水化物与元素③的单质反应的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,回答下列有关问题(用化学符号回答):
(1)①~⑨元素中,非金属性最强的元素是___________ (填元素符号)。
(2)⑥⑨两种元素的原子半径较大的是___________ (填元素符号)。
(3)⑧号元素形成的氢化物中含___________ (填“极性”或“非极性”)共价键。
(4)写出元素②的单质的电子式___________ 。
(5)元素①和元素③以1∶2的个数比形成化合物,写出该物质的结构式___________ 。
(6)①~⑨元素的最高价氧化物对应的水化物中,碱性最强的是___________ (填化学式),呈两性的是___________ (填化学式)。
| H | He | ||||||
| ① | ② | ③ | ④ | ||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)⑥⑨两种元素的原子半径较大的是
(3)⑧号元素形成的氢化物中含
(4)写出元素②的单质的电子式
(5)元素①和元素③以1∶2的个数比形成化合物,写出该物质的结构式
(6)①~⑨元素的最高价氧化物对应的水化物中,碱性最强的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】A、X,Y、Z、R、W为六种短周期元素。A是短周期中半径最小的元素;X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价代数和为4;Z的单质常用于漂白工业;R是短周期元素中金属性最强的元素,W是生活中的常见金属,其氧化物常作耐高温材料。回答下列问题:
(1)Y元素的名称是___ ,在周期表中的位置是___ 。
(2)写出化合物AZX的电子式:___ ;化合物R2X2存在的化学键类型是___ 。
(3)比较X、Z、R三种元素对应的简单离子半径大小:___ (用离子符号和“>”表示)。
(4)下列事实能证明R比W金属性强的这一结论的是___ (填序号)。
a.R的熔点低于W
b.常温下,R与水剧烈反应而W不能
c.最高价氧化物对应的水化物碱性:ROH>W(OH)3
d.最外层电子数:W>R
(5)写出工业上制备W的单质的化学方程式:___ 。
(6)A单质与X单质在KOH溶液中可以组成燃料电池,则正极附近溶液的pH将___ (填“变大”“变小”或“不变”,下同);放电一段时间KOH的物质的量___ 。
(7)用电子式表示RZ的形成过程:___ 。
(1)Y元素的名称是
(2)写出化合物AZX的电子式:
(3)比较X、Z、R三种元素对应的简单离子半径大小:
(4)下列事实能证明R比W金属性强的这一结论的是
a.R的熔点低于W
b.常温下,R与水剧烈反应而W不能
c.最高价氧化物对应的水化物碱性:ROH>W(OH)3
d.最外层电子数:W>R
(5)写出工业上制备W的单质的化学方程式:
(6)A单质与X单质在KOH溶液中可以组成燃料电池,则正极附近溶液的pH将
(7)用电子式表示RZ的形成过程:
您最近一年使用:0次