2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、以及由其制备得到的漂白液、漂白粉都是生活中常见的含氯消毒剂。
(1)常温下用烧碱溶液吸收Cl2制备“84”消毒液,但是将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO、NaClO3的混合溶液。当混合溶液中的Cl-和ClO 的个数比为15:2时,混合液中的ClO-和ClO
的个数比为15:2时,混合液中的ClO-和ClO 的个数比为
的个数比为__ ,从氧化还原角度分析Cl2表现了_______ 性。
(2)“洁厕灵”和“84”消毒液不可以混合使用,请用离子方程式解释原因:_______
(1)常温下用烧碱溶液吸收Cl2制备“84”消毒液,但是将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO、NaClO3的混合溶液。当混合溶液中的Cl-和ClO
 的个数比为15:2时,混合液中的ClO-和ClO
的个数比为15:2时,混合液中的ClO-和ClO 的个数比为
的个数比为(2)“洁厕灵”和“84”消毒液不可以混合使用,请用离子方程式解释原因:
更新时间:2021-03-19 17:44:09
|
相似题推荐
【推荐1】过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:

(1)保存过氧化氢的试剂瓶上最适合贴的标签是_____________ (填字母)。
(2)下列反应中,H2O2体现还原性的是______________ 。
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
D.K2Cr2O7+4H2O2+2H+ =2CrO5+5H2O[CrO5称为过氧化铬,可写成CrO(O2)2]
(3)采矿废液中的氰化物(如KCN)一般用H2O2做无毒化处理,化学方程式为:KCN+H2O2+H2O=KHCO3+NH3↑(KCN中N为﹣3价),生成1mol NH3时转移的电子数为___________ 。
(4)H2O2被称为绿色氧化剂的理由是_____________________________________ 。

(1)保存过氧化氢的试剂瓶上最适合贴的标签是
(2)下列反应中,H2O2体现还原性的是
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
D.K2Cr2O7+4H2O2+2H+ =2CrO5+5H2O[CrO5称为过氧化铬,可写成CrO(O2)2]
(3)采矿废液中的氰化物(如KCN)一般用H2O2做无毒化处理,化学方程式为:KCN+H2O2+H2O=KHCO3+NH3↑(KCN中N为﹣3价),生成1mol NH3时转移的电子数为
(4)H2O2被称为绿色氧化剂的理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】研究物质性质及其转化具有重要的价值,请回答下列问题:
(1)火药是中国四大发明之一。黑火药在爆炸时,发生如下反应:S+2KNO3+3C=K2S+N2↑+3CO2↑。其中氧化剂为___ 。
(2)中国古代有“银针验毒”的记载,其原理为4Ag+O2+2H2S=2X+2H2O,则X的化学式为___ ,其中H2S在反应中作___ (填编号)。
a.氧化剂 b.还原剂 c.还原剂和氧化剂 d.反应物
(3)“84消毒液”的有效成分为NaClO,和“洁厕灵(稀盐酸)”混合会有危险,请用离子方程式表示:___ 。
(4)硝酸铵是一种常见的氮肥,受热易分解NH4NO3 N2O↑+2H2O。当反应转移1 mol电子时,标准状况下生成气体的体积为
N2O↑+2H2O。当反应转移1 mol电子时,标准状况下生成气体的体积为___ L。
(1)火药是中国四大发明之一。黑火药在爆炸时,发生如下反应:S+2KNO3+3C=K2S+N2↑+3CO2↑。其中氧化剂为
(2)中国古代有“银针验毒”的记载,其原理为4Ag+O2+2H2S=2X+2H2O,则X的化学式为
a.氧化剂 b.还原剂 c.还原剂和氧化剂 d.反应物
(3)“84消毒液”的有效成分为NaClO,和“洁厕灵(稀盐酸)”混合会有危险,请用离子方程式表示:
(4)硝酸铵是一种常见的氮肥,受热易分解NH4NO3
 N2O↑+2H2O。当反应转移1 mol电子时,标准状况下生成气体的体积为
N2O↑+2H2O。当反应转移1 mol电子时,标准状况下生成气体的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】水合肼(N2H4·H2O)又称水合联氨,其纯净物为无色透明的油状液体,具有强碱性和吸湿性。将水合肼通入CuO胶体中,可发生如图所示的转化。
(1)图示的转化中,②属于_____________ (填“非氧化还原反应”或“氧化还原反应”)。
(2)转化①中,氧化剂与还原剂的物质的量之比为4: l ,则X的化学式为_____ 。
(3)转化②中,反应一段时间后,溶液中n(OH-)____________ (填“增大”“ 减小” 或“不变”)。
(4)若①中参加反应的CuO物质的量为0.4mol,按图示转化过程进行后,④中生成的CuO物质的量也等于0.4mol,则③中参加反应的O2的物质的量与④中今加反应的NaClO的物质的量之比为_________ 。

(1)图示的转化中,②属于
(2)转化①中,氧化剂与还原剂的物质的量之比为4: l ,则X的化学式为
(3)转化②中,反应一段时间后,溶液中n(OH-)
(4)若①中参加反应的CuO物质的量为0.4mol,按图示转化过程进行后,④中生成的CuO物质的量也等于0.4mol,则③中参加反应的O2的物质的量与④中今加反应的NaClO的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 、
、 、
、 是化工生产中的重要气体原料,它们都有一定的毒性。用氨水可NaOH溶液处理可以有效防止对空气的污染。请回答下列问题:
是化工生产中的重要气体原料,它们都有一定的毒性。用氨水可NaOH溶液处理可以有效防止对空气的污染。请回答下列问题:
(1)工业上用电解饱和食盐水生产氯气,用浓氨水检验 是否泄漏。
是否泄漏。
①在电解池阳极上发生的电极反应是______
②电解饱和食盐水制氯气的化学反应方程式为______
③已知: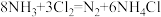 当测试到有少量
当测试到有少量 泄漏时,可以观察到的明显现象
泄漏时,可以观察到的明显现象______ ,若反应中有0.08 mol的氨气被氧化,则有______ mol电子发生转移。
(2)①若用热烧碱溶液吸收 ,反应后的混合溶液中含NaCl、NaClO和
,反应后的混合溶液中含NaCl、NaClO和 物质的量比值为n:1:1,则
物质的量比值为n:1:1,则
______ 。
② 是形成酸雨的主要因素,工业上常利用过量氨水吸收
是形成酸雨的主要因素,工业上常利用过量氨水吸收 ,其发生反应的离子方程式是
,其发生反应的离子方程式是______ 。
(3) 是燃油汽车尾气中的主要污染物之一,实验室可用烧碱溶液吸收
是燃油汽车尾气中的主要污染物之一,实验室可用烧碱溶液吸收 和NO,(已知
和NO,(已知 ,
,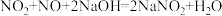 ),当消耗
),当消耗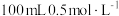 的烧碱溶液时,共吸收混合气体
的烧碱溶液时,共吸收混合气体______ L(标准状态)。
 、
、 、
、 是化工生产中的重要气体原料,它们都有一定的毒性。用氨水可NaOH溶液处理可以有效防止对空气的污染。请回答下列问题:
是化工生产中的重要气体原料,它们都有一定的毒性。用氨水可NaOH溶液处理可以有效防止对空气的污染。请回答下列问题:(1)工业上用电解饱和食盐水生产氯气,用浓氨水检验
 是否泄漏。
是否泄漏。①在电解池阳极上发生的电极反应是
②电解饱和食盐水制氯气的化学反应方程式为
③已知:
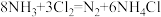 当测试到有少量
当测试到有少量 泄漏时,可以观察到的明显现象
泄漏时,可以观察到的明显现象(2)①若用热烧碱溶液吸收
 ,反应后的混合溶液中含NaCl、NaClO和
,反应后的混合溶液中含NaCl、NaClO和 物质的量比值为n:1:1,则
物质的量比值为n:1:1,则
②
 是形成酸雨的主要因素,工业上常利用过量氨水吸收
是形成酸雨的主要因素,工业上常利用过量氨水吸收 ,其发生反应的离子方程式是
,其发生反应的离子方程式是(3)
 是燃油汽车尾气中的主要污染物之一,实验室可用烧碱溶液吸收
是燃油汽车尾气中的主要污染物之一,实验室可用烧碱溶液吸收 和NO,(已知
和NO,(已知 ,
,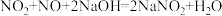 ),当消耗
),当消耗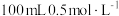 的烧碱溶液时,共吸收混合气体
的烧碱溶液时,共吸收混合气体
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】“84”消毒液是一种常见的含氯消毒剂。
(1)“84”消毒液的有效成分为_______ (用化学式表示)。
(2)常温下,将氯气通入NaOH溶液中可制得“84”消毒液。写出反应的离子方程式:_______ 。
(3)针对不同物品消毒,“84”消毒液需要稀释到不同浓度使用。取含次氯酸钠0.2mol·L-1的“84”消毒液1mL,加水稀释至100mL,稀释后的溶液中次氯酸钠的物质的量浓度为_______  。
。
(1)“84”消毒液的有效成分为
(2)常温下,将氯气通入NaOH溶液中可制得“84”消毒液。写出反应的离子方程式:
(3)针对不同物品消毒,“84”消毒液需要稀释到不同浓度使用。取含次氯酸钠0.2mol·L-1的“84”消毒液1mL,加水稀释至100mL,稀释后的溶液中次氯酸钠的物质的量浓度为
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中含有Cl-、ClO-、ClO 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
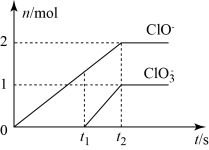
(1)t1时刻之前发生的反应是:___________
(2)t2时,Ca(OH)2与Cl2发生反应的总化学方程式为10Ca(OH)2+10Cl2=2Ca(ClO)2+Ca(ClO3)2+7CaCl2+10H2O,则该石灰乳中含有Ca(OH)2的物质的量是___________ mol。
(3)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入Cl2的速度不同,ClO-和ClO 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
___________ 2(填“>”、“<”或“=”);氯酸钙(Ca(ClO3)2)为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施___________ (写一条即可)。
(4)请配平化学方程式:KClO3+HCl--KCl+Cl2↑+H2O___________ 。若反应过程中转移2mol e-,则生成标准状况下Cl2的体积为___________ L。
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①3FeCl3+2KI=2FeCl2+2KCl+I2;
②2FeCl2+Cl2=2FeCl3;
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(5)FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是___________ 。
(6)在酸性溶液中存在大量的I-,则Cr2O 、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是___________ 。
 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
(1)t1时刻之前发生的反应是:
(2)t2时,Ca(OH)2与Cl2发生反应的总化学方程式为10Ca(OH)2+10Cl2=2Ca(ClO)2+Ca(ClO3)2+7CaCl2+10H2O,则该石灰乳中含有Ca(OH)2的物质的量是
(3)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入Cl2的速度不同,ClO-和ClO
 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
(4)请配平化学方程式:KClO3+HCl--KCl+Cl2↑+H2O
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①3FeCl3+2KI=2FeCl2+2KCl+I2;
②2FeCl2+Cl2=2FeCl3;
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(5)FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是
(6)在酸性溶液中存在大量的I-,则Cr2O
 、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
您最近一年使用:0次



