辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题
辽宁
高一
阶段练习
2021-03-19
388次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、物质结构与性质、化学实验基础
辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题
辽宁
高一
阶段练习
2021-03-19
388次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
解题方法
1. 化学与生活、社会发展息息相关,下列说法不正确的是( )
| A.“外观如雪,强烧之,紫青烟起”,南北朝陶弘景对硝酸钾的鉴定利用了焰色试验原理 |
| B.“熬胆矾铁釜,久之亦化为铜”,北宋沈括用胆矾炼铜的过程属于置换反应 |
| C.“玉不琢不成器”、“百炼方能成钢”发生的均为化学变化 |
| D.稀土元素被称为“冶金工业的维生素”,其加入钢中后可增加钢的韧性、抗氧化性 |
您最近一年使用:0次
2021-03-17更新
|
104次组卷
|
2卷引用:辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题
单选题
|
容易(0.94)
名校
解题方法
2. 下列有关化学用语使用正确的是( )
A.纯碱的电离方程式:NaHCO3=Na++HCO |
B.氯原子的结构示意图: |
| C.H2S的结构式:H—S—H |
D.过氧化氢的电子式: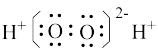 |
【知识点】 化学用语综合判断
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
3. 雷雨天闪电时空气中有O3生成。下列说法中,正确的是( )
| A.O2和O3互为同位素 |
| B.16O和18O的相互转化是化学变化 |
| C.在相同的温度和压强下,等体积的O2和O3含有相同数目的原子 |
| D.等质量的O2和O3含有相同的质子数 |
您最近一年使用:0次
2021-03-17更新
|
292次组卷
|
5卷引用:辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题
单选题
|
较易(0.85)
名校
解题方法
4. 我国首艘使用了钛合金材料的国产航母已成功下水,钛(Ti)常温下与酸、碱均不反应,但高温下能被空气氧化,由钛铁矿(主要成分是FeO和TiO2)提取金属钛的主要工艺流程如图。下列说法错误的是
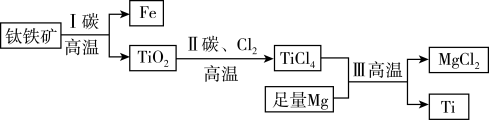
| A.步骤Ⅰ、II中均发生氧化还原反应 |
| B.步骤Ⅰ、Ⅱ中碳元素的化合价均升高 |
| C.步骤Ⅲ中反应可在氩气环境中进行,也可在空气中进行 |
| D.可用稀硫酸除去金属钛中的少量镁杂质 |
您最近一年使用:0次
2020-12-09更新
|
1015次组卷
|
13卷引用:福建省泉州市安溪一中、养正中学、惠安一中、泉州实验中学2020-2021学年高一上学期期中联考化学试题
福建省泉州市安溪一中、养正中学、惠安一中、泉州实验中学2020-2021学年高一上学期期中联考化学试题吉林省长春外国语学校2020-2021学年高一上学期期末考试化学试题广东省汕头市金山中学2020-2021学年高一上学期期末考试化学试题安徽省芜湖市安庆市2020-2021学年高一上学期期末教学质量监控化学试题辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题四川省成都外国语学校2020-2021学年高一4月月考化学试题安徽省涡阳一中2020-2021年高一上学期期末考试化学试题重庆市西南大学附属中学校2021-2022学年高一上学期第一次定时训练(广延班)化学试题广东省广州市广外附设外语学校2021-2022学年高一上学期12月月考化学试题福建省永春第一中学2021-2022学年高一上学期期中考试化学试题作业(十九) 常见的合金及其应用福建省福州市六校2023-2024学年高一上学期期中联考化学试题广东省广州市第六中学2023-2024学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
名校
5. 下列说法正确的是(设NA为阿伏加德罗常数的值)( )
| A.25g质量分数为34%的H2O2水溶液中氧原子数为0.5NA |
| B.78 g Na2O2晶体中阴、阳离子总数为3NA |
| C.0.3 mol/LNaCl溶液中含有0.3 NA氯离子 |
| D.1 mol H2O与足量的铁粉高温条件下完全反应,转移的电子数为NA |
您最近一年使用:0次
2021-03-17更新
|
250次组卷
|
3卷引用:辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题
单选题
|
适中(0.65)
名校
解题方法
6. 下列离子方程式中正确的是( )
A.向10 mL 0.1 mol/L的Na2CO3溶液中逐滴加入0.1 mol/L盐酸 10mL: +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
B.实验室用硫酸铝和氨水制备氢氧化铝:Al3++3NH3.H2O=Al(OH)3↓+3 |
| C.制备氢氧化铁胶体:Fe3++3OH-=Fe(OH)3 |
D.澄清石灰水与过量的碳酸氢钠反应: +OH-+Ca2+=CaCO3↓+H2O +OH-+Ca2+=CaCO3↓+H2O |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
7. 下列除杂试剂的选择或除杂操作不正确的是
| 选项 | 括号内为杂质 | 除杂试剂 | 除杂操作 |
| A | Fe(Al)固体 | NaOH溶液 | 充分反应后过滤 |
| B | NaHCO3(Na2CO3)溶液 | CO2 | 通入过量的CO2 |
| C | FeCl3(FeCl2)溶液 | Cl2 | 通入过量的Cl2 |
| D | CO2(HCl)气体 | 饱和Na2CO3溶液 | 洗气 |
| A.A | B.B | C.C | D.D |
【知识点】 物质的分离、提纯
您最近一年使用:0次
单选题
|
适中(0.65)
名校
8. 向一定量的Cu、Fe2O3的固体混合物中加入300 mL2 mol/L的硫酸,恰好使混合物完全溶解,所得溶液中加入KSCN溶液不显红色。若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为( )
| A.1.6 g | B.4.8 g | C.6.4 g | D.9.6 g |
【知识点】 化学方程式计算中物质的量的运用解读 铁的氧化物
您最近一年使用:0次
2021-03-17更新
|
226次组卷
|
2卷引用:辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题
单选题
|
适中(0.65)
名校
解题方法
9. 室温下,下列各组离子在指定溶液中能大量共存的是( )
A.FeCl2溶液中:K+、H+、NO 、SO 、SO |
B.强酸性溶液中:K+、Na+、HCO 、Cl-、 、Cl-、 |
C.透明溶液中:K+、Cu2+、Cl-、NO |
D.FeCl3溶液中:Na+、SO 、SCN-、NO 、SCN-、NO |
您最近一年使用:0次
2021-03-17更新
|
589次组卷
|
10卷引用:辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题
辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题江苏省苏州市南京航空航天大学苏州附属中学2020-2021学年高一下学期二月月考化学试题四川省绵阳东辰国际学校2020-2021学年高一下学期第一次月考化学试题四川省南充市李渡中学2020-2021学年高一下学期第一次月考化学试题四川省广安友谊中学2020-2021学年高一下学期半期考试化学试题江苏省外国语学校2020-2021学年高一下学期期中考试化学试题云南省昆明市第八中学2020-2021学年高一下学期第一次月考化学试题江苏省海州高级中学2021-2022学年高一下学期期中考试化学试题四川省遂宁中学校2021-2022学年高一下学期6月月考化学试题江苏省苏州外国语学校2023-2024学年高一下学期阶段测试(一)化学试题
单选题
|
较易(0.85)
名校
10. 氢化钠(NaH)可在野外用作生氢剂,化学反应原理为:NaH+ H2O=NaOH+H2↑。下列说法不正确的是( )
| A.氢化钠(NaH)中氢元素化合价为-1价 |
| B.该反应每转移1mol电子,生成22.4L(标准状况下)的氢气 |
| C.H2O在反应中做氧化剂被还原 |
| D.氢氧化钠是氧化产物 |
【知识点】 氧化还原反应的几组概念解读 氧化还原反应有关计算
您最近一年使用:0次
单选题
|
较难(0.4)
名校
11. 利用碳酸钠晶体(Na2CO3·10H2O,相对分子质量286)来配制0.1mol/L的碳酸钠溶液980mL,假如其他操作均准确无误,下列情况会引起配制溶液的浓度偏高的是( )
| A.称取碳酸钠晶体28.6g |
| B.溶解时进行加热,并将热溶液转移到容量瓶中至刻度线 |
| C.转移时,对用于溶解碳酸钠晶体的烧杯没有进行洗涤 |
| D.定容后,将容量瓶振荡摇匀,静置发现液面低于刻度线,又加入少量水至刻度线 |
您最近一年使用:0次
2019-02-03更新
|
995次组卷
|
10卷引用:浙江省杭州市塘栖中学2018-2019学年高一上学期期末复习化学试题
浙江省杭州市塘栖中学2018-2019学年高一上学期期末复习化学试题福建省福清市华侨中学2018-2019学年高一上学期期末考试化学试题云南省玉溪一中2018-2019学年高一上学期期末考试化学试题【全国百强校】内蒙古鄂尔多斯市第一中学2018-2019学年高二下学期第三次月考化学试题安徽省亳州市第二中学2018-2019学年高二下学期期末考试化学试题步步为赢 高一化学寒假作业:作业十八 综合评估(二)福建省三明市福清侨中2018-2019学年高一上学期期末考试化学试题天津市六校联考2020-2021学年度高一上学期期末考试化学试题辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题黑龙江省哈尔滨市第七十三中学校2021-2022学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
12. 下列有关“实验操作”、“现象”及“实验结论”都正确的是( )
| 选项 | 实验操作 | 现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的BaCl2 | 产生白色沉淀 | 证明溶液中含有SO |
| B | 向KMnO4溶液中滴加某溶液,振荡 | 紫红色褪去 | 该溶液一定是KI溶液 |
| C | 向CaCl2溶液中通入适量CO2 | 产生白色沉淀 | 白色沉淀为CaCO3 |
| D | 向包有Na2O2粉末的脱脂棉滴几滴水 | 脱脂棉剧烈燃烧 | Na2O2与水反应放热且有O2生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-03-17更新
|
275次组卷
|
4卷引用:辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题
单选题
|
较难(0.4)
名校
解题方法
13. 今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH 、Cl-、Mg2+、 Ba2+、CO
、Cl-、Mg2+、 Ba2+、CO 、SO
、SO ,现取三份100ml溶液做如下实验: (已知:NH
,现取三份100ml溶液做如下实验: (已知:NH +OH-
+OH- NH3↑+H2O )
NH3↑+H2O )
①第一份加入AgNO3溶液有沉淀生成;
②第二份加足量的NaOH溶液加热后,收集到气体0.04mol;
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,,经足量盐酸洗涤、干燥后,沉淀质量为 2.33g。根据上述实验,以下推测正确的是( )
 、Cl-、Mg2+、 Ba2+、CO
、Cl-、Mg2+、 Ba2+、CO 、SO
、SO ,现取三份100ml溶液做如下实验: (已知:NH
,现取三份100ml溶液做如下实验: (已知:NH +OH-
+OH- NH3↑+H2O )
NH3↑+H2O )①第一份加入AgNO3溶液有沉淀生成;
②第二份加足量的NaOH溶液加热后,收集到气体0.04mol;
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,,经足量盐酸洗涤、干燥后,沉淀质量为 2.33g。根据上述实验,以下推测正确的是( )
| A.K+不一定存在 |
| B.Ba2+ 和Mg2+一定不存在 |
C.100ml溶液中含0.01mol CO |
| D.Cl-一定存在 |
您最近一年使用:0次
2021-03-17更新
|
506次组卷
|
2卷引用:辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题
单选题
|
适中(0.65)
名校
解题方法
14. 下列说法中正确的个数是( )
①化学反应的本质是有旧键的断裂和新建的形成
②共价化合物均是非电解质
③金属单质在反应中失去电子数越多,其还原性越强
④金属单质只有还原性,非金属单质只有氧化性
⑤化学键可以使离子相结合也可以使原子相结合
⑥化学键包括离子键、共价键、氢键
⑦同主族元素的单质熔沸点从上到下逐渐升高
⑧液态氯化氢能导电,所以氯化氢是电解质
①化学反应的本质是有旧键的断裂和新建的形成
②共价化合物均是非电解质
③金属单质在反应中失去电子数越多,其还原性越强
④金属单质只有还原性,非金属单质只有氧化性
⑤化学键可以使离子相结合也可以使原子相结合
⑥化学键包括离子键、共价键、氢键
⑦同主族元素的单质熔沸点从上到下逐渐升高
⑧液态氯化氢能导电,所以氯化氢是电解质
| A.1个 | B.2个 | C.3个 | D.4个 |
【知识点】 无机物质的分类 同主族元素性质递变规律 化学键基本概念 氢键概念及特征解读
您最近一年使用:0次
2021-03-17更新
|
341次组卷
|
2卷引用:辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题
单选题
|
适中(0.65)
名校
15. A、B、C、D、E的原子序数依次增大,A原子核外电子数等于电子层数,B原子的主族序数是周期数的3倍,同周期元素形成的简单离子中C元素的离子半径最小,D的最高价氧化物对应的水化物的化学式为HnZOn+2,E元素的一种氧化物常用做油漆、涂料的红色颜料。下列说法错误的是( )
| A.简单离子半径:A<B<C<D | B.A与B形成的某化合物含有非极性共价键 |
| C.E元素为过渡元素 | D.C与D的最高价氧化物的水化物之间可以反应 |
您最近一年使用:0次
2021-03-17更新
|
257次组卷
|
3卷引用:辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题
二、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
解题方法
16. 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
(1)将Na、K、Mg、Al各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:_______ 与盐酸反应最剧烈,_______ 与盐酸反应产生的气体最多(填元素符号)。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为:__________ 。
(1)将Na、K、Mg、Al各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为:
您最近一年使用:0次
三、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
17. 利用如图装置可验证同主族元素非金属性的变化规律
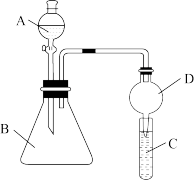
(1)仪器D的名称为____________ 。
(2)实验室中现有药品:①稀盐酸 ②稀硝酸 ③Na2SiO3溶液 ④Na2CO3固体,请选择合适药品设计实验验证N、C、Si的非金属性的变化规律;装置A、B中所装药品分别为_____ 、_______ (填序号)。但有同学认为该装置有缺陷,如何改进?________ 。

(1)仪器D的名称为
(2)实验室中现有药品:①稀盐酸 ②稀硝酸 ③Na2SiO3溶液 ④Na2CO3固体,请选择合适药品设计实验验证N、C、Si的非金属性的变化规律;装置A、B中所装药品分别为
您最近一年使用:0次
四、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
18. (1)过氧化氢俗名双氧水,有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。配平下列反应方程式:______
______H2O2+______Cr2(SO4)3+______KOH—______K2CrO4+______K2SO4+______H2O
(2)消除采矿业胶液中的氰化物(如KCN,C为+2价),经以下反应实现:KCN+H2O2+H2O=A+NH3↑(已配平)。试指出A的化学式______ ,如此反应中有6.72L(标准状况)气体生成,转移电子数目为______
______H2O2+______Cr2(SO4)3+______KOH—______K2CrO4+______K2SO4+______H2O
(2)消除采矿业胶液中的氰化物(如KCN,C为+2价),经以下反应实现:KCN+H2O2+H2O=A+NH3↑(已配平)。试指出A的化学式
【知识点】 氧化还原反应方程式的配平解读 电子转移计算
您最近一年使用:0次
五、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
19. 已知FeCl3的熔点为306 ℃,沸点为315℃,易吸收空气里的水分而潮解,实验室制备FeCl3的装置如图所示。
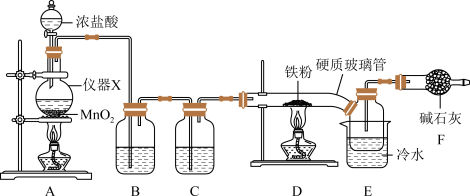
回答下列问题:
(1)写出A中发生反应的离子方程式为____________
(2)装置B中溶液为____________ ,C的作用是_____________ 。
(3)加热时,先点燃装置____ (填A或D)的酒精灯,当_________ 时,再点燃另一装置的酒精灯。
(4)写出装置D制备FeCl3的化学方程式____________ 。
(5)用粗硬质玻璃管直接连接装置D和E,比用细导管连接的优点是_________ 。

回答下列问题:
(1)写出A中发生反应的离子方程式为
(2)装置B中溶液为
(3)加热时,先点燃装置
(4)写出装置D制备FeCl3的化学方程式
(5)用粗硬质玻璃管直接连接装置D和E,比用细导管连接的优点是
您最近一年使用:0次
六、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
解题方法
20. 2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、以及由其制备得到的漂白液、漂白粉都是生活中常见的含氯消毒剂。
(1)常温下用烧碱溶液吸收Cl2制备“84”消毒液,但是将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO、NaClO3的混合溶液。当混合溶液中的Cl-和ClO 的个数比为15:2时,混合液中的ClO-和ClO
的个数比为15:2时,混合液中的ClO-和ClO 的个数比为
的个数比为__ ,从氧化还原角度分析Cl2表现了_______ 性。
(2)“洁厕灵”和“84”消毒液不可以混合使用,请用离子方程式解释原因:_______
(1)常温下用烧碱溶液吸收Cl2制备“84”消毒液,但是将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO、NaClO3的混合溶液。当混合溶液中的Cl-和ClO
 的个数比为15:2时,混合液中的ClO-和ClO
的个数比为15:2时,混合液中的ClO-和ClO 的个数比为
的个数比为(2)“洁厕灵”和“84”消毒液不可以混合使用,请用离子方程式解释原因:
【知识点】 氧化还原反应有关计算 氯气与碱溶液反应解读
您最近一年使用:0次
七、解答题 添加题型下试题
解答题-工业流程题
|
较易(0.85)
名校
21. 过氧化钙晶体(CaO2 8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
轻质CaCO3粉末 滤液
滤液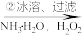 白色结晶体
白色结晶体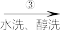 目标产物
目标产物
回答下列问题:
(1)CaO2电子式:_________________ 。
(2)反应①的离子方程式为_________________ ;过滤过程中用到的玻璃仪器有_________ 。
(3)用上述方法制取CaO2 8H2O的化学方程式为
8H2O的化学方程式为___________________________________ 。
(4)操作②温度不宜过高,其可能原因是___________________________________________ 。
(5)实验室常采用以酸为介质,用高锰酸钾溶液测定过氧化钙的含量。其原理为:5CaO2+8H2SO4+2KMnO4=5CaSO4+2MnSO4+5O2 +8H2O+K2SO4
+8H2O+K2SO4
,某同学准确称取ag产品于有塞锥形瓶中,用适量酸溶解,加入cmLbmol L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为
L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为________ (用含a、b、c的代数式表示)。
 8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。轻质CaCO3粉末
 滤液
滤液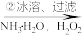 白色结晶体
白色结晶体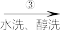 目标产物
目标产物回答下列问题:
(1)CaO2电子式:
(2)反应①的离子方程式为
(3)用上述方法制取CaO2
 8H2O的化学方程式为
8H2O的化学方程式为(4)操作②温度不宜过高,其可能原因是
(5)实验室常采用以酸为介质,用高锰酸钾溶液测定过氧化钙的含量。其原理为:5CaO2+8H2SO4+2KMnO4=5CaSO4+2MnSO4+5O2
 +8H2O+K2SO4
+8H2O+K2SO4,某同学准确称取ag产品于有塞锥形瓶中,用适量酸溶解,加入cmLbmol
 L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为
L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为
您最近一年使用:0次
解答题-无机推断题
|
较难(0.4)
名校
解题方法
22. 下表为元素周期表的一部分,请回答有关问题:
(1)已知元素⑩的一种核素,其中子数为45,用原子符号表示该核素为_________
(2)由元素②和④形成的三核直线形分子的结构式为_________
(3)用电子式表示元素⑤和⑦的原子形成的化合物(该化合物含有三个原子核)的形成过程_______________
(4)由上述元素④和⑤构成的淡黄色固体,该化合物所含的化学键类型为______ (填“离子键”、“极性键”或“非极性键”)④和⑦的氢化物稳定性较强的是__________ 、沸点较高的是_________ (填化学式)⑧和⑩的氢化物还原性较强的是_______ (填化学式)
(5)元素⑦、⑧、⑨的离子半径由大到小的顺序是_________ (用离子符号表示);元素⑨的最高价氧化物的水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为__________
(6)能比较元素⑦和⑧非金属性强弱的实验事实是_________ (填字母序号)。
a.⑦的氢化物的酸性比⑧的氢化物的酸性弱
b.⑧的单质R2与H2化合比⑦的单质Q与H2化合容易,且HR的稳定性比H2Q强
c.在⑦的氢化物H2Q的水溶液中通少量⑧的单质R2气体可置换出单质Q
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)由元素②和④形成的三核直线形分子的结构式为
(3)用电子式表示元素⑤和⑦的原子形成的化合物(该化合物含有三个原子核)的形成过程
(4)由上述元素④和⑤构成的淡黄色固体,该化合物所含的化学键类型为
(5)元素⑦、⑧、⑨的离子半径由大到小的顺序是
(6)能比较元素⑦和⑧非金属性强弱的实验事实是
a.⑦的氢化物的酸性比⑧的氢化物的酸性弱
b.⑧的单质R2与H2化合比⑦的单质Q与H2化合容易,且HR的稳定性比H2Q强
c.在⑦的氢化物H2Q的水溶液中通少量⑧的单质R2气体可置换出单质Q
您最近一年使用:0次
试卷分析
导出
整体难度:适中
考查范围:认识化学科学、常见无机物及其应用、物质结构与性质、化学实验基础
试卷题型(共 22题)
题型
数量
单选题
15
填空题
3
解答题
4
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 物质的转化 焰色试验 铁 | |
| 2 | 0.94 | 化学用语综合判断 | |
| 3 | 0.65 | 阿伏加德罗定律的应用 原子中相关数值及其之间的相互关系 | |
| 4 | 0.85 | 氧化还原反应在生活、生产中的应用 有关铁及其化合物转化的流程题型 物质分离、提纯综合应用 常见无机物的制备 | |
| 5 | 0.65 | 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 6 | 0.65 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 7 | 0.85 | 物质的分离、提纯 | |
| 8 | 0.65 | 化学方程式计算中物质的量的运用 铁的氧化物 | |
| 9 | 0.65 | 限定条件下的离子共存 硝酸的强氧化性 碳酸氢钠与酸反应 Fe3+的检验 | |
| 10 | 0.85 | 氧化还原反应的几组概念 氧化还原反应有关计算 | |
| 11 | 0.4 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 | |
| 12 | 0.65 | 二氧化硫与其他强氧化剂的反应 硫酸根离子的检验 过氧化钠与水的反应 | |
| 13 | 0.4 | 根据n=m/M的相关计算 限定条件下的离子共存 常见阳离子的检验 常见阴离子的检验 | |
| 14 | 0.65 | 无机物质的分类 同主族元素性质递变规律 化学键基本概念 氢键概念及特征 | |
| 15 | 0.65 | 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 “位构性”关系理解及应用 共价键概念及判断 | |
| 二、填空题 | |||
| 16 | 0.65 | 同周期元素性质递变规律探究实验 同主族元素性质递变规律探究实验 | |
| 18 | 0.65 | 氧化还原反应方程式的配平 电子转移计算 | |
| 20 | 0.65 | 氧化还原反应有关计算 氯气与碱溶液反应 | |
| 三、解答题 | |||
| 17 | 0.65 | 元素金属性、非金属性强弱探究实验 物质性质实验方案的设计 | 实验探究题 |
| 19 | 0.65 | 氯气的实验室制法 铁与非金属单质反应 物质制备的探究 | 实验探究题 |
| 21 | 0.85 | 原子、离子、原子团及其电子式的书写与判断 离子方程式的书写 基于氧化还原反应守恒规律的计算 过滤 | 工业流程题 |
| 22 | 0.4 | 元素非金属性强弱的比较方法 微粒半径大小的比较方法 元素、核素、同位素 化学键概念理解及判断 | 无机推断题 |



