工业上已经实现 与
与 反应合成甲醇。在一恒温、恒容密闭容器中充入
反应合成甲醇。在一恒温、恒容密闭容器中充入 和
和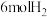 ,一定条件下发生反应:
,一定条件下发生反应: :测得
:测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
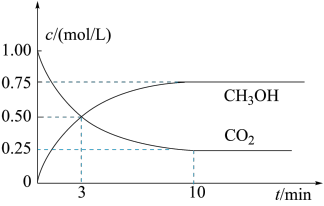
请回答:
(1)该密闭容器的容积是_______ L;
(2)达到平衡状态的时刻是_______  (填“
(填“ ”或“
”或“ ”);
”);
(3)在前 内,用
内,用 浓度的变化表示的反应速率
浓度的变化表示的反应速率
_______  ;
;
(4) 时体系的压强与开始时压强之比为
时体系的压强与开始时压强之比为_______ ;
(5)已知:①
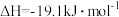
②
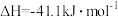
则 与
与 反应合成
反应合成 的热化学方程式为
的热化学方程式为_______ ,反应在 内所放出的热量为
内所放出的热量为_______ kJ。
 与
与 反应合成甲醇。在一恒温、恒容密闭容器中充入
反应合成甲醇。在一恒温、恒容密闭容器中充入 和
和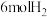 ,一定条件下发生反应:
,一定条件下发生反应: :测得
:测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
请回答:
(1)该密闭容器的容积是
(2)达到平衡状态的时刻是
 (填“
(填“ ”或“
”或“ ”);
”);(3)在前
 内,用
内,用 浓度的变化表示的反应速率
浓度的变化表示的反应速率
 ;
;(4)
 时体系的压强与开始时压强之比为
时体系的压强与开始时压强之比为(5)已知:①

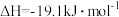
②

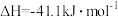
则
 与
与 反应合成
反应合成 的热化学方程式为
的热化学方程式为 内所放出的热量为
内所放出的热量为
更新时间:2021-03-24 15:44:51
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】请回答下列问题:
(1)已知H-O键能为463 kJ·mol-1,O=O键能为498 kJ·mol-1。若1 mol氢气完全燃烧生成1 mol气态水放出241 kJ的热量,计算H-H键能为______ kJ·mol-1。
(2)已知化学方程式:H2(g)+ O2(g) ==H2O(g),该反应的活化能为167.2 kJ·mol-1,其逆反应的活化能为409.0 kJ·mol-1,写出该反应的逆反应的热化学方程式:
O2(g) ==H2O(g),该反应的活化能为167.2 kJ·mol-1,其逆反应的活化能为409.0 kJ·mol-1,写出该反应的逆反应的热化学方程式: ________ 。
(3)4Al(s)+3O2(g)==2Al2O3(s)ΔH1,4Fe(s)+3O2(g)==2Fe2O3(s)ΔH2,则ΔH1________ ΔH2(选填“﹥”、“﹤”或“﹦”)。
(1)已知H-O键能为463 kJ·mol-1,O=O键能为498 kJ·mol-1。若1 mol氢气完全燃烧生成1 mol气态水放出241 kJ的热量,计算H-H键能为
(2)已知化学方程式:H2(g)+
 O2(g) ==H2O(g),该反应的活化能为167.2 kJ·mol-1,其逆反应的活化能为409.0 kJ·mol-1,写出该反应的逆反应的热化学方程式:
O2(g) ==H2O(g),该反应的活化能为167.2 kJ·mol-1,其逆反应的活化能为409.0 kJ·mol-1,写出该反应的逆反应的热化学方程式: (3)4Al(s)+3O2(g)==2Al2O3(s)ΔH1,4Fe(s)+3O2(g)==2Fe2O3(s)ΔH2,则ΔH1
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】根据要求写出下列反应的热化学方程式
(1)一定量氢气与氯气反应生成氯化氢气体,当生成1mol氢氯键时放出91.5kJ的热量______________________ .
(2)某化学反应的能量变化如图所示,该反应的热化学方程式是(反应热用abc表示)_____________________ .

(3)某反应的平衡常数 如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式
如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式_______________ .
(4)实验中不能直接测出石墨和氢气生成甲烷反应的反应热,但可测出甲烷、石墨、氢气燃烧的反应热:
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H1=-890.3kJ/mol
C(石墨,s)+O2(g)=CO2(g) ;ΔH2=-393.5 kJ/mol
H2(g)+1/2O2(g)=H2O(l) ;△H3=-285.8 kJ/moL
则由石墨与氢气反应生成甲烷的热化学反应方程式为____________________ .
(1)一定量氢气与氯气反应生成氯化氢气体,当生成1mol氢氯键时放出91.5kJ的热量
(2)某化学反应的能量变化如图所示,该反应的热化学方程式是(反应热用abc表示)

(3)某反应的平衡常数
 如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式
如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式(4)实验中不能直接测出石墨和氢气生成甲烷反应的反应热,但可测出甲烷、石墨、氢气燃烧的反应热:
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H1=-890.3kJ/mol
C(石墨,s)+O2(g)=CO2(g) ;ΔH2=-393.5 kJ/mol
H2(g)+1/2O2(g)=H2O(l) ;△H3=-285.8 kJ/moL
则由石墨与氢气反应生成甲烷的热化学反应方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(l)ΔH=﹣570 kJ•
②2H2O(g)=2H2(g)+O2(g)ΔH=+483.6kJ•
③2C(s)+O2(g)=2CO(g)ΔH=﹣220.8 kJ•
④C(s)+O2(g)=CO2(g)ΔH=﹣393.5 kJ•
回答下列问题:
(1)上述反应中属于吸热反应的是_______ (填写序号)。
(2)H2的燃烧热为________ 。
(3)燃烧10 g H2生成液态水,放出的热量为________ 。
(4)CO的燃烧热的热化学方程式为______________________ 。
(5)H2O(l)=H2O(g)ΔH=__________ 。
①2H2(g)+O2(g)=2H2O(l)ΔH=﹣570 kJ•

②2H2O(g)=2H2(g)+O2(g)ΔH=+483.6kJ•

③2C(s)+O2(g)=2CO(g)ΔH=﹣220.8 kJ•

④C(s)+O2(g)=CO2(g)ΔH=﹣393.5 kJ•

回答下列问题:
(1)上述反应中属于吸热反应的是
(2)H2的燃烧热为
(3)燃烧10 g H2生成液态水,放出的热量为
(4)CO的燃烧热的热化学方程式为
(5)H2O(l)=H2O(g)ΔH=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
Ⅰ.已知:①2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0 kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+180.5 kJ·mol-1
③2NO(g)+O2(g)=2NO2(g) ΔH3=-116.5 kJ·mol-1
(1)CO的燃烧热为______________ 。
(2)若1 mol N2(g)、1 mol O2(g)分子中化学键断裂时分别需要吸收946 kJ、498 kJ的能量,则1 mol NO(g)分子中化学键断裂时需吸收的能量为________ 。
Ⅱ.利用水煤气合成二甲醚的总反应为:
3CO(g)+3H2(g)=CH3OCH3(g)+CO2(g) ΔH=-246.4 kJ·mol-1
(3)它可以分为两步,反应分别如下:
①2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) ΔH1=-205.1 kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=________ 。
(4)已知CH3OCH3(g)的燃烧热为1455 kJ·mol-1,写出表示其燃烧热的热化学方程式:_________________________________ 。若二甲醚燃烧生成的CO2恰好能被100 mL 0.2 mol·L-1 NaOH溶液吸收生成Na2CO3,则燃烧过程中放出的热量为________ 。
Ⅰ.已知:①2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0 kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+180.5 kJ·mol-1
③2NO(g)+O2(g)=2NO2(g) ΔH3=-116.5 kJ·mol-1
(1)CO的燃烧热为
(2)若1 mol N2(g)、1 mol O2(g)分子中化学键断裂时分别需要吸收946 kJ、498 kJ的能量,则1 mol NO(g)分子中化学键断裂时需吸收的能量为
Ⅱ.利用水煤气合成二甲醚的总反应为:
3CO(g)+3H2(g)=CH3OCH3(g)+CO2(g) ΔH=-246.4 kJ·mol-1
(3)它可以分为两步,反应分别如下:
①2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) ΔH1=-205.1 kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=
(4)已知CH3OCH3(g)的燃烧热为1455 kJ·mol-1,写出表示其燃烧热的热化学方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】“西气东输”是我国开发的重点工程,这里的气是指天然气,其主要成分是甲烷。工业上将碳与水在高温下反应制得水煤气,水煤气的主要成分是CO和H2,二者的体积比为1:1。已知1 molCO气体完全燃烧生成CO2气体放出282. 6kJ热量; 1mol氢气完全燃烧生成液态水放出285. 8kJ热量;1molCH4气体完全燃烧生成CO2气体和液态水放出889. 6kJ热量。
(1)写出氢气完全燃烧生成液态水的热化学方程式:_________ 。
(2)若1molCH4 气体完全燃烧生成CO2气体和水蒸气, 放出的热量______ (填“大于”“等于”或“小于”)889. 6kJ。
(3)忽略水煤气中其他成分,相同状况下若得到相等的热量,所需水煤气与甲烷的体积比约为________ (整数比)。
(1)写出氢气完全燃烧生成液态水的热化学方程式:
(2)若1molCH4 气体完全燃烧生成CO2气体和水蒸气, 放出的热量
(3)忽略水煤气中其他成分,相同状况下若得到相等的热量,所需水煤气与甲烷的体积比约为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】已知下列反应:2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1,Na2O2(s)+CO2(g)=Na2CO3(s)+  O2(g) ΔH=-266kJ·mol-1,试回答:
O2(g) ΔH=-266kJ·mol-1,试回答:
(1)CO的燃烧热ΔH=_______________ 。
(2)在催化剂作用下,一氧化碳可与过氧化钠反应生成固体碳酸钠,该反应的热化学方程式为:________ 。
(3)工业废气中的CO2可用碱液吸收,所发生的反应如下:CO2(g)+2NaOH(aq)=Na2CO3(aq)+H2O(l) ΔH=-a kJ·mol-1,CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-bkJ·mol-1,则:
①CO2(g)+H2O(l)+Na2CO3(aq)=2NaHCO3(aq)的ΔH=________ kJ·mol-1(用含a、b的代数式表示)。
②标况下,11.2LCO2与足量的NaOH溶液充分反应后,放出的热量为_______ kJ(用含a或b的代数式表示)。
(4)根据以下三个热化学方程式:2H2S(g)+3O2(g)= 2SO2 (g) +2H2O (l) ΔH=-Q1kJ·mol-1,2H2S(g)+O2(g)= 2S (s) +2H2O (l) ΔH=-Q2kJ·mol-1,2H2S(g)+O2(g)=2 S (s) +2H2O (g) ΔH=-Q3kJ·mol-1,判断Q1、Q2、Q3的大小关系是____ 。
 O2(g) ΔH=-266kJ·mol-1,试回答:
O2(g) ΔH=-266kJ·mol-1,试回答:(1)CO的燃烧热ΔH=
(2)在催化剂作用下,一氧化碳可与过氧化钠反应生成固体碳酸钠,该反应的热化学方程式为:
(3)工业废气中的CO2可用碱液吸收,所发生的反应如下:CO2(g)+2NaOH(aq)=Na2CO3(aq)+H2O(l) ΔH=-a kJ·mol-1,CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-bkJ·mol-1,则:
①CO2(g)+H2O(l)+Na2CO3(aq)=2NaHCO3(aq)的ΔH=
②标况下,11.2LCO2与足量的NaOH溶液充分反应后,放出的热量为
(4)根据以下三个热化学方程式:2H2S(g)+3O2(g)= 2SO2 (g) +2H2O (l) ΔH=-Q1kJ·mol-1,2H2S(g)+O2(g)= 2S (s) +2H2O (l) ΔH=-Q2kJ·mol-1,2H2S(g)+O2(g)=2 S (s) +2H2O (g) ΔH=-Q3kJ·mol-1,判断Q1、Q2、Q3的大小关系是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】某温度时, 在一个2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
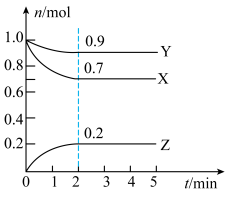
(1)该反应的化学方程式为_____________________________ 。
(2)反应开始至2 min,以气体Z表示的平均反应速为___________________________ 。
(3)若X、Y、Z均为气体,2 min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的_____________ 倍;
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时___ (填”增大”“减小”或”相等”)。

(1)该反应的化学方程式为
(2)反应开始至2 min,以气体Z表示的平均反应速为
(3)若X、Y、Z均为气体,2 min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】将3molA和3molB混合于2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,C的平均反应速率为0.15mol/(L·min)。试求:
xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,C的平均反应速率为0.15mol/(L·min)。试求:
(1)5min后A的浓度________ 。
(2)B的平均反应速率为_____ 。
(3)x的值为____ 。
(4)下列叙述能说明该反应已达到化学平衡状态的是(填字母)_____ 。
A.υ(A)=3υ(B)
B.B的浓度不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗xmol的C的同时生成3mol的A
E.相同时间内消耗2mol的D的同时消耗1mol的B
 xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,C的平均反应速率为0.15mol/(L·min)。试求:
xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,C的平均反应速率为0.15mol/(L·min)。试求:(1)5min后A的浓度
(2)B的平均反应速率为
(3)x的值为
(4)下列叙述能说明该反应已达到化学平衡状态的是(填字母)
A.υ(A)=3υ(B)
B.B的浓度不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗xmol的C的同时生成3mol的A
E.相同时间内消耗2mol的D的同时消耗1mol的B
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】I.用水煤气制天然气的反应过程涉及如下反应:CO(g)+3H2(g)⇌CH4(g)+H2O(g)。现在300°C、容积为2 L的密闭容器中进行有关合成天然气的实验,相关数据记录如下:
根据表中信息回答下列问题:
(1)前30 min内该反应的平均反应速率v(H2)____________ 。
(2)反应达到平衡后,点燃混合气体,充分燃烧后消耗氧气的物质的量为__________ mol。
II.某有机物由碳、氢、氧、氮4种元素组成,其中含碳32%,氢6.7%,氮18.7% (均为质量分数)。该有机物的相对分子质量为75。
(3)通过计算写出该有机物的分子式___________ 。
(4)该有机物是蛋白质水解的产物,它与乙醇反应生成的酯可用于合成医药和农药,请写出生成该酯的化学方程式_______________ 。
| 时间 | CO/mol | H2/mol | CH4/mol | H2O/mol |
| 0 min | 4 | 40 | 0 | 0 |
| 30 min | 2 |
根据表中信息回答下列问题:
(1)前30 min内该反应的平均反应速率v(H2)
(2)反应达到平衡后,点燃混合气体,充分燃烧后消耗氧气的物质的量为
II.某有机物由碳、氢、氧、氮4种元素组成,其中含碳32%,氢6.7%,氮18.7% (均为质量分数)。该有机物的相对分子质量为75。
(3)通过计算写出该有机物的分子式
(4)该有机物是蛋白质水解的产物,它与乙醇反应生成的酯可用于合成医药和农药,请写出生成该酯的化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】为测定镀锌铁皮锌镀层厚度[ρ(Zn)=7.14g•cm-3],某兴趣小组同学截取三块形状规则、大小相近的长方形铁皮(来自同一块镀锌铁皮),量出其长度与宽度,计算得铁片单侧面积;用稀硫酸进行定量试验,数据如下:
该镀锌铁皮锌镀层厚度为___ cm(保留2位有效数字);写出简要计算过程。
| 实验序号 | 铁片单侧面积/cm2 | 反应前质量/g | 反应后质量/g |
| 1 | 25.05 | 14.625 | 13.803 |
| 2 | 24.95 | 14.566 | 13.746 |
| 3 | 24.89 | 14.489 | 12.789 |
该镀锌铁皮锌镀层厚度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】已知: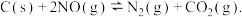
 时.某研究小组向一恒容真空容器中充入NO和足量的碳单质,恒温条件下测得不同时间各物质的浓度如表.
时.某研究小组向一恒容真空容器中充入NO和足量的碳单质,恒温条件下测得不同时间各物质的浓度如表.
 以v(NO)表示的平均反应速率为
以v(NO)表示的平均反应速率为 ______ .
 根据表中数据,计算平衡时的NO转化率为
根据表中数据,计算平衡时的NO转化率为 ______ .
 根据表中数据,计算
根据表中数据,计算 时该反应的平衡常数为
时该反应的平衡常数为 ______ .
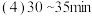 改变的实验条件是
改变的实验条件是 ______ .
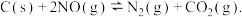
 时.某研究小组向一恒容真空容器中充入NO和足量的碳单质,恒温条件下测得不同时间各物质的浓度如表.
时.某研究小组向一恒容真空容器中充入NO和足量的碳单质,恒温条件下测得不同时间各物质的浓度如表. 浓度 时间  | NO |  |  |
| 0 |  | 0 | 0 |
| 10 | 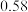 | 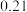 | 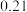 |
| 20 |  | 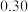 | 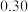 |
| 30 |  | 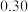 | 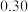 |
| 35 |  | 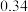 | 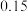 |
 以v(NO)表示的平均反应速率为
以v(NO)表示的平均反应速率为  根据表中数据,计算平衡时的NO转化率为
根据表中数据,计算平衡时的NO转化率为  根据表中数据,计算
根据表中数据,计算 时该反应的平衡常数为
时该反应的平衡常数为 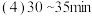 改变的实验条件是
改变的实验条件是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】向1L恒容密闭容器中加入12g活性炭和NO,发生反应: ∆H。在
∆H。在 下,反应进行到不同时刻测得各物质浓度的部分数据如下:
下,反应进行到不同时刻测得各物质浓度的部分数据如下:
(1)10min时,混合气体的平均摩尔质量为_______ 。
(2)T1℃时,该反应的平衡常数K=_______ 。
(3)30min后,若只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是_______ (填字母)。
a.加入一定量的活性炭 b.改变反应体系的温度
c.缩小容器的体积 d.通入一定量的NO
(4)若30min后升高温度至 ,重新达到平衡时,容器中NO、
,重新达到平衡时,容器中NO、 、
、 的浓度之比为7:3:3,则该反应的∆H
的浓度之比为7:3:3,则该反应的∆H______ (填“<”、“=”或“>”)0
 ∆H。在
∆H。在 下,反应进行到不同时刻测得各物质浓度的部分数据如下:
下,反应进行到不同时刻测得各物质浓度的部分数据如下:
(1)10min时,混合气体的平均摩尔质量为
(2)T1℃时,该反应的平衡常数K=
(3)30min后,若只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是
a.加入一定量的活性炭 b.改变反应体系的温度
c.缩小容器的体积 d.通入一定量的NO
(4)若30min后升高温度至
 ,重新达到平衡时,容器中NO、
,重新达到平衡时,容器中NO、 、
、 的浓度之比为7:3:3,则该反应的∆H
的浓度之比为7:3:3,则该反应的∆H
您最近一年使用:0次



