如表是元素周期表的一部分,针对表中①~⑩种元素,填写下列空白:
(1)同位素在生活生产和科学研究中有着重要的用途。例如,考古时利用___________ (填核素符号)测定一些文物的年代。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是___________ ,碱性最强的化合物的化学式是___________ 。
(3)写出⑤和⑦的最高价氧化物的水化物反应的离子方程式___________ 。
(4)元素①与⑧形成的化合物属于___________ (填“共价”或“离子”)化合物。
(5)若要比较⑤比⑥的金属性强弱,下列实验方法可行的是___________ 。
A.将单质⑤置于⑥的盐溶液中,如果⑤不能置换出单质⑥,说明⑤的金属性弱
B.比较⑤和⑥的最高价氧化物对应水化物的水溶性,前者比后者溶解度大,故前者金属性强
C.将⑤和⑥的单质分别投入到水中,观察到⑤与水反应更剧烈,说明⑤的金属性强
D.将⑤和⑥的单质分别在O2中燃烧,前者得到氧化物的颜色比后者得到氧化物的颜色深,则前者金属性强
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)写出⑤和⑦的最高价氧化物的水化物反应的离子方程式
(4)元素①与⑧形成的化合物属于
(5)若要比较⑤比⑥的金属性强弱,下列实验方法可行的是
A.将单质⑤置于⑥的盐溶液中,如果⑤不能置换出单质⑥,说明⑤的金属性弱
B.比较⑤和⑥的最高价氧化物对应水化物的水溶性,前者比后者溶解度大,故前者金属性强
C.将⑤和⑥的单质分别投入到水中,观察到⑤与水反应更剧烈,说明⑤的金属性强
D.将⑤和⑥的单质分别在O2中燃烧,前者得到氧化物的颜色比后者得到氧化物的颜色深,则前者金属性强
更新时间:2021-03-27 11:40:03
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】回答以下关于元素及其化合物的问题。
(1)Na原子核外有________ 种不同能量的电子,其离子最外层电子的轨道表示式________ 。
(2)相同压强下,部分元素氟化物的熔点见下表:
①试解释上表中氟化物熔点差异的原因:___________ 。
② 分子的空间构型为
分子的空间构型为___________ , 中Si—F键间的键角是
中Si—F键间的键角是___________ 。
(3)元素周期表有多种形式。下图分别是三种不同形式元素周期表的局部区域。

①图A中,数值越大,则该元素的___________ (填“金属性”或“非金属性”)越强。写出能说明O、F两元素该性质强弱的化学方程式___________ 。
②根据图B预测,整个周期表中位置最低的元素应位于___________ (放射性元素除外)。图B所示第二周期主族元素中,某元素该性质反常偏高,则该元素原子核外电子排布式为___________ 。
③图C表示的意义是___________ 。
(4)元素周期表中,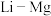 、
、 、
、 处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。
处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。
(1)Na原子核外有
(2)相同压强下,部分元素氟化物的熔点见下表:
| 氟化物 |  |  |  |
| 熔点/℃ | 1266 | 1534 | 183 |
②
 分子的空间构型为
分子的空间构型为 中Si—F键间的键角是
中Si—F键间的键角是(3)元素周期表有多种形式。下图分别是三种不同形式元素周期表的局部区域。

①图A中,数值越大,则该元素的
②根据图B预测,整个周期表中位置最低的元素应位于
③图C表示的意义是
(4)元素周期表中,
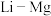 、
、 、
、 处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。
处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。A. 易溶于水 易溶于水 | B. |
C. 熔点高 熔点高 | D.晶体硼为分子晶体 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】下表为元素周期表的一部分,其中编号代表对应的元素。
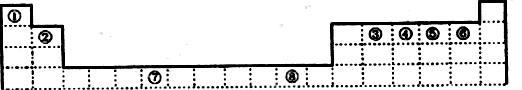
请回答下列问题:
(1)写出元素⑦的基态原子外围电子排布式________________ ,元素⑧位于_______ 区。⑤元素原子的价层电子的电子排布图为_____________________ ;
(2)若元素①③⑤形成的某化合物显酸性,经测定这三种元素的质量比为1:6:16,该化合物对氢气的相对密度为23,则其中所有杂化原子的杂化方式分别为___________ 和________________ 。
(3)元素③④⑤⑥的第一电离能由大到小的顺序是_________ (用元素符号表示)。请写出由④和⑤两种元素形成的与N3ˉ互为等电子体的分子的化学式________________ ,(写出一种即可)其VSEPR构型为___________ 。
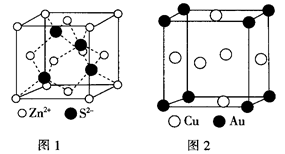
(4)ZnS的晶胞结构如图1所示,在ZnS晶胞中,S2-的配位数为___________ 。
(5)铜能与类卤素(SCN)2分子(与氯气分子性质相似)反应生成Cu(SCN)2,1mol(SCN)2分子中含有共价键的数目为______________ 。铜与金形成的金属互化物结构如图2,其晶胞边长为a nm,该金属互化物的密度为__________ (用含“a、NA的代数式表示)g/cm3)。

请回答下列问题:
(1)写出元素⑦的基态原子外围电子排布式
(2)若元素①③⑤形成的某化合物显酸性,经测定这三种元素的质量比为1:6:16,该化合物对氢气的相对密度为23,则其中所有杂化原子的杂化方式分别为
(3)元素③④⑤⑥的第一电离能由大到小的顺序是
(4)ZnS的晶胞结构如图1所示,在ZnS晶胞中,S2-的配位数为
(5)铜能与类卤素(SCN)2分子(与氯气分子性质相似)反应生成Cu(SCN)2,1mol(SCN)2分子中含有共价键的数目为

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】下表是元素周期表的一部分,针对表中的①~⑨九种元素,填写下列空白:

I.(1)在最高价氧化物的水化物中,酸性最强的化合物的化学式是___ ,碱性最强的化合物的电子式是____ 。
(2)最高价氧化物是两性的氧化物与氢氧化钠反应的离子方程式____ 。
(3)用电子式表示元素④与⑥形成的化合物的过程:___ ,该化合物属于___ (填“共价”或“离子”)化合物。
(4)表示①与⑦形成的化合物的电子式____ 。
(5)判断④、⑤、⑥原子半径的大小顺序____ (用元素符号或化学式表示,下同),比较③和⑥的气态氢化物的稳定性大小___ 。
II.A、B、C、D、F是由上表中的元素构成的五种物质,且焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃气体。而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊。D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体。请回答下列问题:
(1)写出A、E的化学式:A____ ,E____
(2)常温常压下制取100mL纯净的H,将其通入装有F粉末的两通玻璃管中。
①反应的化学方程式为_______ 。
②若反应后收集的气体体积为65mL,则反应消耗H的体积是_______ mL。

I.(1)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(2)最高价氧化物是两性的氧化物与氢氧化钠反应的离子方程式
(3)用电子式表示元素④与⑥形成的化合物的过程:
(4)表示①与⑦形成的化合物的电子式
(5)判断④、⑤、⑥原子半径的大小顺序
II.A、B、C、D、F是由上表中的元素构成的五种物质,且焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃气体。而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊。D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体。请回答下列问题:
(1)写出A、E的化学式:A
(2)常温常压下制取100mL纯净的H,将其通入装有F粉末的两通玻璃管中。
①反应的化学方程式为
②若反应后收集的气体体积为65mL,则反应消耗H的体积是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】某化学兴趣小组利用如下图装置验证元素非金属性的变化规律。

(1)仪器A的名称为________ ,干燥管D的作用是________ 。
(2)实验室中现有药品KMnO4、MnO2、浓盐酸、Na2S,请选择合适药品设计实验验证非金属性:Cl>S,装置A、B、C中所装药品应分别为浓盐酸、________ 、Na2S溶液,装置C中的实验现象为有淡黄色沉淀生成,装置C中发生反应的离子方程式为____________ 。
(3)若利用上装置证明非金属性:S>C>Si。在A中加入稀硫酸、B中加入Na2CO3溶液、C中加入Na2SiO3溶液,观察到B中产生气泡,试管C中出现________ 现象,则可以证明非金属性:S>C>Si。若将A中的稀硫酸改为稀盐酸,试管C中会出现同样的现象,是否可以得出结论:非金属性Cl>C>Si?__________ (填“是”或“否”),你的理由是______________________ 。

(1)仪器A的名称为
(2)实验室中现有药品KMnO4、MnO2、浓盐酸、Na2S,请选择合适药品设计实验验证非金属性:Cl>S,装置A、B、C中所装药品应分别为浓盐酸、
(3)若利用上装置证明非金属性:S>C>Si。在A中加入稀硫酸、B中加入Na2CO3溶液、C中加入Na2SiO3溶液,观察到B中产生气泡,试管C中出现
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】部分短周期元素的原子结构及相关性质如表所示:
(1)T在元素周期表中的位置为 ______。
(2)X的一种同位素可用于测定文物年代,该同位素为 ______ (用原子符号表示)。
(3)Z单质的电子式为____ ;Y的氢化物的水溶液显碱性的原因为_____(用离子方程式表示)。
(4)Z与T相比,非金属性较强的是__(用元素符号表示),下列能证明这一事实的是 (填字母)
a.常温下,Z单质为气体,T单质为固体
b.Z的氢化物的水溶液的酸性比T强
c.Z的最高正价比Y高
d.最高价氧化物对应水化物的酸性Z比T强
(5)Z的氢化物与Y的氢化物发生反应的化学方程式为 ,产物中含有的化学键类型为 。
| 元素编号 | 元素性质或原子结构 |
| T | 最高正价与最低负价的代数和为4 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 最高正价是+7价 |
(1)T在元素周期表中的位置为 ______。
(2)X的一种同位素可用于测定文物年代,该同位素为 ______ (用原子符号表示)。
(3)Z单质的电子式为____ ;Y的氢化物的水溶液显碱性的原因为_____(用离子方程式表示)。
(4)Z与T相比,非金属性较强的是__(用元素符号表示),下列能证明这一事实的是 (填字母)
a.常温下,Z单质为气体,T单质为固体
b.Z的氢化物的水溶液的酸性比T强
c.Z的最高正价比Y高
d.最高价氧化物对应水化物的酸性Z比T强
(5)Z的氢化物与Y的氢化物发生反应的化学方程式为 ,产物中含有的化学键类型为 。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期表的重要性。下表列出了a~j10种元素在周期表中的位置:
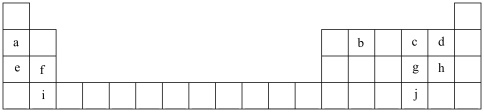
(1)元素a的原子结构示意图为___________ 。
(2)元素b可以形成多种单质,写出其中的两种___________ (填名称)。
(3)元素a~j中非金属性最强的是___________ (填元素符号)。
(4)若e单质着火,可用于灭火的物质是___________(填字母)。
(5)h单质与NaOH溶液反应的离子方程式为___________ 。
(6)元素b、e的最高价氧化物发生反应的化学方程式为___________ 。
(7)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法中正确的有___________(填字母)。
(8)NA为阿伏加德罗常数的值,已知ag某气体中含有的分子数为b,则该气体的摩尔质量为___________  。标准状况下,密度为
。标准状况下,密度为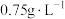 的
的 与
与 组成的混合气体中,
组成的混合气体中, 的体积分数为
的体积分数为___________ 。取均为0.2mol的金属钠、铁、铝,分别投入 盐酸中,产生
盐酸中,产生 的体积(相同状况下)比为
的体积(相同状况下)比为___________ 。

(1)元素a的原子结构示意图为
(2)元素b可以形成多种单质,写出其中的两种
(3)元素a~j中非金属性最强的是
(4)若e单质着火,可用于灭火的物质是___________(填字母)。
| A.自来水 | B. | C.干沙子 | D.湿抹布 |
(5)h单质与NaOH溶液反应的离子方程式为
(6)元素b、e的最高价氧化物发生反应的化学方程式为
(7)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法中正确的有___________(填字母)。
| A.a的金属性比e的弱 | B.自然界中,e的储量比a的高 |
| C.a的原子半径比e的大 | D.基于a的电池质量轻、易携带 |
(8)NA为阿伏加德罗常数的值,已知ag某气体中含有的分子数为b,则该气体的摩尔质量为
 。标准状况下,密度为
。标准状况下,密度为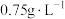 的
的 与
与 组成的混合气体中,
组成的混合气体中, 的体积分数为
的体积分数为 盐酸中,产生
盐酸中,产生 的体积(相同状况下)比为
的体积(相同状况下)比为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】A、B、C、D是原子序数依次增大的短周期主族元素,A、C在元素周期表中的相对位置如图,A元素最外层与次外层的电子数之差为3,B为地壳中含量最多的金属元素。

(1)D原子结构示意图为_______ 。
(2)将C的低价态氧化物甲中通入到D单质的水溶液会使之褪色,体现了甲的_______ 性,写出该反应的离子方程式_______ 。
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到100mL8.0mol/L乙的浓溶液中,充分反应,共收集到6.72L(标准状况)气体,则该气体的成分是_______ ,还原剂失电子数为_______ 。
(4)将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,充分反应生成气体的体积比为_______ ,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为_______ ;B单质表面的氧化膜可用NaOH溶液除去,写出该反应的化学方程式_______ 。

(1)D原子结构示意图为
(2)将C的低价态氧化物甲中通入到D单质的水溶液会使之褪色,体现了甲的
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到100mL8.0mol/L乙的浓溶液中,充分反应,共收集到6.72L(标准状况)气体,则该气体的成分是
(4)将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,充分反应生成气体的体积比为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】如表是元素周期表的一部分,参照元素在表中的位置,请用化学用语 回答下列问题:
(1)这些元素中,化学性质最不活泼原子的原子结构示意图为__________ ;气态氢化物中,最稳定的是___________ ;最高价氧化物对应水化物中,酸性最强的是______________ 。
(2)①和④两种元素的原子按1:1组成的常见化合物的电子式为___________________ 。
(3)②、③的单质中更容易与①的单质反应的是___________________ (用化学式表示)。
(4)④、⑦、⑧、⑨的简单离子半径由大到小的顺序为___________________ (用离子符号和“>”表示)。
(5)⑥和⑧的最高价氧化物对应水化物之间发生反应的离子方程式____________________ 。
(6)⑤⑨⑪三种元素的单质沸点由高到低的顺序是________________ (用化学式和“>”表示)。
(7)⑦⑧两元素相比较,金属性较强的是_____________ (填名称),可以验证该结论的实验是____________________ (填字母)。
A.将在空气中放置已久的这两种元素的块状单质分别放入热水中
B.将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
C.将形状、大小相同这两种元素的单质分别和热水作用,并滴入酚酞溶液
D.比较这两种元素的气态氢化物的稳定性
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
| 4 | ⑪ |
(2)①和④两种元素的原子按1:1组成的常见化合物的电子式为
(3)②、③的单质中更容易与①的单质反应的是
(4)④、⑦、⑧、⑨的简单离子半径由大到小的顺序为
(5)⑥和⑧的最高价氧化物对应水化物之间发生反应的离子方程式
(6)⑤⑨⑪三种元素的单质沸点由高到低的顺序是
(7)⑦⑧两元素相比较,金属性较强的是
A.将在空气中放置已久的这两种元素的块状单质分别放入热水中
B.将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
C.将形状、大小相同这两种元素的单质分别和热水作用,并滴入酚酞溶液
D.比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次



