测量司机是否酒后驾驶的反应原理为:3C2H5OH+2CrO3+3H2SO4=3CH3CHO+Cr2(SO4)3+6H2O请回答下列问题:
(1)该反应涉及元素中,基态原子核外未成对电子数最多的元素在元素周期表中的位置为___________ ,价电子排布式___________ 。
(2)对于Cr2(SO4)3的组成元素,电负性从小到大的顺序为___________ 。(用元素符号表示)
(3)HOCH2CN的结构简式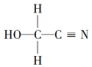 ,该分子中碳原子轨道的杂化类型分别是
,该分子中碳原子轨道的杂化类型分别是___________ 和___________ 。
(4)将CrCl3·6H2O溶解在适量水中,溶液中Cr3+以[Cr(H2O)5Cl]2+形式存在,[Cr(H2O)5Cl]2+中含有σ键的数目为___________ ;
(1)该反应涉及元素中,基态原子核外未成对电子数最多的元素在元素周期表中的位置为
(2)对于Cr2(SO4)3的组成元素,电负性从小到大的顺序为
(3)HOCH2CN的结构简式
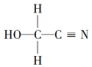 ,该分子中碳原子轨道的杂化类型分别是
,该分子中碳原子轨道的杂化类型分别是(4)将CrCl3·6H2O溶解在适量水中,溶液中Cr3+以[Cr(H2O)5Cl]2+形式存在,[Cr(H2O)5Cl]2+中含有σ键的数目为
更新时间:2021-04-15 23:40:03
|
相似题推荐
【推荐1】元素周期表中锑元素的数据如图。

(1)根据锑的价层电子排布式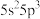 可知,锑在元素周期表中位于第
可知,锑在元素周期表中位于第_______ 周期第_______ 族。
(2)基态锑原子中有_______ 个未成对电子,这些未成对电子具有_______ (填“相同”或“不同”)的自旋状态。
(3)基态锑原子的5s轨道形状为_______ 形;该原子最外层电子占有_______ 个轨道。
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。
①下列推断正确的是_______ 。
a.电负性:Sb>Bi b.原子半径:Sb>Bi c.金属性:Sb>Bi d.氧化性: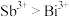
②第一电离能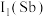
_______ (填“大于”或“小于”) 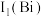 ,原因是
,原因是_______ 。

(1)根据锑的价层电子排布式
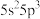 可知,锑在元素周期表中位于第
可知,锑在元素周期表中位于第(2)基态锑原子中有
(3)基态锑原子的5s轨道形状为
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。
①下列推断正确的是
a.电负性:Sb>Bi b.原子半径:Sb>Bi c.金属性:Sb>Bi d.氧化性:
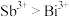
②第一电离能
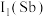
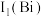 ,原因是
,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】五种元素原子的电子层结构如下:
A.1s22s22p63s23p63d54s2;B.1s22s22p63s2;C.1s22s22p6;D.1s22s22p63s23p2; E.[Ar]4s1
请回答:
(1)___________ (填字母,下同)元素是稀有气体。含未成对电子数最多的元素是___________ 。
(2)A的元素符号是___________ ,其核外电子共有___________ 种运动状态。
(3)D元素原子核外电子排布图是___________ ,总共有___________ 个能级。
A.1s22s22p63s23p63d54s2;B.1s22s22p63s2;C.1s22s22p6;D.1s22s22p63s23p2; E.[Ar]4s1
请回答:
(1)
(2)A的元素符号是
(3)D元素原子核外电子排布图是
您最近一年使用:0次
【推荐1】超强酸“魔酸”是五氟化锑 和氟磺酸
和氟磺酸 的混合物,二者的结构如图:
的混合物,二者的结构如图:

 中
中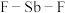 键的键角的度数分别为
键的键角的度数分别为______ ,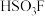 中所含元素电负性由大到小的顺序是
中所含元素电负性由大到小的顺序是______ (用元素符号表示)。
 和氟磺酸
和氟磺酸 的混合物,二者的结构如图:
的混合物,二者的结构如图:
 中
中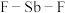 键的键角的度数分别为
键的键角的度数分别为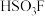 中所含元素电负性由大到小的顺序是
中所含元素电负性由大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】已知电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性:
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是_____________ 。
(2)下列物质属于离子化合物的是________ ,属于共价化合物的有________ 。
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是
(2)下列物质属于离子化合物的是
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出符合下列要求的符号。
(1)第二电子层 s能级________ 。
(2)n=3 p能级________ 。
(3)第五电子层 d能级________ 。
(4)n=4 p能级________ 。
(5)铜氨络离子的结构式________ 。
(1)第二电子层 s能级
(2)n=3 p能级
(3)第五电子层 d能级
(4)n=4 p能级
(5)铜氨络离子的结构式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在配合物 中,
中,___________ 是中心离子,___________ 是配位原子,___________ 是配位体; 的结构式为
的结构式为___________ 。
 中,
中, 的结构式为
的结构式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】回答下列问题:
(1)基态O原子核外电子的运动状态有___________ 种。
(2) 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为___________ (填化学式)。
(3)已知 与
与 的价电子数和原子数目相同,它们互为等电子体,写出与
的价电子数和原子数目相同,它们互为等电子体,写出与 互为等电子体的一种分子的化学式
互为等电子体的一种分子的化学式________ 。
(4)在 低压合成甲醇反应(
低压合成甲醇反应( )所涉及的4种物质中,沸点从高到低的顺序为
)所涉及的4种物质中,沸点从高到低的顺序为________ 。
(5) 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是_______ 。
(6) 中含氧官能团的名称为
中含氧官能团的名称为___________ 。
(7)写出高分子化合物 的单体
的单体___________ 。
(1)基态O原子核外电子的运动状态有
(2)
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(3)已知
 与
与 的价电子数和原子数目相同,它们互为等电子体,写出与
的价电子数和原子数目相同,它们互为等电子体,写出与 互为等电子体的一种分子的化学式
互为等电子体的一种分子的化学式(4)在
 低压合成甲醇反应(
低压合成甲醇反应( )所涉及的4种物质中,沸点从高到低的顺序为
)所涉及的4种物质中,沸点从高到低的顺序为(5)
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(6)
 中含氧官能团的名称为
中含氧官能团的名称为(7)写出高分子化合物
 的单体
的单体
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按照要求填空:
(1)判断下列分子的极性、分子的空间构型和中心原子的杂化方式。
(2)① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ 。
。
①既有 键,又有
键,又有 键的是
键的是_______ (用序号作答);既含有极性键又含有非极性键的极性分子的电子式为_______ ;既含有极性键又含有非极性键的非极性分子中碳原子的杂化方式为________ ;苯环中存在的大 键可表示为
键可表示为________ 。
②属于离子化合物的物质的电子式为______ ; 与
与 结构相似,则
结构相似,则 的电子式为
的电子式为_____ ; 中
中 键和
键和 键之比为
键之比为______ 。
(1)判断下列分子的极性、分子的空间构型和中心原子的杂化方式。
| 序号 | 化学式 | 分子的极性 | 空间构型 | 中心原子的杂化方式 |
| ① |  | |||
| ② |  | |||
| ③ |  | - |
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ 。
。①既有
 键,又有
键,又有 键的是
键的是 键可表示为
键可表示为②属于离子化合物的物质的电子式为
 与
与 结构相似,则
结构相似,则 的电子式为
的电子式为 中
中 键和
键和 键之比为
键之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)乙二胺( )是一种有机化合物,分子中氮、碳的杂化类型分别是
)是一种有机化合物,分子中氮、碳的杂化类型分别是______ 、______ 。
(2)元素 与N同族。预测
与N同族。预测 的氢化物分子的空间结构为
的氢化物分子的空间结构为______ 。
(3) 中,电负性最高的元素是
中,电负性最高的元素是______ ;P的______ 杂化轨道与O的 轨道形成
轨道形成______ 键。
(4)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为______ 。

 )是一种有机化合物,分子中氮、碳的杂化类型分别是
)是一种有机化合物,分子中氮、碳的杂化类型分别是(2)元素
 与N同族。预测
与N同族。预测 的氢化物分子的空间结构为
的氢化物分子的空间结构为(3)
 中,电负性最高的元素是
中,电负性最高的元素是 轨道形成
轨道形成(4)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】请填空:
(1)亚铁氰化钾(K4[Fe(CN)6])俗称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝)+3KCl,回答问题:
①K4[Fe(CN)6]中的作用力除C、N原子间的共价键外,还有___________ 和___________ 。
②C、N、O的电负性由大到小的排序为___________ 。
(2)新型储氢材料是开发利用氢能的研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
①基态Cl原子有___________ 种空间运动状态的电子,属于___________ 区(填“s”或“p”或“d”或“f”)
②LiBH4由Li+和BH 构成,与BH
构成,与BH 互为等电子体的分子为
互为等电子体的分子为___________ ,Li、Be、B元素的第一电离能由大到小排列顺序为___________ 。
③某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是___________ (填元素符号)。
(3)下列状态的镁中,电离最外层一个电子所需能量最大的是___________ (填标号)。
A.[Ne]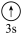 B.[Ne]
B.[Ne] 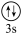 C.[Ne]
C.[Ne] 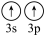 D.[Ne]
D.[Ne] 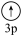
(1)亚铁氰化钾(K4[Fe(CN)6])俗称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝)+3KCl,回答问题:
①K4[Fe(CN)6]中的作用力除C、N原子间的共价键外,还有
②C、N、O的电负性由大到小的排序为
(2)新型储氢材料是开发利用氢能的研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
①基态Cl原子有
②LiBH4由Li+和BH
 构成,与BH
构成,与BH 互为等电子体的分子为
互为等电子体的分子为③某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 |
| 580 | 1820 | 2750 | 11600 |
(3)下列状态的镁中,电离最外层一个电子所需能量最大的是
A.[Ne]
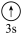 B.[Ne]
B.[Ne] 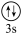 C.[Ne]
C.[Ne]  D.[Ne]
D.[Ne] 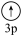
您最近一年使用:0次

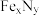 )在磁记录材料领域有着广泛的应用前景。某
)在磁记录材料领域有着广泛的应用前景。某 基态核外电子排布式为
基态核外电子排布式为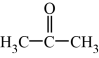 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是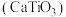 型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。
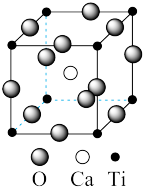
型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。 的晶胞如图所示,其组成元素的电负性大小顺序是
的晶胞如图所示,其组成元素的电负性大小顺序是 的配位数是
的配位数是