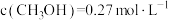在不同浓度、温度条件下,蔗糖水解的瞬时速率如下表。下列判断不正确 的是
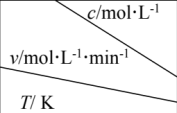 | 0.600 | 0.500 | 0.400 | 0.300 |
| 318.2 | 3.60 | 3.00 | 2.40 | 1.80 |
| 328.2 | 9.00 | 7.50 |  | 4.50 |
 | 2.16 | 1.80 | 1.44 | 1.08 |
A. |
B.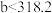 |
| C.不同温度时,蔗糖浓度减少一半所需的时间不同 |
| D.同时改变反应温度和蔗糖的浓度,蔗糖水解的瞬时速率一定改变 |
更新时间:2021-04-14 08:43:08
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】已知反应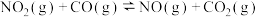
 ,下列说法正确的是
,下列说法正确的是

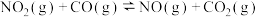
 ,下列说法正确的是
,下列说法正确的是
| A.该反应的能量变化如如图所示 |
| B.理论上该反应可以设计成原电池 |
| C.升高温度,该反应的化学反应速率不一定加快 |
D.1 mol  和1 mol 和1 mol  的总能量低于1 mol 的总能量低于1 mol  和1 mol 和1 mol  的总能量 的总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】三元WO3/C3N4/Ni(OH)x光催化剂产氢机理如图。下列说法正确的是


| A.TEOA→TEOA+为还原反应 |
| B.Ni(OH)x降低了H+→H2的活化能 |
| C.能量转化形式为太阳能→电能→化学能 |
| D.WO3没有参与制氢反应过程 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于活化能和简单碰撞理论说法正确的是
| A.活化分子间的碰撞都是有效碰撞 |
| B.催化剂之所以能改变化学反应速率,是因为它能改变反应历程,改变反应的焓变 |
| C.活化分子具有的平均能量与反应物分子具有的平均能量之差,叫做活化能 |
| D.升高温度和增加反应物浓度,都能加快反应速率,是因为增加了活化分子百分数,使单位时间内的有效碰撞次数增加,从而增加化学反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】2-甲基丙烯与HCl的加成反应有两种产物,这两种加成反应过程与其相应的能量变化曲线关系如下图所示。在恒容绝热密闭容器中通入一定量的2-甲基丙烯与HCl的混合物进行有关反应。下列说法正确的是
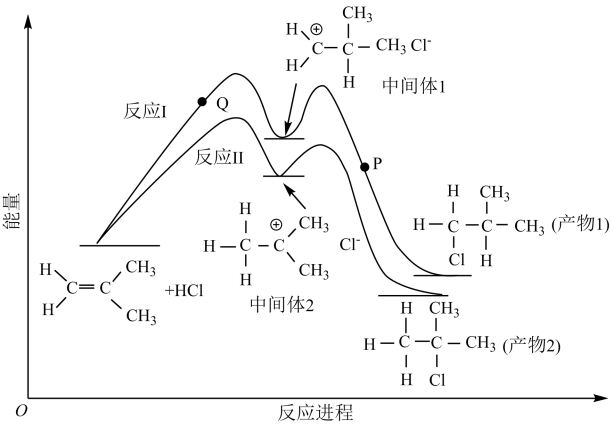

| A.产物稳定性的强弱:产物1>产物2 |
| B.反应的活化能大小:反应I>反应II |
| C.升高温度,反应I的逆反应速率变化值小于反应II的逆反应速率变化值 |
D.2-甲基丙烯与 的加成反应产物中, 的加成反应产物中,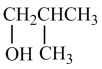 更稳定 更稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】为了探究温度和浓度对化学反应速率的影响,某同学设计了如下实验:在一张白纸上用黑色记号笔在合适的位置画上三个粗细、深浅一致的“十”字,分别在“十”字上放锥形瓶;按照表格中的试剂和条件进行反应Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,随着反应的进行,锥形瓶底部的“十”字会被遮盖。下列说法错误的是
| 实验序号 | 反应温度/℃ | Na2S2O3溶液 | 硫酸 | H2O | ||
| V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | ||
| Ⅰ | 20 | 10.0 | 0.10 | 10.0 | 0.10 | 0 |
| Ⅱ | 20 | 5.0 | 0.10 | 10.0 | 0.10 | V1 |
| Ⅲ | 40 | 10.0 | 0.10 | 10.0 | 0.10 | V2 |
| A.V1=0,V2=5.0 |
| B.实验还需要秒表,用于测定锥形瓶底部的“十”字完全被遮盖所需的时间 |
C.锥形瓶内发生反应的离子方程式 +2H+= SO2↑+S↓+H2O +2H+= SO2↑+S↓+H2O |
| D.进行实验Ⅲ时,应分别将Na2S2O3溶液和硫酸加热至40℃,然后在锥形瓶内混合 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】探究等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实验条件,下列说法中不正确的是
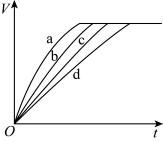
| 组别 | 对应曲线 | c(HCl)/mol·L-1 | 反应温度/°C | 铁的颗粒状态 |
| 1 | a | X | 30 | 粉末状 |
| 2 | b | 2.5 | 30 | 粉末状 |
| 3 | c | 2.5 | Y | 粉末状 |
| 4 | d | 2.5 | 30 | Z |

| A.第1、2组实验的目的是探究浓度对反应速率影响X > 2.5 |
| B.第2、3组实验的目的是探究温度对反应速率影响Y < 30 |
| C.第2、4组实验的目的是探究铁的颗粒状态对反应速率影响Z为片状 |
| D.第3组实验一定加了催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学课外小组的同学通过实验探究温度和浓度对反应速率的影响。实验原理及方案:在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生反应生成碘,反应原理是2IO +5SO
+5SO +2H+=I2+5SO
+2H+=I2+5SO +H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。
+H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。
下列判断正确的是
 +5SO
+5SO +2H+=I2+5SO
+2H+=I2+5SO +H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。
+H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。| 实验序号 | 0.01 mol·L-1 KIO3酸性溶液(含淀粉)的体积/mL | 0.01 mol·L-1 Na2SO3溶液的体积/mL | 水的体积/mL | 实验温度/℃ | 出现蓝色的时间/s |
| ① | 5 | 5 | V1 | 5 | t1 |
| ② | 5 | 5 | 40 | 25 | t2 |
| ③ | 5 | V2 | 35 | 25 | t3 |
| A.实验①③中V1=10,V2=40 |
| B.最先出现蓝色的一组是实验③ |
| C.开始出现蓝色的时间:t1<t2 |
| D.探究温度对化学反应速率的影响应该选择实验①③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 是一种新型硝化剂,在一定温度下可发生如下反应:
是一种新型硝化剂,在一定温度下可发生如下反应: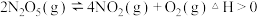 ,
, 温度时,向密闭容器中通入
温度时,向密闭容器中通入 气体,部分实验数据见下表:
气体,部分实验数据见下表:
下列说法正确的是
 是一种新型硝化剂,在一定温度下可发生如下反应:
是一种新型硝化剂,在一定温度下可发生如下反应: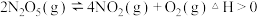 ,
, 温度时,向密闭容器中通入
温度时,向密闭容器中通入 气体,部分实验数据见下表:
气体,部分实验数据见下表:时间 | 0 | 500 | 1000 | 1500 |
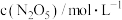 |  | 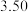 | 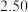 | 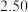 |
下列说法正确的是
A.500 s内 的生成速率为 的生成速率为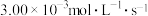 |
B. 温度下该反应平衡时 温度下该反应平衡时 的转化率为 的转化率为 |
C.达平衡后其他条件不变,将容器体积压缩到原来的 , ,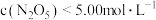 |
D. 温度下的平衡常数为 温度下的平衡常数为 , , 温度下的平衡常数为 温度下的平衡常数为 ,若 ,若 ,则 ,则 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一定条件下的恒容密闭容器中发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),图1表示反应过程中能量的变化,图2表示反应过程中物质浓度的变化。下列有关说法正确的是( )
CH3OH(g)+H2O(g),图1表示反应过程中能量的变化,图2表示反应过程中物质浓度的变化。下列有关说法正确的是( )

 CH3OH(g)+H2O(g),图1表示反应过程中能量的变化,图2表示反应过程中物质浓度的变化。下列有关说法正确的是( )
CH3OH(g)+H2O(g),图1表示反应过程中能量的变化,图2表示反应过程中物质浓度的变化。下列有关说法正确的是( )
| A.该反应的焓变和熵变:ΔH>0,ΔS<0 |
| B.温度降低,该反应的平衡常数K增大 |
| C.升高温度,n(CH3OH)/n(CO2)增大 |
| D.从反应开始到平衡,用氢气表示的平均反应速率为2.25 mol/(L·min) |
您最近一年使用:0次


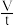 mL/s
mL/s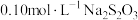 溶液与
溶液与 稀
稀 反应速率的影响。测定结果如下,下列说法
反应速率的影响。测定结果如下,下列说法 溶液/mL
溶液/mL ,“时间/s”可以是收集等量气体所需时间
,“时间/s”可以是收集等量气体所需时间 ,则上述实验①③是探究温度对化学反应速率的影响
,则上述实验①③是探究温度对化学反应速率的影响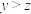
 发生反应
发生反应
 。控制两种温度(
。控制两种温度( 、
、 ),测定不同时刻容器中CO的物质的量(mol),如下表:
),测定不同时刻容器中CO的物质的量(mol),如下表: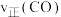 在
在