硅铝合金广泛应用于航空、交通、建筑、汽车等行业。
完成下列填空:
(1)硅原子的结构示意图为___________ ;比较硅铝的原子半径:r(Si)___________ r(Al)(选填:“>”、“<”或“=”)。硅铝合金中的铝与氢氧化钠溶液反应的化学方程式为___________ 。
(2)氟化铝和氯化铝的熔点分别为1040 和194
和194 ,它们熔点差异大的原因可能是
,它们熔点差异大的原因可能是___________ 。
(3)门捷列夫准确预测了铝、硅下一周期的同主族元素(当时并未被发现)的性质,并将他们分别命名为“类铝”和“类硅”。你据此推断类铝的最外层电子排布式为___________ ,推断的依据是___________ 。
(4)制备硅铝合金时,在高温真空炉中发生如下反应:
 ;
;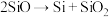 ;
;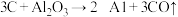
上述反应的最终还原产物为___________ ;当有1mol C参加反应时,转移的电子数目为___________ 。
完成下列填空:
(1)硅原子的结构示意图为
(2)氟化铝和氯化铝的熔点分别为1040
 和194
和194 ,它们熔点差异大的原因可能是
,它们熔点差异大的原因可能是(3)门捷列夫准确预测了铝、硅下一周期的同主族元素(当时并未被发现)的性质,并将他们分别命名为“类铝”和“类硅”。你据此推断类铝的最外层电子排布式为
(4)制备硅铝合金时,在高温真空炉中发生如下反应:
 ;
;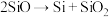 ;
;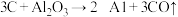
上述反应的最终还原产物为
2021·上海浦东新·二模 查看更多[3]
上海市浦东新区2021届高三二模化学试题(已下线)第15讲 原子结构 化学键(练)-2023年高考化学一轮复习讲练测(全国通用)上海市奉贤区致远高级中学2021-2022学年高二上学期期末教学评估(等级考)化学试题
更新时间:2021-04-20 15:02:44
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)已知短周期元素A、B,A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为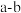 ,L层电子数为
,L层电子数为 ,则A为
,则A为___________ (填元素符号,下同),B为___________ 。
(2)已知X元素原子的L层比Y元素原子的L层少3个电子,Y元素原子的核外电子总数比X元素原子多5,则X、Y分别为___________ 、___________ 。
(1)已知短周期元素A、B,A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为
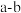 ,L层电子数为
,L层电子数为 ,则A为
,则A为(2)已知X元素原子的L层比Y元素原子的L层少3个电子,Y元素原子的核外电子总数比X元素原子多5,则X、Y分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小 的,其核外电子排布式为______ ,价电子构型为______ ,属________ 区元素。
(2)某元素原子的价电子构型为4s24p1,它属于第________ 周期________ 族,最高正化合价为________ ,元素符号是________ 。
(3)原子序数为24的元素原子中有________ 个电子层,________ 个能级,________ 个未成对电子。
(4)请写出有2个能层的p轨道中只有一个未成对电子的基态原子的外围电子排布图(有几个写几个)________________ 。
(2)某元素原子的价电子构型为4s24p1,它属于第
(3)原子序数为24的元素原子中有
(4)请写出有2个能层的p轨道中只有一个未成对电子的基态原子的外围电子排布图(有几个写几个)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据信息回答下列问题:
(1)如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
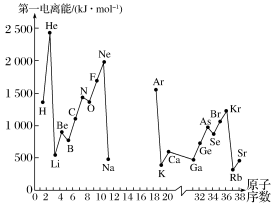
①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为________ <Al<________ (填元素符号);
②图中第一电离能最小的元素在周期表中的位置是第________ 周期________ 族。
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性。
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
①根据表中给出的数据,可推知元素的电负性具有的变化规律是______________________ ;
②通过分析电负性值变化规律,确定Mg元素电负性值的最小范围________ ;
③判断下列物质是离子化合物还是共价化合物:
A.Li3N B.BeCl2
C.AlCl3 D.SiC
Ⅰ.属于离子化合物的是________ ;
Ⅱ.属于共价化合物的是________ ;
请设计一个实验方案证明上述所得到的结论________________ 。
(1)如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。

①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
②图中第一电离能最小的元素在周期表中的位置是第
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性。
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
①根据表中给出的数据,可推知元素的电负性具有的变化规律是
②通过分析电负性值变化规律,确定Mg元素电负性值的最小范围
③判断下列物质是离子化合物还是共价化合物:
A.Li3N B.BeCl2
C.AlCl3 D.SiC
Ⅰ.属于离子化合物的是
Ⅱ.属于共价化合物的是
请设计一个实验方案证明上述所得到的结论
您最近一年使用:0次
【推荐2】开发新型储氢材料是开发利用氢能的重要研究方向。
(1) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
①基态Cl原子中,电子占据的最高电子层符号为_______ ,该电子层具有的原子轨道数为 _______ 。
②Li、B、H元素的电负性由大到小的排列顺序为___________ 。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+___________ (填“>”“=”或“<”)H-。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如表所示:
则M是 ______________ (填元素符号)。
(1)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。①基态Cl原子中,电子占据的最高电子层符号为
②Li、B、H元素的电负性由大到小的排列顺序为
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如表所示:
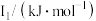 | 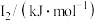 | 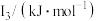 | 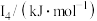 | 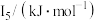 |
| 738 | 1451 | 7733 | 10540 | 13630 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】1932年美国化学家鲍林(L.Pauling)首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
(1)根据表中所给数据分析,同主族内不同元素X值的变化规律是___________ ;简述元素电负性X的大小与元素金属性、非金属性之间的关系__________________ 。
(2)预测周期表中电负性最大的元素应为_______ ,估计钙(Ca)元素电负性的取值范围 ______ < X <_______ 。
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型为___________ ,其理由是____________ 。
元素 | H | Li | Be | B | C | N | O | F |
电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
元素 | Na | Mg | Al | Si | P | S | Cl | K |
电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)根据表中所给数据分析,同主族内不同元素X值的变化规律是
(2)预测周期表中电负性最大的元素应为
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是_____
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为_____ ,氧化性最弱的简单阳离子是_____ 。
(3)已知:
工业制镁时,电解MgCl2而不电解MgO的原因是_________________ ;
制铝时,电解Al2O3而不电解AlCl3的原因是_________________ 。
(4)晶体硅(熔点1410 ℃)是良好的半导体材料。由粗硅制纯硅过程如下:
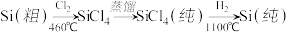
写出SiCl4的电子式:___________ ;在上述由SiCl4制纯硅的反应中,测得每生成1.12 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:_________________
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是_________________
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400 ℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:_____________________
(7)工业上,通过如下转化可制得KClO3晶体: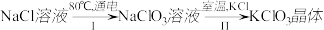
完成Ⅰ中反应的总化学方程式:
( ) NaCl+( ) H2O==( ) NaClO3+( ) H2↑
Ⅱ该反应过程能析出KClO3晶体而无其他晶体析出的原因是_____________________ 。
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是
制铝时,电解Al2O3而不电解AlCl3的原因是
(4)晶体硅(熔点1410 ℃)是良好的半导体材料。由粗硅制纯硅过程如下:
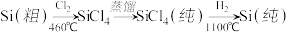
写出SiCl4的电子式:
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400 ℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:
(7)工业上,通过如下转化可制得KClO3晶体:
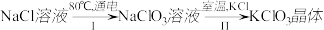
完成Ⅰ中反应的总化学方程式:
Ⅱ该反应过程能析出KClO3晶体而无其他晶体析出的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)1个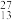 Al原子捕获1个中子能产生
Al原子捕获1个中子能产生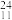 Na和X粒子,则X粒子的组成符号为:
Na和X粒子,则X粒子的组成符号为:___________ 。
(2)NaCN是离子化合物,各原子均满足8电子稳定结构,NaCN 的电子式是___________ 。
(3)相同条件下,TiF4熔点650K,TiCl4 熔点249K,熔点不同的原因是___________ 。
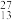 Al原子捕获1个中子能产生
Al原子捕获1个中子能产生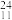 Na和X粒子,则X粒子的组成符号为:
Na和X粒子,则X粒子的组成符号为:(2)NaCN是离子化合物,各原子均满足8电子稳定结构,NaCN 的电子式是
(3)相同条件下,TiF4熔点650K,TiCl4 熔点249K,熔点不同的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】日常消毒应做到安全消毒、有效消毒、绿色消毒。下列是我们常见的几种消毒剂:
①“84”消毒液、②高铁酸钠 、③漂白粉、④
、③漂白粉、④ 、⑤
、⑤ 、⑥碘酒、⑦75%的酒精、⑧过氧乙酸(
、⑥碘酒、⑦75%的酒精、⑧过氧乙酸( ,是一种弱酸)。回答下列问题:
,是一种弱酸)。回答下列问题:
(1)上述物质中属于电解质的是______ (填标号);“84”消毒液的有效成分NaClO在水中的电离方程式为______ 。
(2)已知反应 ,则在该反应的条件下,氧化性:
,则在该反应的条件下,氧化性:
______ (填“>”或“<”) ,当反应中转移电子的数目为
,当反应中转移电子的数目为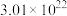 时,生成的氧气在标准状况下的体积为
时,生成的氧气在标准状况下的体积为______ L。
(3)高铁酸钠是一种新型净水剂,在水中发生反应: (胶体)
(胶体)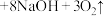 。
。
①该反应中,高铁酸钠中铁元素被______ (填“还原”或“氧化”)。
②某课外活动小组进行 胶体的制备及相关性质实验。
胶体的制备及相关性质实验。
制备:若将饱和 溶液分别滴入下列物质中,能形成胶体的是
溶液分别滴入下列物质中,能形成胶体的是______ (填标号)。
A.冷水 B.沸水 C. 浓溶液 D.
浓溶液 D. 浓溶液
浓溶液
鉴别: 胶体与
胶体与 溶液的鉴别方法是
溶液的鉴别方法是______ 。
 胶体区别于
胶体区别于 溶液最本质的特征是
溶液最本质的特征是______ 。
①“84”消毒液、②高铁酸钠
 、③漂白粉、④
、③漂白粉、④ 、⑤
、⑤ 、⑥碘酒、⑦75%的酒精、⑧过氧乙酸(
、⑥碘酒、⑦75%的酒精、⑧过氧乙酸( ,是一种弱酸)。回答下列问题:
,是一种弱酸)。回答下列问题:(1)上述物质中属于电解质的是
(2)已知反应
 ,则在该反应的条件下,氧化性:
,则在该反应的条件下,氧化性:
 ,当反应中转移电子的数目为
,当反应中转移电子的数目为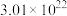 时,生成的氧气在标准状况下的体积为
时,生成的氧气在标准状况下的体积为(3)高铁酸钠是一种新型净水剂,在水中发生反应:
 (胶体)
(胶体)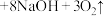 。
。①该反应中,高铁酸钠中铁元素被
②某课外活动小组进行
 胶体的制备及相关性质实验。
胶体的制备及相关性质实验。制备:若将饱和
 溶液分别滴入下列物质中,能形成胶体的是
溶液分别滴入下列物质中,能形成胶体的是A.冷水 B.沸水 C.
 浓溶液 D.
浓溶液 D. 浓溶液
浓溶液鉴别:
 胶体与
胶体与 溶液的鉴别方法是
溶液的鉴别方法是 胶体区别于
胶体区别于 溶液最本质的特征是
溶液最本质的特征是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.下表是生活生产中常见的物质,表中列出了它们的一种主要成分(其中加碘盐是氯化钠中添加适量的KIO3,其他成分未列出)
(1)请你对表中①~⑦的主要成分进行分类,是电解质的是___________ ,是非电解质的是___________ 。(填序号)
(2)写出④在水中的电离方程式___________ 。
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的化学方程式:___________ 。
Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为 。
。
(4)反应中氧化剂与还原剂的物质的量之比为___________ ,其中HNO3反应中显示出来的性质是___________ 。
(5)该反应中的氧化产物为___________ ,每生成11.2L(标准状况下)的NO,转移的电子个数为___________ 。
(6)请用双线桥标出电子转移的情况___________ 。
| 名称 | 天然气 | 白酒 | 醋酸 | 小苏打 | 熟石灰 | 铜线 | 加碘盐 |
| 主要成分 | ①CH4 | ②C2H5OH | ③CH3COOH | ④NaHCO3 | ⑤Ca(OH)2 | ⑥Cu | ⑦NaCl和KIO3混合 |
(2)写出④在水中的电离方程式
(3)写出用④治疗胃酸(主要成分为盐酸)过多涉及的化学方程式:
Ⅱ.铁的化学性质比较活泼,常温下铁可以与稀硝酸发生反应,反应的化学方程式为
 。
。(4)反应中氧化剂与还原剂的物质的量之比为
(5)该反应中的氧化产物为
(6)请用双线桥标出电子转移的情况
您最近一年使用:0次
【推荐3】阅读下列材料,并完成相应填空,制备碘的方法之一是从碘酸盐开始,共分为两步。
(1)第一步的反应为:NaIO3 + 3NaHSO3=NaI + 3NaHSO4,此反应中氧化剂为_______ ,被氧化的元素为________ 。
(2)第二步的反应共包含NaIO3、NaI、I2、Na2SO4、NaHSO4和H2O六种物质,请完成并配平方程式:_________ → ________ 。
(3)第二步反应中氧化产物与还原产物的物质的量之比为________ ,当有1.5mol氧化产物生成时,转移电子的物质的量为________ mol。
(4)要使碘的产率最高,全程投入的NaIO3与NaHSO3的总物质的量之比为_________ 。
(1)第一步的反应为:NaIO3 + 3NaHSO3=NaI + 3NaHSO4,此反应中氧化剂为
(2)第二步的反应共包含NaIO3、NaI、I2、Na2SO4、NaHSO4和H2O六种物质,请完成并配平方程式:
(3)第二步反应中氧化产物与还原产物的物质的量之比为
(4)要使碘的产率最高,全程投入的NaIO3与NaHSO3的总物质的量之比为
您最近一年使用:0次

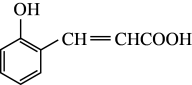 ,写出A中的含氧官能团名称
,写出A中的含氧官能团名称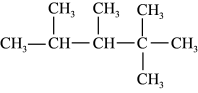 的名称是
的名称是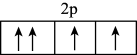 违反了
违反了

