将Cu投入足量的FeCl3的水溶液中,两者发生反应的化学方程式如下:2FeCl3+Cu=2FeCl2+CuCl2
(1)请用双线桥法标出电子转移的方向和数目_______ 。
(2)在该反应中,氧化剂是_______ ,氧化产物是_______ 。
(3)当有0.3mol电子发生转移时,发生反应的Cu的物质的量为_______ 。
(4)请将以上反应改写为离子方程式_______ 。
(1)请用双线桥法标出电子转移的方向和数目
(2)在该反应中,氧化剂是
(3)当有0.3mol电子发生转移时,发生反应的Cu的物质的量为
(4)请将以上反应改写为离子方程式
更新时间:2021-04-17 11:18:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)某学生在实验室做了5个实验
①在铝盐溶液中逐滴加入稀氨水直至过量,
②在明矾溶液中加入NaOH溶液直至过量,
③在强碱性溶液中逐滴加入铝盐溶液直至过量,
④在偏铝酸钠溶液中通入CO2直至过量,
⑤在强酸溶液中逐滴加入偏铝酸钠溶液直至过量。
并根据以上实验画出下列5种图象(纵坐标为沉淀的物质的量,横坐标为溶液中加入物质的量)实验与图象对应关系正确的是:___________ 。
A.①和(a) B.②和(b) C.③和(e) D.④和(c)

(2)已知:氧化性:KMnO4>HNO3;Bi位于周期表中VA,+3价较稳定,NaBiO3溶液为无色。取一定量的Mn(NO3)2溶液依次进行下列实验,现象记录如下。
①滴加适量的NaBiO3溶液,溶液变为紫红色。
②继续滴加适量H2O2,紫红色褪去,并有气泡产生。
③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
④最后通入足量的SO2气体,
请回答下列问题:
(a)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为___________________ ;
(b)实验④中的现象为:___________________ ;
(c)实验②③反应的离子方程式分别是:__________ 、____________ 。
①在铝盐溶液中逐滴加入稀氨水直至过量,
②在明矾溶液中加入NaOH溶液直至过量,
③在强碱性溶液中逐滴加入铝盐溶液直至过量,
④在偏铝酸钠溶液中通入CO2直至过量,
⑤在强酸溶液中逐滴加入偏铝酸钠溶液直至过量。
并根据以上实验画出下列5种图象(纵坐标为沉淀的物质的量,横坐标为溶液中加入物质的量)实验与图象对应关系正确的是:
A.①和(a) B.②和(b) C.③和(e) D.④和(c)

(2)已知:氧化性:KMnO4>HNO3;Bi位于周期表中VA,+3价较稳定,NaBiO3溶液为无色。取一定量的Mn(NO3)2溶液依次进行下列实验,现象记录如下。
①滴加适量的NaBiO3溶液,溶液变为紫红色。
②继续滴加适量H2O2,紫红色褪去,并有气泡产生。
③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
④最后通入足量的SO2气体,
请回答下列问题:
(a)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为
(b)实验④中的现象为:
(c)实验②③反应的离子方程式分别是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】描述下列反应的现象并写出反应的离子方程式
(1)向FeCl3溶液中滴加NaOH溶液,现象____ ,离子方程式___ 。
(2)向NaHCO3溶液中滴加稀H2SO4,现象____ ,离子方程式___ 。
(3)MgSO4溶液和Ba(OH)2溶液混合,现象____ ,离子方程式____ 。
(1)向FeCl3溶液中滴加NaOH溶液,现象
(2)向NaHCO3溶液中滴加稀H2SO4,现象
(3)MgSO4溶液和Ba(OH)2溶液混合,现象
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.有一块镀铜的铁制品,已严重锈蚀[铜锈成分视为 ],铁锈成分视为
],铁锈成分视为 ],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
(1)气体甲的成分是___________ (填化学式),固体乙的成分是___________ (填名称)。
(2)铁发生的反应属于四种基本反应类型中的___________ 。
(3)滤液丙的颜色可能是___________(选填编号)。
(4)确认滤液丙中是否含有亚铁离子,适宜的试剂是___________(选填编号)。
Ⅱ.铁与不同浓度硝酸反应时主要还原产物不同。现将过量铁与一定浓度的硝酸充分反应,测得消耗的铁与被还原的硝酸的物质的量之比为 。
。
(5)假若反应生成的还原产物只有一种,则还原产物是___________ 。
(6)所得溶液与碳酸氢铵溶液混合可获得碳酸亚铁沉淀,同时有气体生成。写出反应生成碳酸亚铁的离子方程式___________ 。
 ],铁锈成分视为
],铁锈成分视为 ],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。(1)气体甲的成分是
(2)铁发生的反应属于四种基本反应类型中的
(3)滤液丙的颜色可能是___________(选填编号)。
| A.棕黄色 | B.蓝色 | C.浅绿色 | D.无色 |
A. 溶液 溶液 | B.NaOH溶液 |
C.KSCN溶液和 溶液 溶液 | D. 淀粉试纸 淀粉试纸 |
Ⅱ.铁与不同浓度硝酸反应时主要还原产物不同。现将过量铁与一定浓度的硝酸充分反应,测得消耗的铁与被还原的硝酸的物质的量之比为
 。
。(5)假若反应生成的还原产物只有一种,则还原产物是
(6)所得溶液与碳酸氢铵溶液混合可获得碳酸亚铁沉淀,同时有气体生成。写出反应生成碳酸亚铁的离子方程式
您最近一年使用:0次
【推荐1】氧化还原反应在生产生活中有很多实际应用:
Ⅰ.二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;
②2SO2+SeO2+2H2O=Se+2SO +4H+。
+4H+。
(1)Se与浓H2SO4的反应中,氧化剂是_______ ,氧化产物是_______ 。
(2)依据反应①判断氧化性强弱是:SeO2_______ 浓H2SO4(填大于、小于或等于)
(3)用双线桥法标出反应②电子转移的方向和数目:_______ 。
Ⅱ.对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(4)含氰废水中的CN-有剧毒。在微生物的作用下,CN-能够被氧气氧化成HCO ,同时生成NH3,该反应的离子方程式为
,同时生成NH3,该反应的离子方程式为_______ 。
(5)白磷有剧毒,被白磷污染的物品可用硫酸铜溶液浸泡清洗,其原理为:11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4。该反应中,被10个CuSO4氧化的P的数目为_______ 。
Ⅰ.二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;
②2SO2+SeO2+2H2O=Se+2SO
 +4H+。
+4H+。(1)Se与浓H2SO4的反应中,氧化剂是
(2)依据反应①判断氧化性强弱是:SeO2
(3)用双线桥法标出反应②电子转移的方向和数目:
Ⅱ.对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(4)含氰废水中的CN-有剧毒。在微生物的作用下,CN-能够被氧气氧化成HCO
 ,同时生成NH3,该反应的离子方程式为
,同时生成NH3,该反应的离子方程式为(5)白磷有剧毒,被白磷污染的物品可用硫酸铜溶液浸泡清洗,其原理为:11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4。该反应中,被10个CuSO4氧化的P的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求完成下列试题
(1)用单线桥标出下列反应电子转移的方向和数目
2Na+2H2O=2NaOH+H2↑____
(2)用双线桥标出下列反应化合价升降、电子得失、被氧化或被还原
C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O_____
(3)写出下列物质在水溶液中的电离方程式。
CH3COOH:_________ 。
KAl(SO4)2:_______________ 。
(4)写出硫酸铜溶液与氢氧化钡溶液反应的离子方程式:__________
(1)用单线桥标出下列反应电子转移的方向和数目
2Na+2H2O=2NaOH+H2↑
(2)用双线桥标出下列反应化合价升降、电子得失、被氧化或被还原
C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O(3)写出下列物质在水溶液中的电离方程式。
CH3COOH:
KAl(SO4)2:
(4)写出硫酸铜溶液与氢氧化钡溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为3ClO-+2Fe3++xOH-=2 +3Cl-+yH2O。
+3Cl-+yH2O。
(1)上述反应中的x=___________ ,y=___________ 。
(2)上述反应中氧化剂为___________ ;还原产物为___________ 。
(3)由上述反应可知,氧化性强弱:ClO-___________  (填“>”或“<”,下同);还原性强弱:Cl-
(填“>”或“<”,下同);还原性强弱:Cl-_________ Fe3+。
(4)请用单线桥法表示该反应中电子的转移情况:___________ 。
 +3Cl-+yH2O。
+3Cl-+yH2O。(1)上述反应中的x=
(2)上述反应中氧化剂为
(3)由上述反应可知,氧化性强弱:ClO-
 (填“>”或“<”,下同);还原性强弱:Cl-
(填“>”或“<”,下同);还原性强弱:Cl-(4)请用单线桥法表示该反应中电子的转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】双氧水和84消毒液是生活中常用的两种消毒剂,了解物质的性质是科学合理使用化学品的基础和前提。请回答下列问题:
(1)某同学设计如下实验研究H2O2的性质:
① 从理论上看H2O2既有氧化性又有还原性,具有还原性的原因是______ 。
② 能证明H2O2具有还原性的实验是______ (填序号)。可作为证据的实验现象是______ (填字母序号)。
(2)84消毒液的有效成分为NaClO
① 将Cl2通入NaOH溶液中可制得84消毒液,化学反应方程式为:______
② 84消毒液不能用于钢制器具的消毒,原因是NaClO具有______ 性。
③ 84消毒液的溶液在浸泡餐具过程中,因吸收空气中CO2消毒杀菌能力增强,该反应说明酸性强弱为______
(3)2016年巴西奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
① 该反应说明氧化性:NaClO______ H2O2的(填“>”或“<”)。
② 当有0.1mol O2生成时,转移电子______ mol
(1)某同学设计如下实验研究H2O2的性质:
| 序号 | 实验 | 实验现象 |
| ⅰ | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a. 溶液紫色褪去 b. 有大量气泡产生 |
| ⅱ | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c. 溶液变蓝 |
① 从理论上看H2O2既有氧化性又有还原性,具有还原性的原因是
② 能证明H2O2具有还原性的实验是
(2)84消毒液的有效成分为NaClO
① 将Cl2通入NaOH溶液中可制得84消毒液,化学反应方程式为:
② 84消毒液不能用于钢制器具的消毒,原因是NaClO具有
③ 84消毒液的溶液在浸泡餐具过程中,因吸收空气中CO2消毒杀菌能力增强,该反应说明酸性强弱为
(3)2016年巴西奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
① 该反应说明氧化性:NaClO
② 当有0.1mol O2生成时,转移电子
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将过量的铜置入一定量的浓硝酸中,充分反应后放出11.2 L气体(标准状况下),试回答下列问题:
(1)反应放出的气体中,含有_____________ (写化学式);
(2)写出反应过程中的的化学方程式:___________________________ ;
(3)若有19.2g铜溶解,则参加反应的HNO3的物质的量__________ 被还原HNO3的质量为______________
(1)反应放出的气体中,含有
(2)写出反应过程中的的化学方程式:
(3)若有19.2g铜溶解,则参加反应的HNO3的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】NOx(主要指NO和NO2)是大气主要污染物之一、有效去除大气中的NOx是环境保护的重要课题。
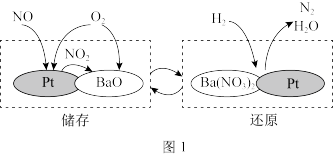
(1)NSR储存还原时,NO的储存和还原在不同时段交替进行,如图1所示。
①NO储存转化为Ba(NO3)2过程中,参加反应的NO和O2的物质的量之比为___________ 。
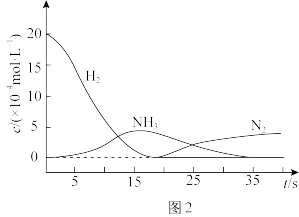
②H2还原Ba(NO3)2的过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。第一步反应的化学方程式为___________ 。
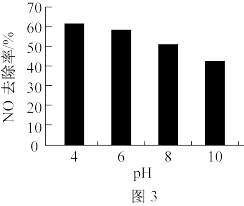
(2)NaClO溶液能有效去除NO。25℃时,NO的去除率随pH的变化如图3所示(用盐酸调节pH);pH=4时,NO的去除率随温度的变化如图4所示。

①25℃时,随着pH降低,NO脱除率增大的原因是___________ 。
②pH=4时,60~80℃间NO脱除率下降的原因是___________ 。
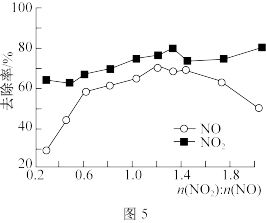
(3)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入Ca(OH)2悬浊液中,改变n(NO2)︰n(NO)的值,NOx的去除率如图5所示。
已知:a.NOx的去除率=1-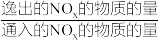 ×100%
×100%
b.NO与Ca(OH)2不反应
①当n(NO2)︰n(NO)在0.3~0.5之间,NO与NO2吸收转化为Ca(NO2)2反应的离子方程式为___________ 。
②当n(NO2)︰n(NO)大于1.4时,NO2的去除率升高,但NO的去除率却降低。其可能的原因是___________ 。
(1)NSR储存还原时,NO的储存和还原在不同时段交替进行,如图1所示。
①NO储存转化为Ba(NO3)2过程中,参加反应的NO和O2的物质的量之比为
②H2还原Ba(NO3)2的过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。第一步反应的化学方程式为
(2)NaClO溶液能有效去除NO。25℃时,NO的去除率随pH的变化如图3所示(用盐酸调节pH);pH=4时,NO的去除率随温度的变化如图4所示。




①25℃时,随着pH降低,NO脱除率增大的原因是
②pH=4时,60~80℃间NO脱除率下降的原因是
(3)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入Ca(OH)2悬浊液中,改变n(NO2)︰n(NO)的值,NOx的去除率如图5所示。

已知:a.NOx的去除率=1-
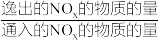 ×100%
×100%b.NO与Ca(OH)2不反应
①当n(NO2)︰n(NO)在0.3~0.5之间,NO与NO2吸收转化为Ca(NO2)2反应的离子方程式为
②当n(NO2)︰n(NO)大于1.4时,NO2的去除率升高,但NO的去除率却降低。其可能的原因是
您最近一年使用:0次



